graduirana pipeta → graduated pipette
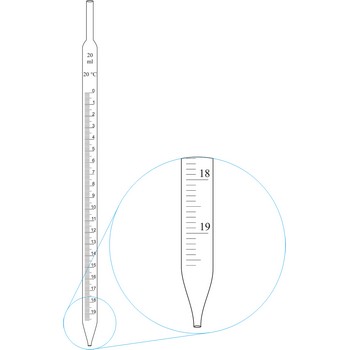
Graduirane pipete (Mohrove pipete) imaju skalu razdijeljenu na jedinice i desetinke mililitra. Zbog svog širokog vrata manje su precizne od prijenosnih pipeta i koriste se pri uzimanju volumena otopina čija točnost ne mora biti velika. Usisavanjem (ustima, propipetom ili vodenom sisaljkom) povuče se tekućina malo iznad oznake i otvor pipete zatvori vrškom kažiprsta. Obriše se vanjska stjenka pipete i laganim popuštanjem kažiprsta tekućina se ispusti do oznake 0. Pipeta se prazni tako da maknemo kažiprst i pustimo da tekućina slobodno istječe do željene oznake.
grafit → graphite
Grafit je alotrop ugljika. Dobar je vodič topline i elektriciteta. U grafitu atomi su povezani u heksagonalne prstenove koji su složeni u slojevima. Kako ovi slojevi lako klize jedan preko drugog grafit se često koristi kao kruto mazivo. Sintetski grafit dobiva se zagrijavanjem smjese gline (aluminijeva silikata) i koksa u procesu koji je izumio američki kemičar Edward Goodrich Acheson (1856.–1931.). U reakciji nastaje silicijev karbid koji pri 4150 °C gubi silicij ostavljajući čisti grafit.
Gratzelova sunčeva ćelija → Gratzel solar cell
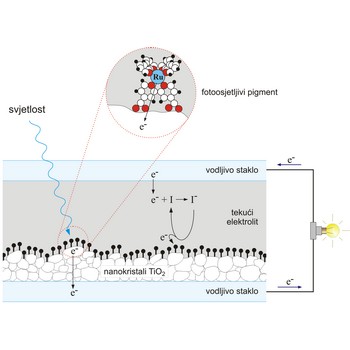
Grätzelova sunčeva ćelija je fotoelektrokemijska ćelija koju je razvio Michael Grätzel sa suradnicima. Oponaša djelomice prirodnu sunčevu ćeliju, koja omogućava biljkama da ostvare fotosintezu. U prirodnoj sunčevoj ćeliji molekule klorofila apsorbiraju svjetlost i to najjače u crvenom i plavom dijelu spektra, dok se zelena svjetlost reflektira. Apsorbirana energija dovoljna je za izbacivanje elektrona iz pobuđenog klorofila. U prijenosu tog naboja, sudjeluju potom druge molekule. U Grätzelovoj ćeliji su, također, za stvaranje naboja apsorpcijom svjetlosti i prijenos tog naboja "zaduženi" različiti dijelovi ćelije.
Na vodljivo staklo nanesen je sloj nanokristala poluvodiča TiO2 čija je površina jako velika. Na TiO2 nanesen je fotoosjetljivi pigment koji čine rutenijevi ioni povezani s organskim molekulama koje jako apsorbiraju vidljivu svjetlost. Fotopobuđeni elektroni prelaze s rutenijevih iona na kristalite TiO2, koji ih odvode daleko od iona-donora. Čitav sustav uronjen je u tekući jodidni elektrolit koji preuzima elektrone s elektrode i prenosi ih na rutenijeve ione kako bi se nastavio proces apsorpcije svjetlosti.
Efikasnost ovih ćelija iznosi oko 10 % i raste u difuznoj svjetlosti, tj. za oblačna vremena.
Haberov proces → Haber process
Haberov proces je industrijski postupak sinteze amonijaka iz dušika i vodika:
Reakcija je egzotermna i reverzibilna, tako da se prinos na amonijaku povećava na nižim temperaturama. Brzina reakcije je previše mala na normalnoj temperaturi, pa se reakcija provodi pri optimalnoj temperatura od oko 450 °C. U reakciji se kao katalizator koristi željezo s aluminijevim oksidom kao promotorom. Povišenjem tlaka reakcija se pomiče u smjeru nastajanja amonijaka, pa se koristi tlak od 250 atmosfera. Amonijak se uklanja iz reaktora čime se reakcija pomiče u smjeru nastajanja produkata. Kao izvor vodika u originalnom procesu koristio se vodeni plin, dok se danas koristi vodik dobiven reformiranjem zemnog plina.
Proces je vrlo važan jer je to jedini industrijski način fiksacije dušika iz zraka u svrhu dobivanja umjetnih gnojiva i eksploziva. Postupak je razvio 1908. njemački kemičar Fritza Haber (1868.-1934.), a za industrijsku primjenu prilagodio ga je Carl Bosh (1874.-1940.), te se postupak još naziva Haber-Boshov postupak.
polučlanak → half-cell
Polučlanak je dio galvanskog članka u kojem dolazi do oksidacije ili do redukcije elementa u dodiru s vodom ili vodenom otopinom jednog od njegovih spojeva.
halogenirani ugljikovodik → halocarbon
Halogenirani ugljikovodici su spojevi koji sadržavaju samo ugljik, jedan ili više halogena, i ponekad vodik, primjerice ugljikov tetraklorid ili tetraklorometan (CCl4), tetrabromometan (CBr4). Niži članovi različitih homolognih nizova koriste se kao sredstva za hlađenje, sredstva za gašenje požara i kao sredstva za pjenjenje poliuretanske pjene. Polimerizacijom halogeniranih ugljikovodika nastaju plastične mase koje karakterizira visoka kemijska otpornost, visoka električna otpornost i dobra toplinska stabilnost.
helij → helium
Helij su 1868. godine otkrili Pierre Jules César Janssen (Francuska) i Sir William Ramsay (Škotska). Ime mu dolazi od grčke riječi helios što znači sunce. To je plin bez boje i mirisa koji se u prirodi pojavljuje kao jednoatomni. Helij je kemijski inertan, nezapaljivi plin koji se ne spaja s drugim elementima. Prvi put pronađen je u spektru sunčevog zračenja. Helij je drugi element, iza vodika, po rasprostranjenosti u cijelom svemiru. Nastaje raspadom radioaktivnih elemenata, a industrijski se proizvodi iz zemnog plina iz Teksasa (SAD) u kojem ga ima oko 2 % (volumna). Upotrebljava se za punjenje balona, a smjesa koja se sastoji od 21 % O2 i 79 % He koristi se kao zamjena za zrak kod ronjenja na velikim dubinama.
Hessov zakon → Hesse’s law
Zakonitost termokemijskih pojava otkrio je 1840. ruski kemičar švicarskog porijekla Germain Henri Hess (1802.-1850.). Njegov zakon glasi: Reakcijska toplina neke kemijske promjene ne ovisi o putu kojim reakciju vodimo, već samo o početnom i konačnom stanju sustava. Hessov zakon poznat je i kao zakon o stalnosti zbroja toplina reakcije.
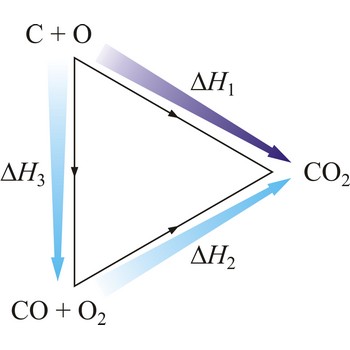
Na primjer, eksperimentalno je određena entalpija oksidacije grafita u ugljikov dioksid i ugljikova monoksida u ugljikov dioksid. Zbog ravnoteže
nije moguće odrediti entalpiju oksidacije grafita u ugljikov monoksid. Međutim, reakcijska toplina te reakcije može se izračunati primjenom Hessovog zakona.
| C(s) + O2(g) →← CO2(g) | ΔrH1 = -393 kJ mol-1 |
| CO(g) + 1/2O2(g) →← CO2(g) | ΔrH2 = -283 kJ mol-1 |
| C(s) + 1/2O2(g) →← CO(g) | ΔrH3 = -110 kJ mol-1 |
hidratacija → hydration
Hidratacija je proces vezanja molekula vode na ione ion-dipolnom vezom. Ioni u vodenoj otopini nalaze se obavijeni slojem molekula vode. Hidrataciju nekog spoja A+B- možemo prikazati
Hidratacijom se oslobađa toplina hidratacije koja je to veća što je ion jače hidratiziran.
hidroliza → hydrolysis
Hidroliza je kemijska reakcija u kojoj voda reagira s drugom tvari pri čemu nastaju dvije ili više novih tvari. To uključuje ionizaciju molekula vode kao i cijepanje spoja hidrolizom, primjerice
Primjeri su pretvaranje škroba u glukozu pomoću vode u prisutnosti odgovarajućih katalizatora i reakcije iona otopljenih soli s vodom pri čemu nastaju različiti produkti, kao na primjer kiseline, kompleksni ioni, itd.
Hidroliza je proces suprotan neutralizaciji i esterifikaciji.
Citiranje ove stranice:
Generalić, Eni. "Omekšivač vode." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav