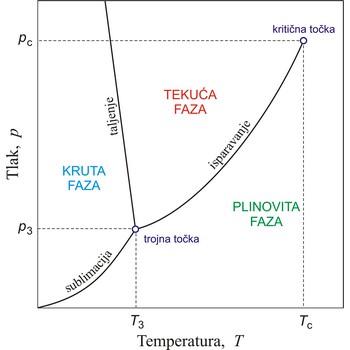
fazni dijagram → phase diagram
Ravnotežna stanja koja se uspostavljaju, pri određenim uvjetima, između pojedinih agregatnih stanja ili faza prikazuju se faznim dijagramom ili dijagramom stanja.
Krivulje na faznom dijagramu prikazuju ravnotežna stanja između dviju faza. Točku u kojoj su sve tri faze u ravnoteži nazivamo trojna točka. Krivulja isparavanja završava u kritičnoj točki. Iznad te temperature (kritična temperatura) ni u kojim uvjetima ne može se vodena para prevesti u tekuće stanje.
fosforescencija → phosphorescence
Fosforescencija je pojava svijetljenje tijela koja traje i nakon ukidanja izvora energije. Za razliku od fluorescencije, u kojoj se apsorbirana energija skoro trenutačno spontano emitira nakon pobude (potrebno je manje od 10-8 sekunda), fosforesciranje zahtijeva dodatnu energiju za povratak u osnovno stanje, što može trajati od nekoliko milisekundi pa do nekoliko dana ili godina, ovisno o okolnostima.
plazma → plasma
Plazma je visoko ionizirani plin u kojem je naboj elektrona uravnotežen s nabojem pozitivnih iona, tako da je sustav u cjelini električno neutralan. Plazma se stvara na način da se plinovi izlažu električnom ili elektromagnetskom polju pri niskom tlaku. U proizvodnji poluvodiča koristi se za graviranje (jetkanje) i deponiranje tankog filma (ekscitirano stanje je čini vreoma reaktivnom). U svakidašnjem životu plazma se koriste za dobivanje svjetla u žaruljama, neonkama i plavim klopkama za kukce.
potencijalna energija → potential energy
Potencijalna energija (Ep) jest energija pohranjena unutar tijela ili sustava kao posljedica mjesta, oblika ili stanja (uključuje gravitacijsku, električnu, nuklearnu i kemijsku energiju). Gravitacijska potencijalna energija je energija povezana sa stanjem razdvojenosti tijela koja se međusobno privlače gravitacijskom silom. Elastična potencijalna energija povezana je sa stanjem sabijenosti ili rastegnutosti elastičnog tijela (poput opruge). Toplinska energija povezana je s nasumičnim gibanjem atoma i molekula u tijelu.
zaštita žrtvovanom elektrodom → sacrificial protection
Zaštita žrtvovanom elektrodom zaštita je željeza ili čelika protiv korozije koristeći reaktivniji metal. Komadići cinkove ili magnezijeve slitine pričvrste se za tijela pumpi ili cijevi. Zaštićeni metal je katoda i ne korodira dok anoda korodira. Ovakvi se predmeti zovu žrtvovane anode. Žrtvovane elektrode moraju se periodično zamjenjivati ovisno o brzini trošenja.
Željezna cijev spojena je s reaktivnijim metalom, kao što je magnezij, koji će donirati svoje elektrone i sprječiti hrđanje željeza. Eventualno oksidirano željezo će se reducirati nazad u elementarno stanje.
zasićena mast → saturated fat
Zasićene masti u čvrstom su stanju pri sobnoj temperaturi. Zasićene masti u hranu dolaze uglavnom iz životinjskih izvora (govedina, mlijeko i mliječni proizvodi, crveno meso) ali također i iz tropskih biljnih ulja (kokosovog ili palminog ulja).
zasićena otopina → saturated solution
Zasićena otopina je otopina koja sadrži maksimalno moguću količinu otopljene tvari. Kada je otopina zasićena, postignuto je stanje ravnoteže jer je brzina otapajnja čvrste tvari i brzina rekristalizacije ista. Količina tvari koja se može otopiti varira s temperaturom; hladne otopine obično sadrže manje otopljene tvari nego vruće otopine. Plinovi su topljiviji u hladnim nego u vrućim tekućinama.
Koncentracija tvari u takvoj zasićenoj otopini naziva se topljivošću te tvari pri danoj temperaturi.
sekunda → second
Sekunda (s) je SI jedinica za vrijeme.
To je trajanje 9 192 631 770 perioda zračenja koje odgovara prijelazu između dvaju hiperfinih nivoa (od F = 4, mF = 0 do F = 3, mF = 0) osnovnog stanja atoma cezija 133 (133Cs). Periodu definiramo kao vrijeme potrebno da svjetlost prevali put koji odgovara jednoj valnoj duljini.
sumpor → sulfur
Sumpor je poznat od davnih vremena. Ime mu potječe od sanskrtskog sulva-ari što znači neprijatelj bakra. To je žuti kristaličan ili amorfan prah bez okusa i mirisa koji se ne otapa u vodi ali se otapa u ugljikovom disulfidu (CS2). Sumpor na zraku gori plavičastim plamenom. Osim u elementarnom stanju sumpor se u prirodi pojavljuje u obliku sulfida i sulfata. Od sulfidnih minerali najčešći su pirit (FeS2), halkopirit (CuFeS2) i sfalerit (ZnS), a od sulfatnih gips (CaSO4·2H2O). Upotrebljava se za proizvodnju sulfatne kiseline, vulkanizaciju gume i proizvodnju baruta.
superkritični ugljikov dioksid → supercritical carbon dioxide
Superkritični ugljikov dioksid (scCO2) moćno je, jeftino, netoksično i ekološki prihvatljivo otapalo. Kada se upotrebljava u superkritičnom stanju (iznad 74 bar i 31 °C) ima sličan otapajući potencijal kao i njegovi organski suparnici, ugljikovodici i klorirana otapala. Superkritični ugljikov dioksid je jedno od rijetkih otapala koje se može bez ograničenja upotrebljavati u prehrambenoj industriji.
Citiranje ove stranice:
Generalić, Eni. "Nascentno stanje." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav