glikogen → glycogen
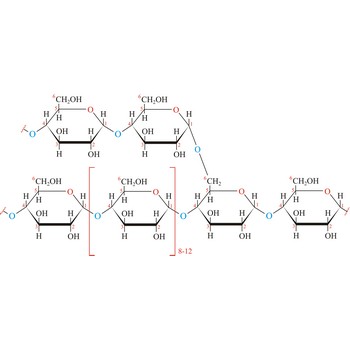
Glikogen ili animalni škrob je polisaharid koji životinje (među njima i čovjek) koriste za skladištenje molekula glukoze. Organizam stvara glikogen iz viška glukoze i pohranjuje ga u jetri i mišićnom tkivu. Struktura mu je slična strukturi amilopektina iz škroba, ali je mnogo razgranatiji i veće relativne molekularne mase (može se sastojati od preko 100 000 glukoznih jedinica). Osnovni lanci glikogena sastoje se od molekula glukozne povezanih α(1→4) glikozidnim vezama. Pobočni lanci, vezani α(1→6) glikozidnim vezama, granaju se na približno svakih 10 ostataka glukoze (kod amilopektina je grananje na približno svakih 25 glukoznih jedinica). Pri napornom radu glikogen se cijepa nazad u glukozu a razgranata struktura omogućuje enzimima da hidrolizu započnu na više mjesta i tako brzo stvore organizmu potrebnu glukozu.
glikozid → glycoside
Glikozidi su skupina organskih spojeva u kojoj je šećerna skupina (glikon), preko svog anomernog ugljikovog atoma, glikozidnom vezom povezana s nekom drugom skupinom - aglikonom. Prema IUPAC-ovoj definiciji svi disaharidi i polisaharidi su također glikozidi u kojima je aglikon također šećer.
Vodene otopine cikličkih poluacetala ili poluketala šećera spontano uspostavljaju ravnotežu između α i β anomera koji prelaze jedan u drugi preko otvorenog aldehidnog oblika. Međutim, kada se glikozidna veza formira anomerna konfiguracija ostaje zaključana. α i β glikozidi imaju različita kemijska, fizikalna i biološka svojstva.
Naziv glikozid je naknadno proširen tako da obuhvaća ne samo veze između anomernog ugljikovog atoma, i -OR skupine već i njegove veze sa -SR (tioglikozidi) i -SeR (selenoglikozidi). Nazivi N-glikozid (za anomerni C-atom vezan na -NR1R2) i C-glikozid (za anomerni C-atom vezan na -CR1R2R3), iako su široko rasprostranjeni u biokemijskoj literaturi, pogrešni su i ne bi ih se smjelo koristiti.
glikozidna veza → glycosidic bond
Glikozidna veza je veza između glikozidne skupine, strukture nastale uklanjanjem hidroksilne skupine s anomernog ugljikovog atoma, i -OR skupine (koja i sama može biti izvedena iz šećera) ili njenih halkogenih analoga (RS- i RSe-). Imena N-glikozidi i C-glikozidi su pogrešna i ne ih se smjelo koristiti. Glikozidna veza može biti α ili β ovisno o konfiguraciji anomernog ugljikovog atoma prije nastajanja glikozidne veze. Jednom kad glikozidna veza nastane anomerna konfiguracija se "zaključava". U imenu spoja glikozidna veza označava se kao α(1→4), β(1→4), α(1→6) itd. I škrob i celuloza sačinjeni su samo od glukoze ali u celulozi molekule glukoze povezane su β(1→4)-glikozidnom vezom a škroba α(1→4)-glikozidnom vezom.
zlato → gold
Zlato je poznato od davnih vremena (~3000. godine prije Krista). Simbol elementa dolazi od latinskog naziva za zlato - aurum. To je sjajni, žuti metal. Mekan, kovak i savitljiv te se može izvući u listiće debele samo 10-5 mm. Ne zraku je stabilno i ne reagira s kisikom ni na kojoj temperaturi. Ne otapa se u kiselinama ni lužinama. Otapa se jedino u zlatotopci (HNO3:HCl=1:3) i u cijanidnim otopinama koje sadrže kisik, zbog stvaranja kompleksa s kloridom odnosno cijanidom. Zlato je rijedak element i ima ga deset puta manje od srebra. U prirodi se obično nalazi u elementarnom stanju u kremenim žilama ili pijesku rijeka. Upotrebljava se za izradu nakita, novca, zubnih proteza kao i za elektroničke krugove i kontakte.
Goldschmidtov postupak → Goldschmidt process
Goldschmidtov postupak (termitni postupak) je postupak dobivanja čistih metala redukcijom njihovih oksida aluminijem u prahu. Skoro se svi metalni oksidi mogu reducirati ovom metodom. Glavna iznimka je magnezijev oksid. Termitni postupak razvio je 1893. njemački kemičar Hans Goldschmidt (1861.-1923.).
Goldschmidt je brzo uvidio da se osim dobivanja čistih metala termitni postupak može upotrijebiti i za zavarivanje metala, primjerice željezničkih tračnica. Postupak je poznat kao termitno zavarivanje (aluminotermijsko zavarivanje).
graduirana pipeta → graduated pipette
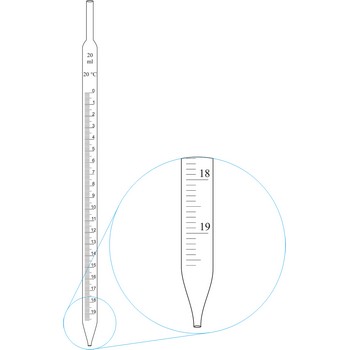
Graduirane pipete (Mohrove pipete) imaju skalu razdijeljenu na jedinice i desetinke mililitra. Zbog svog širokog vrata manje su precizne od prijenosnih pipeta i koriste se pri uzimanju volumena otopina čija točnost ne mora biti velika. Usisavanjem (ustima, propipetom ili vodenom sisaljkom) povuče se tekućina malo iznad oznake i otvor pipete zatvori vrškom kažiprsta. Obriše se vanjska stjenka pipete i laganim popuštanjem kažiprsta tekućina se ispusti do oznake 0. Pipeta se prazni tako da maknemo kažiprst i pustimo da tekućina slobodno istječe do željene oznake.
grafit → graphite
Grafit je alotrop ugljika. Dobar je vodič topline i elektriciteta. U grafitu atomi su povezani u heksagonalne prstenove koji su složeni u slojevima. Kako ovi slojevi lako klize jedan preko drugog grafit se često koristi kao kruto mazivo. Sintetski grafit dobiva se zagrijavanjem smjese gline (aluminijeva silikata) i koksa u procesu koji je izumio američki kemičar Edward Goodrich Acheson (1856.–1931.). U reakciji nastaje silicijev karbid koji pri 4150 °C gubi silicij ostavljajući čisti grafit.
Gratzelova sunčeva ćelija → Gratzel solar cell
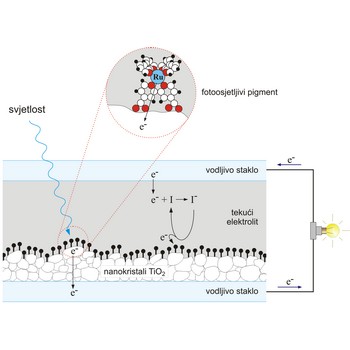
Grätzelova sunčeva ćelija je fotoelektrokemijska ćelija koju je razvio Michael Grätzel sa suradnicima. Oponaša djelomice prirodnu sunčevu ćeliju, koja omogućava biljkama da ostvare fotosintezu. U prirodnoj sunčevoj ćeliji molekule klorofila apsorbiraju svjetlost i to najjače u crvenom i plavom dijelu spektra, dok se zelena svjetlost reflektira. Apsorbirana energija dovoljna je za izbacivanje elektrona iz pobuđenog klorofila. U prijenosu tog naboja, sudjeluju potom druge molekule. U Grätzelovoj ćeliji su, također, za stvaranje naboja apsorpcijom svjetlosti i prijenos tog naboja "zaduženi" različiti dijelovi ćelije.
Na vodljivo staklo nanesen je sloj nanokristala poluvodiča TiO2 čija je površina jako velika. Na TiO2 nanesen je fotoosjetljivi pigment koji čine rutenijevi ioni povezani s organskim molekulama koje jako apsorbiraju vidljivu svjetlost. Fotopobuđeni elektroni prelaze s rutenijevih iona na kristalite TiO2, koji ih odvode daleko od iona-donora. Čitav sustav uronjen je u tekući jodidni elektrolit koji preuzima elektrone s elektrode i prenosi ih na rutenijeve ione kako bi se nastavio proces apsorpcije svjetlosti.
Efikasnost ovih ćelija iznosi oko 10 % i raste u difuznoj svjetlosti, tj. za oblačna vremena.
skupine periodnog sustava → groups in periodic system of elements
Periodni sustav elemenata podijeljen je u 18 skupina kemijskih elemenata. Elementi iste skupine imaju isti broj valentnih elektrona i slična kemijska svojstva. Elementi glavnih skupina su u 1., 2. i od 13. do 18. skupine. Različite skupine elemenata mogu se imenovati prema prvom elementu u skupini (elementi borove skupine, elementi ugljikove skupine) ili imaju posebna imena (plemeniti plinovi, halogeni elementi, halkogeni elementi, zemnoalkalijski metali, alkalijski metali).
Citiranje ove stranice:
Generalić, Eni. "Rare earth elements." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav