klorinitet → chlorinity
Klorinitet (simbol Cl) je definiran kao ukupna količina halida (klorida, bromida i jodida) u 1 kg mora, a da su pri tome jodid i bromid zamijenjeni ekvivalentnom količinom klorida. Kako bi se napravio neovisnim o promjenama atomskih masa halida, klorinitet se danas definira kao masa čistog srebra potrebna da se istalože svi kloridi, bromidi i jodidi pomnožena s 0.37285233. Klorinitet se općenito određuje kako bi se izračunala slanost (salinitet) mora.
Klorinitet se određuje Mohrovom metodom, jednom od najstarijih metoda titracije - uveo ju je 1856. njemački kemičar Karl Friedrich Mohr (1806.-1879.), titracijom uzorka mora sa standardnom otopinom srebrovog nitrata (AgNO3) uz kalijev kromat (K2CrO4) kao indikator.
pri tome se uz AgCl talože još i AgBr i AgI.
Problem kod Mhorove titracije je u tome što srebrov nitrat nije primarni standard. Kako bi ovo izbjegao i omogućio da sva mjerenja saliniteta budu usporediva, predsjednik Međunarodnog povjerenstva za istraživanje mora (ICES, International Council for the Exploration of the Sea), danski fizičar Martin Knudsen (1871.-1949.) definirao je kao standard Normalnu vodu (Eau de mer Normale) stalnog sastava s točno određenim klorinitetom (oko 19.38 ‰). Ova voda je potom korištena za standardizaciju otopine srebrova nitrata. Na taj način sva određivanja kloriniteta referirala su se na isti standard što je omogućilo da svi rezultati budu usporedivi. Upotrebom Normalne vode, Knudsenove pipete i birete za analizu te Hidrografskih tablica dobivali su se rezultati točnosti usporedive onima dobivenim gravimetrijom.
Mjerenjem saliniteta i kloriniteta u devet uzoraka mora iz različitih dijelova svijeta Knudsen je, 1889., došao do empirijske formule za određivanje saliniteta:
Ova formula koristila se do 1962., kada je Zajedničko vijeće za oceanografske tablice i standarde (JPOTS, Joint Panel for Oceanographic Tables and Standards) odredilo novu konstantu proporcionalnosti u Knudsenovoj formuli
sastav oceanske vode → composition of ocean water
More je nezasićena homogena otopina koja se sastoji od vode kao otapala (96.5 %), otopljene soli (3.5 %), manjih količina partikularne tvari, otopljenih plinova i organskih sastojaka. Odnosi glavnih konstituenata oceanske vode su skoro konstantni u svim oceanima. Salinitet (ukupna koncentracija otopljenih soli) i koncentracija pojedinih konstituenata dana je u psu jedinicama (practical salinity units). U većini slučajeva može se pretpostaviti da su psu i stara jedinica ‰ sinonimi.
Prosječni sastav oceanske vode dan je u tablici:
| konstituent | udio ukupnih soli |
|---|---|
| klor | 55.3 % |
| natrij | 30.8 % |
| magnezij | 3.7 % |
| sumpor | 2.6 % |
| kalcij | 1.2 % |
| kalij | 1.1 % |
kristalni sustav → crystal system
Kristalni sustav je metoda razvrstanja kristalnih tvari na osnovu njihove jedinične ćelije. Postoji sedam jedinstvenih kristalnih sustava i po redu opadanja simetrije to su: kubični (ili teseralni), heksagonski, tetragonski, trigonski (ili romboedarski), rompski (ili ortorompski), monoklinski i triklinski.
|
Kristalni sustav
|
Jedinična ćelija
|
Odnos stranica i kutova u jediničnoj ćeliji |
|
kubični |
 |
a=b=c α=β=γ=90° |
|
heksagonski |
 |
a≠c α=γ=90° β=120° |
|
tetragonski |
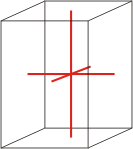 |
a=b≠c α=β=γ=90° |
|
romboedarski |
 |
a=b=c α=β=γ≠90° |
|
ortorompski |
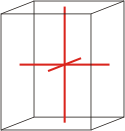 |
a≠b≠c α=β=γ=90° |
|
monoklinski |
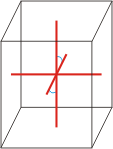 |
a≠b≠c α=γ=90°≠β |
|
triklinski |
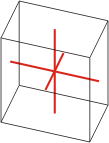 |
a≠b≠c α≠β≠γ≠90° |
Daniellov članak → Daniell cell
Britanski kemičar John Frederic Daniell (1790-1845) predstavio je 1836. poboljšani naponski članak koji je davao stalnu struju tijekom rada. Daniellov članak galvanski je članak u kojem su anoda (cink) i katoda (bakar) uronjeni u sulfatno kiselu otopinu svojih iona. Otopine su razdvojene pregradom od porozne gline. U članku se spontano odvija redukcija Cu2+ iona i oksidacija cinka u Zn2+ uz elektromotornu silu od 1.100 V.
Zn(s) |
→ | Zn2+ + 2e- |
+0.763 V |
Cu2+ + 2e- |
→ | Cu(s) |
+0.337 V |
Zn(s) + Cu2+ |
→← | Zn2+ + Cu(s) |
+1.100 V |
deionizirana voda → deionised water
Deionizirana voda dobije se uklanjanjem otopljenih soli ionskim izmjenjivačima, a koristi se kao zamjena za destiliranu vodu.
| Tip vode | Vodljivost / µScm-1 |
|---|---|
| Ultračista voda | 0.05 |
| Destilirana voda | 0.5 |
| Voda iz slavine | 50 |
| Oceanska voda | 50 000 |
dielektrična konstanta → dielectric constant
Dielektrična konstanta ili permitivnost (ε) jest mjera sposobnosti tvari da smanji elektrostatske sile između dva nabijena tijela. Što je vrijednost manja, smanjenje je veće.
Dielektrična konstanta za različite materijale pri 20 °C iznosi:
| vakuum | 1 |
| zrak | 1.00058 |
| staklo | 3 |
| benzen | 2.3 |
| octena kiselina | 6.2 |
| amonijak | 15.5 |
| etanol | 25 |
| glicerol | 56 |
| voda | 81 |
Vrijednost dielektrične konstante opada s porastom temperature.
Zemljina kora → Earth’s crust
Zemljina kora je vanjski površinski sloj planeta Zemlje iznad Mohorovićeva diskontinuiteta. Prosječna debljina Zemljine kore iznosi 35 km na kontinentima i oko 7 km ispod oceanskog dna. Približni sastav joj je:
| Element | Postotak (%) |
|---|---|
| kisik | 47 |
| silicij | 28 |
| aluminij | 8 |
| željezo | 4.5 |
| kalcij | 3.5 |
| natrij | 2.5 |
| kalij | 2.5 |
| magnezij | 2.2 |
elektronski afinitet → electron affinity
Elektronski afinitet je promjena energije koja se dešava kada atom, molekula ili radikal primi elektron. Za atom ili molekulu X može se reakcija pisati kao
Jedinica za elektronski afinitet jest kJ, ali se češće izražava u elektronvoltima.
Elektronski afinitet u istoj skupini opada s porastom atomskog broja, a u istoj periodi raste s porastom atomskog broja.
homologni niz → homologous series
Homologni niz je niz spojeva zajedničke opće formule u kojem se svaki član od idućeg razlikuje za istu skupinu, npr. metilensku skupinu (-CH2-). Članovi homolognog niza zovu se homolozi.
Ravnolančani alkani primjer su homolognog niza opće formule CnH2n+2
| Struktura | Ime |
|---|---|
| CH4 | metan |
| CH3-CH3 | etan |
| CH3-CH2-CH3 | propan |
| CH3-CH2CH2CH3 | butan |
| CH3-(CH2)3-CH3 | pentan |
| CH3-(CH2)4-CH3 | heksan |
| CH3-(CH2)5-CH3 | heptan |
| CH3-(CH2)6-CH3 | oktan |
| CH3-(CH2)7-CH3 | nonan |
| CH3-(CH2)8-CH3 | dekan |
Hessov zakon → Hesse’s law
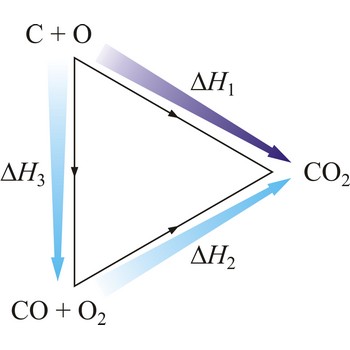
Zakonitost termokemijskih pojava otkrio je 1840. ruski kemičar švicarskog porijekla Germain Henri Hess (1802.-1850.). Njegov zakon glasi: Reakcijska toplina neke kemijske promjene ne ovisi o putu kojim reakciju vodimo, već samo o početnom i konačnom stanju sustava. Hessov zakon poznat je i kao zakon o stalnosti zbroja toplina reakcije.
Na primjer, eksperimentalno je određena entalpija oksidacije grafita u ugljikov dioksid i ugljikova monoksida u ugljikov dioksid. Zbog ravnoteže
nije moguće odrediti entalpiju oksidacije grafita u ugljikov monoksid. Međutim, reakcijska toplina te reakcije može se izračunati primjenom Hessovog zakona.
| C(s) + O2(g) →← CO2(g) | ΔrH1 = -393 kJ mol-1 |
| CO(g) + 1/2O2(g) →← CO2(g) | ΔrH2 = -283 kJ mol-1 |
| C(s) + 1/2O2(g) →← CO(g) | ΔrH3 = -110 kJ mol-1 |
Citiranje ove stranice:
Generalić, Eni. "Periodic table." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav