elektronska konfiguracija → electron configuration
Elektronska konfiguracija nam kaže broj elektrona u atomu ili ionu i njihov razmještaj po orbitalama (Vidi Tablica elektronskih konfiguracija elemenata). Struktura i sve zakonitosti u periodnom sustavu ovise o elektronskoj konfiguraciji atoma elemenata. Svojstva elementa uglavnom ovise o elektronskoj konfiguraciji vanjske ljuske. Popunjavanjem nove elektronske ljuske nastaju atomi elemenata slične elektronske konfiguracije kao i u prethodnoj ljuski, što dovodi do periodičnosti svojstava elemenata.
periodni sustav elemenata → periodic table of the elements
Periodni sustav elemenata jest tablica u kojoj su svi elementi složeni na temelju fizičkih i kemijskih svojstava. Elementi su svrstani u 18 vertikalnih skupina i 7 horizontalnih perioda. Svaka skupina (kolona tablice) sadrži elemente koji imaju slična svojstva. Broj koji određuje položaj elementa u periodnom sustavu, odnosno vrstu atoma, naziva se redni ili atomski broj. Svojstva elemenata periodična su funkcija njihovog rastućeg atomskog broja. Originalna tablica, koju je predstavio 1869. ruski kemičar D. I. Mendeljejev (1834.-1907.), bila je složena po rastućim atomskim masama (uz neke iznimke).
Bravaisova rešetka → Bravais lattice
Bravaisova rešetka je beskrajni niz zasebnih točaka čiji se raspored i orijentacija ponavlja iz koje god točke niza se gledalo. Francuski kristalograf Auguste Bravais (1811.-1863.) ustanovio je da se u prostoru mogu konstruirati samo četrnaest različitih prostornih rešetki. Svi kristalni materijali mogu se uklopiti u jedan od ovih rasporeda.
|
Kristalni sustav
|
Bravaisove kristalne rešetke
|
|||
|
kubični a=b=c α=β=γ=90° |
 |
 |
 |
|
|
|
jednostavna kubična
|
prostorno centrirana kubična
|
plošno centrirana kubična
|
|
|
tetragonski a=b≠c α=β=γ=90° |
 |
 |
||
|
|
jednostavna tetragonska
|
prostorno centrirana tetragonska
|
||
|
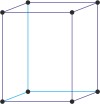
ortorompski a≠b≠c α=β=γ=90° |
 |
 |
 |
 |
|
|
jednostavna ortorompska
|
bazno centrirana ortorompska
|
prostorno centrirana ortorompska
|
plošno centrirana ortorompska
|
|
monoklinski a≠b≠c α=γ=90°≠β |
 |
 |
||
|
|
jednostavna monoklinska
|
bazno centrirana monoklinska
|
||
|
heksagonski a=b≠c α=β=90° γ=120° |
 |
|||
|
|
heksagonska
|
|||
|
romboedarski a=b=c α=β=γ≠90° |
 |
|||
|
|
romboedarska
|
|||
|
triklinski a≠b≠c α≠β≠γ≠90° |
 |
|||
|
triklinska
|
||||
frekvencija → frequency
Frekvencija (ν) ili učestalost jest broj ciklusa nekog periodičkog fenomena u jedinici vremena. Jedinica frekvencije je herc (Hz) a dobila je ime u čast njemačkog znanstvenika Heinrich Hertza (1857.-1894.).
harmoničko gibanje → harmonic motion
Jednostavno harmoničko gibanje nastaje kad na tijelo pomaknuto iz položaja ravnoteže djeluje povratna sila, po veličini proporcionalna pomaku. Uobičajeni primjer su gibanje tijela pričvršćenog o elastičnu oprugu (vidi Hookeov zakon) i gibanje matematičkog njihala. Tijelo se giba periodično, amo-tamo oko položaja ravnoteže.
kalomel elektroda → calomel electrode
Kalomel elektroda referentna je elektroda temeljena na polureakciji
Tablica: Ovisnost potencijala kalomel elektrode o temperaturi i koncentraciji KCl prema standardnoj vodikovoj elektrodi
| potencijal prema SHE / V | |||
|---|---|---|---|
| t / °C | 0.1 mol dm-3 | 3.5 mol dm-3 | zasić. otop. |
| 15 | 0.3362 | 0.254 | 0.2511 |
| 20 | 0.3359 | 0.252 | 0.2479 |
| 25 | 0.3356 | 0.250 | 0.2444 |
| 30 | 0.3351 | 0.248 | 0.2411 |
| 35 | 0.3344 | 0.246 | 0.2376 |
kemijska jednadžba → chemical equation
Kemijska jednadžba je način prikazivanja kemijske reakcije upotrebom simbola za reagirajuće čestice (atome, molekule, ione itd.). Na lijevoj strani jednadžbe pišemo formule ili simbole čestica koje stupaju u kemijsku reakciju, reaktante. Na desnoj strani jednadžbe pišemo formule ili simbole čestica koje nastaju kemijskom reakcijom, produkte.
Kod reverzibilnih reakcija umjesto znaka jednakosti stavlja se dvostruka strelica a kod ireverzibilnih jednostruka. Ako reakcija sadrži više faza, uobičajeno je staviti oznaku faze u zagrade neposredno iz formule:
| s | = | čvrsto (solid) |
| l | = | tekuće (liquid) |
| g | = | plinovito (gas) |
| aq | = | vodena otopina (aqueous) |
Brojevi a, b, c i d pokazuju relativni broj molekula koje sudjeluju u reakciji i nazivaju se stehiometrijski koeficijenti. Dogovoreno je da je stehiometrijski koeficijent pozitivan za reaktante a negativan za produkte. Ako je suma stehiometrijskih koeficijenata jednaka nuli, reakcija je uravnotežena.
Da bi se napisala jednadžba kemijske reakcije, moraju biti poznati svi reaktanti i produkti kemijske reakcije kao i njihovi stehiometrijski odnosi. Poznavanje jednadžbe kemijske reakcije omogućuje nam da odredimo količine međusobno ekvivalentnih tvari.
energija ionizacije → ionisation energy
Energija ionizacije jest energija potrebna da se elektron ukloni iz atoma. Energija ionizacije najmanja je za prvi elektron i za svaki idući raste jer se elektron sada uklanja s pozitivno nabijenog, a ne neutralnog atoma. Energija ionizacije opada u istoj skupini periodnog sustava s porastom atomskog broja elementa, a u istoj periodi raste s porastom atomskog broja.
kvazikristal → quasicrystal
Kvazikristal je kruto tijelo koje ima konvencionalna kristalna svojstva osim što njegova rešetka ne pokazuje periodičnost.
Citiranje ove stranice:
Generalić, Eni. "Periodic table." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav


