praktični salinitet → practical salinity
Praktični salinitet (praktična slanost), označen kao SP, definirao je JPOTS 1978. Skala praktičnog saliniteta (Practical Salinity Scale 1978, PSS-78) definirana je preko K15, odnosno odnosa električne vodljivosti uzorka mora pri t68 = 15 °C i tlaku od jedne standardne atmosfere i otopine kalijevog klorida (KCl) u kojoj je maseni udio KCl točno 0.0324356 (32.4356 g KCl otopljeno je u 1 kg otopine) pri istom tlaku i temperaturi. Praktični salinitet je bezdimenzijska veličina iako mu ponekad (pogrešno) pripisuju jedinicu "psu". Po definiciji, K15 iznosi točno 1 kada je praktični salinitet jednak 35 (pri gornjim uvjetima vodljivost obje otopine je C(35,1568,0) = 42.914 mS/cm = 4.2914 S/m). Praktični salinitet definiran je slijedećom jednadžbom koja vrijedi za slanosti od 2 do 42:
Kod mjerenja pri temperaturama i tlakovima (dubinama) različitim od standardnih računa se odnos vodljivosti R koji se može prikazati kao produkt tri faktora označena s Rp, Rt i rt:
Za svaku temperaturu različitu od t68 = 15 °C Praktični salinitet dan je kao funkcija od Rt (pri čemu je k = 0.0162). Pri temperaturi t68 = 15 °C Rt postaje K15.
proton → proton
Protoni su sastavni dijelovi atomske jezgre i o njihovom broju ovisi naboj jezgre. Redni broj elementa jednak je broju protona. Masa protona (mp) iznosi 1.672×10-27 kg, a naboj je +1 e.
Godine 1886. njemački fizičar Eugene Goldstein (1850.-1930.) primijetio je da u modificiranoj Crookesovoj cijevi sa šupljom katodom nastaju zrake koje se šire od anode (pozitivnog pola) i prolaze kroz katodu. Te pozitivne čestice Rutherford je nazvao protonima.
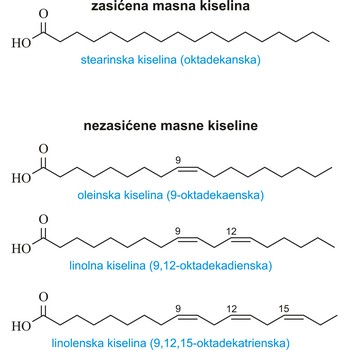
zasićena masna kiselina → saturated fatty acid
Zasićene masne kiseline su kiseline koje imaju maksimalni broj vodikovih atoma vezan za ugljikovodični lanac (nemaju dvostrukih veza između ugljikovih atoma). Najvažnije od njih su:
| maslačna (butanska kiselina) | CH3(CH2)2COOH |
| laurinska (dodekanska kiselina) | CH3(CH2)10COOH |
| miristinska (tetradekanska kiselina) | CH3(CH2)12COOH |
| palmitinska (heksadekanska kiselina) | CH3(CH2)14COOH |
| stearinska (oktadekanska kiselina) | CH3(CH2)16COOH |
| arahinska (eikosanoidna kiselina) | CH3(CH2)18COOH |
značajne znamenke → significant figures
Mjerenja nikad nisu beskrajno točna i mora se procijeniti mjera njihove neizvjesnosti. U nekom podatku mjerenja sve sigurne i prva nesigurna znamenka značajne su.
Pravila za određivanje značajnih znamenki jesu:
- Sve nule na početku broja zanemaruju se
- Sve nule na kraju broja zanemaruju se osim ako nisu iza decimalnog zareza
- Sve ostale znamenke, uključujući nulu između brojaka koje nisu nule, značajne su
Tako npr. broj
| 0.0023 | ima dvije značajne znamenke |
| 0.109 | ima tri značajne znamenke |
| 2.00 | ima tri značajne znamenke |
| 70 | ima jednu značajnu znamenku |
Rezultat treba imati samo značajne znamenke.
Prilikom zbrajanja i oduzimanja rezultat može imati onoliko znamenki iza decimalnog zareza koliko ih ima podatak s najmanjim brojem decimala (s najvećom apsolutnom pogreškom).
U množenju i dijeljenju rezultat treba imati onoliko značajnih znamenki koliko ih ima podatak s najmanjim brojem značajnih znamenki (s najvećom relativnom pogreškom). Ovo pravilo valja primijeniti s oprezom.
U logaritmu broja zadrži se onoliko znamenki desno od decimalnog zareza koliko je značajnih znamenki u izvornom broju
U antilogaritmu broja zadrži se onoliko znamenki koliko je znamenki desno od decimalnog zareza u izvornom broju.
topljivost → solubility
Topljivost je najveća količina neke tvari koja se može otopiti u nekoj količini otapala pri određenoj temperaturi. Općenito, topljivost čvrstih tvari u tekućinama raste s temperaturom a topljivost plinova opada. Topljivost se obično izražava masom otopljene tvari po masi otopine (maseni udio), molnim udjelom otopljene tvari, molalitetom, koncentracijom, i drugim.
spin → spin
Spin je unutrašnji kinetički moment osnovne čestice, ili sustava čestica kao što je npr. jezgra. Također je odgovoran za magnetski moment čestice. Spinovi jezgara imaju karakteristične fiksne vrijednosti. Parovi neutrona i protona poredaju se tako da se njihovi spinovi ponište, tako da će jezgre s neparnim brojem neutrona i/ili protona imati kvantni nuklearni spinski broj različit od nule.
Stern-Gerlachov su 1921. ustanovili da se utjecajem nehomogenoga magnetskog polja na mlaz atoma srebra ovaj cijepa u dva snopa, jedan paralelan a drugi antiparalelan magnetskom polju.
kvadratna piramidalna geometrija molekule → square pyramidal molecular geometry
Kvadratna piramidalna geometrija molekule onaj je oblik molekule kod kojeg su pet veza i jedan slobodan elektronski par vezani na centralni atom molekule. Bromov pentafluorid (BrF5) primjer je molekule koja ima geometriju kvadratne piramide. Smještaj nepodijeljenog elektronskog para potpuno je proizvoljan jer su svih šest elektronskih skupina ekvivalentne. Oktaedarski raspored elektronskih orbitala posljedica je sp3d2 (ili d2sp3) hibridizacije na centralnom atomu.
standardna devijacija → standard deviation
Standardna devijacija (σ) je statistički pojam koji označava mjeru raspršenosti podataka u skupu. Interpretira se kao prosječno odstupanje od prosjeka i to u apsolutnom iznosu.
Pretpostavimo da smo izvršili velik broj mjerenja neke veličine, koja su vrlo slična, kao što je, na primjer, promjer zrna graška u mahuni. Ako bi se grafički prikazao broj očitanja za svaki promjer, najvjerojatnije bi se dobila zvonolika krivulja, s vrlo malo očitanja velikih i malih zrna, a s većinom očitanja u blizini srednje vrijednosti. Oko dvije trećine mjerenja naći će se u intervalu koji "razapinje" standardna devijacija, mjera rasprostranjenosti.
stehiometrijski koeficijent → stoichiometric coefficient
Stehiometrijski koeficijent (ν) jest broj koji se nalazi ispred formule svakog spoja u jednadžbi kemijske reakcije. Ako ne piše nijedan broj ispred formule, stehiometrijski koeficijent je 1. Prema konvenciji negativan je za reaktante a pozitivan za produkte.
Stehiometrijski koeficijenti opisuju stehiometriju kemijske reakcije.
U ovoj reakciji, a, b, c i d predstavljaju stehiometrijske koeficijente A, B, C i D.
kositar → tin
Kositar je poznat od davnih vremena (~2000. godine prije Krista). Rimljani su ga zvali stagnum od čega je nastao latinski naziv stannum. Naziv kositar dolazi od grčkog naziva za mineral kasiterit (SnO2) - kassiteros. To je srebrno bijeli, mekani, elastični metal čija se izložena površina prevuče zaštitnim oksidnim filmom. Stabilan je na zraku i u vodi. Topljiv je u kiselinama i lužinama. Organski spojevi kositra mogu biti jako toksični. Najvažnije rude kositra su kasiterit (SnO2), stanit (Cu2FeSnS4) i tealit (PbZnSnS2). Zbog svoje stabilnosti na zraku upotrebljava se kao zaštitna prevlaka na mnogim metalima, osobito željezu (bijeli lim). Vrlo važna primjena kositra je za dobivanje legura (bronca, bijele ležajne kovine, legura za lemljenje).
Citiranje ove stranice:
Generalić, Eni. "Maseni broj." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav