galvaniziranje → electroplating
Galvaniziranje je postupak nanašanja metalne prevlake na predmet upotrebom elektrolize. Predmet se uroni u otopinu koja sadrži sol metala koji se nanaša i spoji na negativni pol baterije. Pozitivni metalni ioni putuju prema katodi (predmetu) na kojoj se reduciraju do elementarnog stanja stvarajući na predmetu tanki metalni film.
Primjerice, posrebrenjivanje mesinganih ili niklenih predmeta radi se u otopini srebrovih iona. Predmeti se spoje kao katoda i urone u otopinu a kao anoda uzme se čistog srebro. Otopina je smjesa srebrova nitrata i kalijeva cijanida koji smanjuje koncentraciju srebrovih iona čime se poboljšava kvaliteta galvaniziranja. Reakcije na elektrodama su:
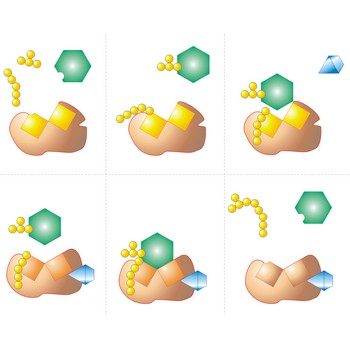
enzim → enzyme
Enzimi su biokemijski katalizatori koji po svom sastavu spadaju u grupu globularnih (klupčastih) proteina. Enzimi su specifični katalizatori i svaki enzim katalizira jednu reakciju ili skupinu srodnih reakcija. Molekule koje sudjeluju u reakciji (supstrat) veže se na specifično aktivno mjesto na molekuli enzima stvarajući kratkoživući intermedijer: to jako, ponekad i za faktor 1020 ubrzava reakciju u smjeru nastajanja produkta. Određeni enzim može sudjelovati i u sintezi i u razgradnji određene tvari.
europij → europium
Europij je 1896. godine otkrio Eugene Demarcay (Francuska). Ime mu dolazi od engleske riječi za Europu. To je srebrni, mekani metal, tvrd kao olovo. Snažno reagira s kisikom i vodom. Metal se sam zapali na zraku ako se zagrije iznad 150 °C. Glavni izvor teških lantanoida je gadolinit (Y, Ce, Cr, Be, Fe silikat), euksenit (sadrži Y, Ce, Er, Nb, Ti, U) i ksenotim (YPO4 s nešto Th i lakih lantanoida). Nalaze se i u monacitnim pijescima. Koristi se za izradu lasera i s itrijevim vanadatom kao crveni fosfor u katodnim cijevima TV-prijemnika u boji.
eksploziv → explosive
Eksplozivi (lat. explodere - raspasti se) su kemijski spojevi ili smjese koje zagrijavanjem, udarcem, trenjem ili inicijalnim paljenjem u veoma kratkom vremenskom razmaku oslobađaju veliku količinu energije. Kod gotovo svih eksploziva kemijska je reakcija trenutna oksidacija; potrebni kisik nalazi se u molekulama samog eksploziva, npr. sumpor i ugljen u crnom barutu izgaraju na račun kisika kojega u salitri (KNO3) ima oko 50 %. Stoga sumpor i ugljen izgaraju mnogo brže u barutu nego na zraku. Kod nitroglicerina prilikom eksplozije potreban kisik daju atomske grupe NO3-. Brzina izgaranja eksploziva određuje se vremenom koje je potrebno za izgaranje jednog komada eksploziva određene dužine i naziva se brzina detonacije (mjeri se u m/s). Eksplozija je egzotermna reakcija, tj. reakcija pri kojoj se razvija toplina. Ovako razvijena energija izaziva golem učinak zbog trenutačnosti reakcije. Eksplozivi se upotrebljavaju u razne svrhe: u građevinarstvu, rudarstvu i vojnoj industriji. Razne vrste eksploziva mogu se prema primjeni svrstati u tri kategorije: barute, brizantne eksplozive i inicijalne eksplozive.
Fischer-Tropschov postupak → Fischer-Tropsch process
Fischer-Tropschov postupak jest industrijska metoda dobivanja ugljikovodika iz ugljikova monoksida i vodika. Postupak, razvijen 1933. su Nijemci primijenili za dobivanje motornih goriva u II. svjetskom ratu. Naziv je dobio po njemačkom kemičaru Franzu Fischeru (1852.-1932.) i češkom kemičaru Hansu Tropschu (1839.-1935.). Vodik i ugljikov monoksid miješaju se u omjeru 2:1 i prevode pri temperaturi od 200 °C preko nikla ili kobalta kao katalizatora. Dobivena smjesa ugljikovodika može se razdijeliti u dizelsku i benzinsku frakciju.
gorivi članak → fuel cell
Gorivi članci su naprave koje pretvaraju kemijsku u električnu energiju. Razlikuju se od baterija po tome što se proces pretvorbe odvija sve dotle dok se u članak dovode gorivo i oksidirajuće sredstvo, dok je baterija napravljena s ograničenom količinom kemikalija, te je ispražnjena kada sve kemikalije izreagiraju. Gorivi članak je galvanski članak u kojem se na elektrodama odvijaju spontane reakcije. Gorivo (uglavnom vodik) oksidira se na anodi, a oksidans (gotovo uvijek kisik ili zrak) reducira se na katodi.
Neki gorivi članci koriste kao elektrolit vodene otopine, on može biti kiseli ili alkalni, a može biti i ionski vodljiva membrana namočena vodenom otopinom. Ovakvi gorivi članci rade na relativno niskim temperaturama, od sobne temperature do temperature vrenja vode. Neki gorivi članci kao elektrolit koriste taline soli (posebno karbonata) i rade na temperaturi od nekoliko stotina Celzijevih stupnjeva. Drugi koriste ionski vodljive čvrste tvari a rade na temperaturama blizu 1 000 °C.
gadolinij → gadolinium
Gadolinij je 1880. godine otkrio Jean de Marignac (Francuska). Ime je dobio u čast finskog kemičara i mineraloga Johana Gadolina. To je srebrno bijeli metal. Sporo reagira sa suhim zrakom ali brzo potamni u vlažnom. Topljiv je u kiselinama. Metal se zapali na zraku ako se zagrije. Gadolinij najbolje apsorbira neutrone od svih elemenata. Glavni izvor teških lantanoida je gadolinit (Y, Ce, Cr, Be, Fe silikat), euksenit (sadrži Y, Ce, Er, Nb, Ti, U) i ksenotim (YPO4 s nešto Th i lakih lantanoida). Nalaze se i u monacitnim pijescima. Koristi se za izradu lasera i fosfora u katodnim cijevima TV-prijemnika u boji.
Geigerov brojač → Geiger counter
Geigerov brojač (Geiger Millerov brojač) uređaj je za određivanje i mjerenje ionizirajuće radijacije. Sastoji se od cijevi s plinom pri niskom tlaku (obično argon ili neon s metanom) u kojoj se nalaze cilindrična katoda kroz čiji centar prolazi anoda u obliku tanke žice. Između elektroda narinuta je razlika potencijala od oko 1 000 V. Kroz prikladan otvor (prozor) u cijev ulazi ionizirana čestica ili foton izazivajući nastanak iona a jaka potencijalna razlika će ga usmjeriti na odgovarajuću elektrodu što će izazvati lančanu ionizaciju. Konačni strujni puls može se brojati odgovarajućim elektronskim krugom ili jednostavno preusmjeriti na zvučnik instrumenta. Uređaj je izmislio 1908. njemački fizičar Hans Geiger (1882.-1945.), a 1928. zajedno s W. Mullerom ga je unaprijedio.
globalno zatopljenje → global warming
Globalno zatopljenje ili efekt staklenika pojava je koja se zbiva u atmosferi zbog prisustva određenih plinova koji apsorbiraju infracrveno zračenje. Vidljive i ultraljubičaste zrake sposobne su prodrijeti kroz atmosferu i zagrijati Zemljinu površinu. Ovu energiju Zemlja reemitira kao infracrveno zračenje, koje zbog veće valne duljine biva apsorbirano od strane ugljikova dioksida. Posljedica toga je povećanje srednje temperature Zemlje i njene atmosfere (globalno zatopljenje). Slično se dešava i u stakleniku gdje svjetlost i duže ultraljubičaste zrake mogu proći kroz staklo ali infracrvenu radijaciju staklo apsorbira i dio reemitira u staklenik.
Ova pojava se smatra velikim rizikom i opasnošću za okoliš. Prosječno povećanje temperature može promjeniti klimu te može dovesti do otapanja ledenih polarnih kapa, a onda bi porast razine mora mogao imati katastrofične posljedice. Pokraj ugljikova dioksida, koji nastaje sagorijevanjem fosilnih goriva, negativan utjecaj na atmosferu imaju dušikovi oksidi, ozon, metan i klorofluorougljici.
Haberov proces → Haber process
Haberov proces je industrijski postupak sinteze amonijaka iz dušika i vodika:
Reakcija je egzotermna i reverzibilna, tako da se prinos na amonijaku povećava na nižim temperaturama. Brzina reakcije je previše mala na normalnoj temperaturi, pa se reakcija provodi pri optimalnoj temperatura od oko 450 °C. U reakciji se kao katalizator koristi željezo s aluminijevim oksidom kao promotorom. Povišenjem tlaka reakcija se pomiče u smjeru nastajanja amonijaka, pa se koristi tlak od 250 atmosfera. Amonijak se uklanja iz reaktora čime se reakcija pomiče u smjeru nastajanja produkata. Kao izvor vodika u originalnom procesu koristio se vodeni plin, dok se danas koristi vodik dobiven reformiranjem zemnog plina.
Proces je vrlo važan jer je to jedini industrijski način fiksacije dušika iz zraka u svrhu dobivanja umjetnih gnojiva i eksploziva. Postupak je razvio 1908. njemački kemičar Fritza Haber (1868.-1934.), a za industrijsku primjenu prilagodio ga je Carl Bosh (1874.-1940.), te se postupak još naziva Haber-Boshov postupak.
Citiranje ove stranice:
Generalić, Eni. "Kate greenaway." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav