oktaedarska geometrija molekule → octahedral molecular geometry
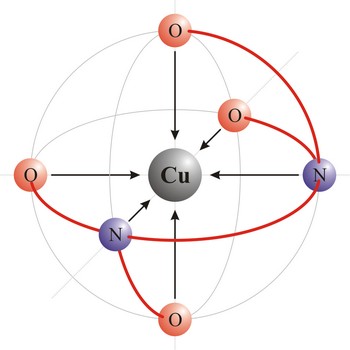
Oktaedarska geometrija molekule (kvadratni bipiramidalni oblik) opisuje onaj oblik molekule kod kojeg su šest atoma ili liganada simetrično vezani na centralni atom. Molekula sumporovog heksafluorida (SF6) ima oktaedarsku geometriju molekule. Sumporov atom i četiri atoma fluora smješteni su u jednoj ravnini s kutom od 90° među vezama. Preostala dva fluorova atoma smještena su okomito na ovu ravninu s obje njene strane. Oktaedarski raspored elektronskih orbitala posljedica je sp3d2 (ili d2sp3) hibridizacije na centralnom atomu.
polidentantni liganad → polydentant ligand
Polidentantni liganadi sadrže više koordinacijskih mjesta (mogu dati više elektronskih parova) i grade komplekse prstenaste strukture (kelatne komplekse) zamjenjujući dva ili više monodentantna liganda. Takav ligand je EDTA koja ima 6 koordinacijskih mjesta i gradi s metalima komplekse uvijek u odnosu 1:1.
tehnička vaga → precision balance
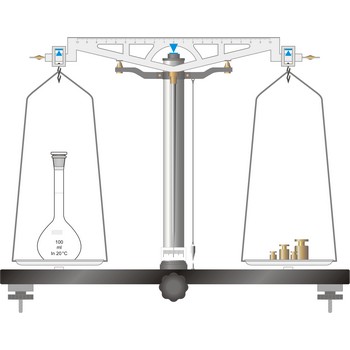
Tehničke i analitičke vage su u principu iste konstrukcije a razlikuju se jedino u materijalima i preciznosti izrade. Preciznost tehničkih vaga je manja i kreće se od 0.001 g do 0.1 g ali, za razliku od analitičke vage, mogu vagati predmete težine i do nekoliko kilograma. Klasična tehnička vaga je poluga na čijem je jednom kraku obješena zdjelica na koju se stavlja predmet nepoznate mase a na drugoj zdjelica s odgovarajućom masom utega. Kada je poluga u ravnoteži masa predmeta jednaka je masi utega.
Elektronske tehničke vage na svojoj gornjoj strani obično imaju platformu na koju se stavlja predmet koji se važe. Računalo iz struje kroz zavojnicu potrebne da se kompenzira pomak platforme izračuna težinu predmeta i rezultat prikaže na ekranu. Masa prazne posude može biti spremljena u memoriju računala i automatski oduzeta od mase posude s vaganom tvari.
kvadratna planarna geometrija molekule → square planar molecular geometry
Kvadratna planarna geometrija molekule onaj je oblik molekule kod kojeg su četiri veze i dva slobodna elektronska para vezani na centralni atom molekule. Ksenonov tetraflurid (XeF4) primjer je kvadratne građe molekule. Nepodijeljeni elektronski parovi smještaju se u dva nasuprotna vrha oktaedra a fluorovi atomi u preostala četiri tvoreći kvadrat oko ksenona. Oktaedarski raspored elektronskih orbitala posljedica je sp3d2 (ili d2sp3) hibridizacije na centralnom atomu.
kvadratna piramidalna geometrija molekule → square pyramidal molecular geometry
Kvadratna piramidalna geometrija molekule onaj je oblik molekule kod kojeg su pet veza i jedan slobodan elektronski par vezani na centralni atom molekule. Bromov pentafluorid (BrF5) primjer je molekule koja ima geometriju kvadratne piramide. Smještaj nepodijeljenog elektronskog para potpuno je proizvoljan jer su svih šest elektronskih skupina ekvivalentne. Oktaedarski raspored elektronskih orbitala posljedica je sp3d2 (ili d2sp3) hibridizacije na centralnom atomu.
sunčeva ćelija → solar cell
Sunčeva ili fotonaponska ćelija jest naprava koja sunčevu svjetlost pretvara u elektricitet. Sve sunčeve ćelije koriste se fotonaponskom pojavom, pa se često zovu fotonaponskim napravama. U većini ovih ćelija osnovni materijal čine poluvodiči, a najčešći je silicij.
Fotonaponska pojava zasniva se na stvaranju pokretnih nositelja naboja - elektrona i šupljina - uslijed apsorpcije fotona svjetlosti. Ovaj par naboja stvara se kad elektron u najvišoj popunjenoj elektronskoj vrpci poluvodiča (valentnoj vrpci) apsorbira foton dostatne energije i prijeđe u praznu elektronsku vrpcu (vodljivu vrpcu). Ovo pobuđenje može se inducirati samo fotonom čija energija odgovara širini energijskog procjepa koji razdvaja valentnu i vodljivu vrpcu. Stvaranje para naboja elektron-šupljina može se pretvoriti u električnu struju u poluvodičkoj napravi, u kojoj je sloj jednog poluvodiča spojen sa slojem drugačijeg poluvodiča ili pak metala. U većini poluvodičkih ćelija ovaj je spoj takozvani p-n spoj, tj. sučeljavaju se p-dopirani i n-dopirani poluvodič. Na sučelju višak pozitivnog naboja (šupljina) u p-dopiranom poluvodičkom sloju i višak negativnog naboja (elektrona) u n-dopiranom poluvodičkom sloju stvara električno polje, koje se prostire s obje strane sučelja. Kad se apsorpcijom fotona u ovom području stvori par elektron-šupljina, ovi naboji se, zbog djelovanja polja, udaljuju od sučelja krećući se u suprotnim smjerovima prema vrhu i dnu ćelije, gdje se nalaze metalne elektrode za skupljanje struje. Elektroda na vrhu (kroz koju se apsorbira svjetlost ) podijeljena je na trake tako da ne zaklanja poluvodički sloj. U većini komercijalnih ćelija p-n spoj se formira unutar monolitnog komada kristalnog silicija. Silicij apsorbira sunčevu svjetlost onih valnih duljina pri kojima je najintenzivnija, od bliskog infracrvenog područja (valnih duljina oko 1200 nm) do ljubičastog (valnih duljina oko 350 nm).
superoksid → superoxide
Superoksidi binarni su spojevi koji sadrže kisik sa stupnjem oksidacije -½. Superoksidni ion, O2-, ima nespareni elektronski par i vremenom se spontano disproporcionira u peroksid. Teži alkalijski elementi (K, Rb, Cs) stvaraju superokside direktnim spaljivanjem na zraku (KO2, RbO2, CsO2). To su žuto do narančasto obojeni paramagnetični spojevi. Superoksidi su jaki oksidansi koji burno hidroliziraju dajući peroksid i elementarni kisik.
T-oblik geometrije molekule → T-shaped molecular geometry
T-oblik molekule imaju molekule koje oko centralnog atoma imaju tri veze i 2 slobodna elektronska para. Atomi vezani na centralni atom leže na krajevima slova T s kutovima od 90° između njih. Elektronske orbitale usmjerene u vrhove trigonske bipiramide posljedica su sp3d (ili dsp3) hibridizacije na centralnom atomu. ICl3 ima T-oblik molekule.
tantal → tantalum
Tantal je 1802. godine otkrio Anders Ekeberg (Švedska). Ime je dobio po Tantalu iz grčke mitologije zbog velikih teškoća kod njegovog dobivanja i odvajanja od niobija. To je vrlo tvrdi srebrno sivi metal. Čisti metal se može izvući u vrlo fine žice. Na izloženoj površini formira se oksidni film otporan na koroziju. Ne otapa se u kiselinama niti u vodenim otopinama lužina, reagira jedino s fluoridnom kiselinom i rastaljenim alkalijama. Zagrijani metal se zapali na zraku. Spada u rjeđe elemente javlja se zajedno s niobijem u rudama tantalitu, niobitu ili kolumbitu ((Fe, Mn)(Nb, TaO3)2). Upotrebljava se za proizvodnju kondenzatora i drugih elektronskih komponenti, specijalnih čelika, za izradu aparata za kemijsku industriju. Otporan je na sve tjelesne tekućine i ne iritira pa se koristi u medicini.
tetraedarska geometrija molekule → tetrahedral molecular geometry
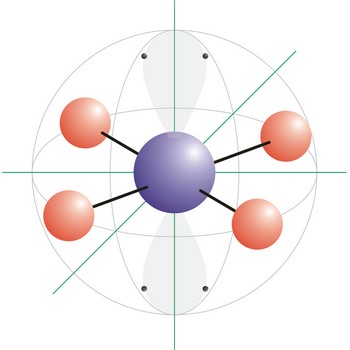
Tetraedarska geometrija molekule onaj je oblik kod kojeg u molekuli postoje četiri veze na centralnom atomu bez slobodnih elektronskih parova. Atomi vezani na centralni atom leže na vrhovima tetraedra s kutom od 109.5° između njih. Tetraedarski raspored elektronskih orbitala posljedica je sp3 hibridizacije na centralnom atomu. Npr. amonijev ion (NH4+) i metan (CH4) imaju tetraedarsku geometriju molekule.
Citiranje ove stranice:
Generalić, Eni. "Elektronska konfiguracija." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav