bazno centrirana ortorompska rešetka → base-centered orthorhombic lattice
Bazno centrirana ortorompska rešetka (označava se sa C), kao i sve ostale rešetke ima po jedan čvor kristalne rešetke u svakom uglu jedinične ćelije plus po jedan dodatni čvor na sredini dvije paralelne stranice jedinične ćelije. Kristalografski vektori jedinične ćelije su a≠b≠c a kutovi među njima α=β=γ=90°.
Beerov zakon → Beer’s law
Beerov zakon (naziva se i Beer-Lambertov zakon) daje funkcijski odnos između veličine mjerene apsorpcijskom metodom (A) i veličine koja se određuje, koncentracije (c). Posljedica međudjelovanja fotona i čestica koje apsorbiraju jest smanjenje snage snopa s Po na P. Beerov zakon može se prikazati kao
gdje je A apsorbancija na danoj valnoj duljini svjetlosti, ε je molarni apsorpcijski (ekstinkcijski) koeficijent (L mol-1 cm-1), svojstven svakoj molekulskoj vrsti i ovisan o valnoj duljini svjetlosti, b je duljina puta svjetlosti kroz uzorak (cm) a c je koncentracija tvari u otopini (mol L-1).
benzen → benzene
Benzen (benzol), C6H6, najjednostavniji je aromatski ugljikovodik, lako hlapiva tekućina karakteristična mirisa, vrelišta 80 °C, netopljiva u vodi, topljiva u benzinu, alkoholu i eteru. Gori jako čađavim plamenom, a pomiješan sa zrakom stvara eksplozivnu smjesu. Pare su mu vrlo otrovne.
Njemački kemičar Friedrich August Kekulé je, 1865., predložio strukturu molekule benzena kao heksagonalni prsten koji se sastoji od šest atoma ugljika s naizmjeničnim jednostrukim i dvostrukim ugljik-ugljik vezama. Takva struktura kaže da bi benzen trebao biti vrlo reaktivan ali to nije slučaj. Mi danas znamo da je struktura benzena doista šesterokutna, kod koje su sve C-C veze jednake i čija se duljina nalazi između onih za jednostruku i dvostruku vezu. To je objašnjeno time da se π-orbitale susjednih ugljikovih atoma preklapaju i tvore delokaliziranu molekulsku orbitalu koja se proteže oko prstena, dajući mu dodatnu stabilnost i sukladno tomu smanjenu reaktivnost. To je razlog zašto se strukturna formula benzena predstavlja kao šesterokut s krugom u sredini koji predstavlja delokalizirane elektrone.
bidentatni ligand → bidentate ligand
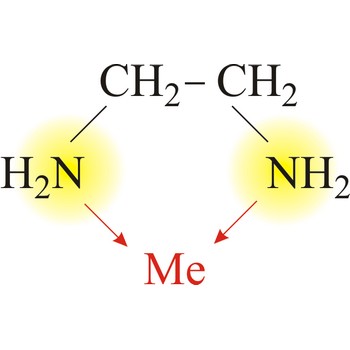
Bidentatni ili dvozubi ligandi imaju dva donorska atoma s nepodijeljenim elektronskim parovima koji se mogu vezati s dvije koordinacijske veze na centralni atom. Primjer bidentatnog liganda je etilendiamin. Jedna molekula etilendiamina formira dvije veze s metalnim ionom. Tako se na centralni atom s kordinacijskim brojm 4 vežu dvije molekule etilendiamina a na onaj s koordinacijskim brojem 6 tri molekule.
zračenje crnog tijela → blackbody radiation
Zračenje crnog tijela jest zračenje emitirano s idealnog crnog tijela, tj. tijela koje apsorbira sve zračenje koje padne na njegovu površinu. Osnovni zakon koji opisuje zračenje crnog tijela je Planckov zakon zračenja koji daje intenzitet emitiranog zračenja idealnog crnog tijela po jedinici površine u određenom smjeru kao funkciju valne duljine za određenu temperaturu. Planckov zakon može se prikazati slijedećom jednadžbom
gdje je λ valna duljina, h je Planckova konstanta, c je brzina svjetlosti, k je Boltzmannova konstanta i T je temperatura.
visoka peć → blast furnace
Visoka peć je peć koja služi u procesu dobivanja željeza iz oksidnih ruda željeza (hematita, Fe2O3 ili magnetita, Fe3O4). Koks, vapnenac i ruda ubacuju se kroz vrh peći. Vrući zrak uvodi se na dnu peći i pali koks čime se održava visoka temperatura u peći. Reakcijom između zraka i koksa razvija se ugljikov monoksid koji reducira željezov oksid.
Temperatura u peći je tolika da se rastaljeno željezo skuplja u bazi peći.
Proizvodnja željeza u visokoj peći je kontinuirani proces. Sirovine se kontinuirano ubacuju kroz vrh peći a sirovo željezo i šljaka se vade s dna. Visoka peć može raditi i do deset godina prije nego što joj se vatrostalna obloga istroši.
prostorno centrirana kubična rešetka → body-centered cubic lattice
Prostorno centrirana kubična rešetka (označava se sa bcc ili I), kao i sve ostale rešetke ima po jedan čvor kristalne rešetke u svakom uglu jedinične ćelije plus jedan dodatni čvor u sredini jedinične ćelije. Kristalografski vektori jedinične ćelije su a = b = c a kutovi među njima α=β=γ=90°.
Najjednostavnija kristalna struktura jeste ona koja ima po jedan atom u svakom čvoru jedinične ćelije. Jediničnoj ćeliji pripadaju dva atoma (8×1/8 + 1 = 2), a atomi popunjavaju 68 % volumena kocke. 23 metala kristaliziraju u kubičnom sustavu s prostorno centriranom rešetkom.
prostorno centrirana ortorompska rešetka → body-centered orthorhombic lattice
Prostorno centrirana ortorompska rešetka (označava se sa I), kao i sve ostale rešetke ima po jedan čvor kristalne rešetke u svakom uglu jedinične ćelije plus jedan dodatni čvor u sredini jedinične ćelije. Kristalografski vektori jedinične ćelije su a≠b≠c a kutovi među njima α=β=γ=90°.
prostorno centrirana tetragonska rešetka → body-centered tetragonal lattice
Prostorno centrirana tetragonska rešetka (označava se sa I), kao i sve ostale rešetke ima po jedan čvor kristalne rešetke u svakom uglu jedinične ćelije plus jedan dodatni čvor u sredini jedinične ćelije. Kristalografski vektori jedinične ćelije su a=b≠c kutovi među njima α=β=γ=90°.
kalorimetrijska bomba → bomb calorimeter
Kalorimetrijska bomba ili točnije kalorimetar s kalorimetrijskom bombom je tip kalorimetra za mjerenje pri konstantnom volumenu koji se koristi za mjerenje topline izgaranja uzorka u čistom kisiku. Četiri osnovna dijela ovog tipa kalorimetra su:
- čelična posuda (bomba) u kojoj se spaljuje uzorak,
- posuda s točno poznatim volumenom vode opskrbljena miješalicom,
- vanjska izolacijska posuda koja štiti kalorimetar od toplinskih utjecaja iz prostorije, i
- precizni termometar kojim se mjeri promjena temperature vode u unutrašnjoj posudi.
Citiranje ove stranice:
Generalić, Eni. "Blast furnace glossary." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav