Zemljina kora → Earth’s crust
Zemljina kora je vanjski površinski sloj planeta Zemlje iznad Mohorovićeva diskontinuiteta. Prosječna debljina Zemljine kore iznosi 35 km na kontinentima i oko 7 km ispod oceanskog dna. Približni sastav joj je:
| Element | Postotak (%) |
|---|---|
| kisik | 47 |
| silicij | 28 |
| aluminij | 8 |
| željezo | 4.5 |
| kalcij | 3.5 |
| natrij | 2.5 |
| kalij | 2.5 |
| magnezij | 2.2 |
EDTA → EDTA
Etilendiamintetraoctena kiselina (C10H16N2O8) ili skraćeno EDTA (ethylenediaminetetraacetic acid) heksadentantni je heksadentatni ligand koji tvori komplekse i s prijelaznim metalima i s metalima glavnih skupina. EDTA se koristi kao dinatrijeva sol zbog slabe topljivosti kiseline. Koordinacijski broj EDTA je 6. Negativni ion EDTA4- okruži metalni ion uspostavljajući koordinativne veze sa svih šest koordinacijskih mjesta (četiri na kisikovom i dva na dušikovom atomu).
EDTA se često koristi kao aditiv deterdžentima. Ona stvara kompleks s kalcijevim i magnezijevim ionima čime se poboljšava moć pranja deterdženta. EDTA se upotrebljava kao stabilizator u proizvodnji hrane i kao antikoagulans za krv u bankama krvi. EDTA je najčešći reagens u kompleksometrijskoj titraciji.
električni članak → electric cell
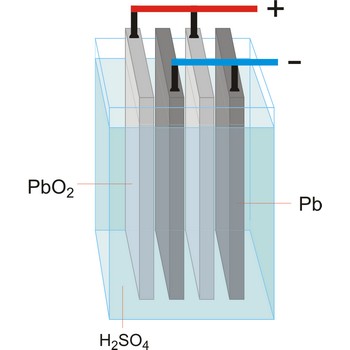
Električni članak (baterija) je naprava za proizvodnju trajnih električnih struja pretvorbom kemijske, nuklearne, toplinske ili svjetlosne energije u električnu. Prema načinu pretvorbe kemijske energije u električnu razlikuju se galvanski članci, akumulatori, gorivi članci i biološki članci.
električno polje → electric field
Ako na malu količinu naboja djeluje sila, u njegovoj blizini postoji električno polje. Električno polje, E, definira se uz pomoć elektrostatske sile, F, koja djeluje na točkasti pozitivni probni naboj, qp, smješten u polje:
SI jedinica za električno polje je N C-1 ili V m-1.
Električno polje mirnog naboja q na udaljenosti r od naboja dano je izrazom:
gdje je εo permitivnost, jednaka ε0=8.85×10-12 C2 N-1 m-2.
elektrokemijski članak → electrochemical cell
Elektrokemijski članak jest članak u kojem se pri odvijanju kemijske reakcije kemijska energija pretvara u električnu ili obrnuto. Sastoji se od dvije elektronski vodljive faze (metal ili poluvodič) koje se zovu elektrode, međusobno povezane ionski vodljivom fazom (vodene i nevodene otopine elektrolita, taline ili ionski vodljive čvrste tvari).
Pri svom prolazu kroz članak struja se mora mijenjati iz elektronske u ionsku i ponovo u elektronsku. Ove promjene vrste vodljivosti popraćene su oksido-redukcijskim reakcijama. Reakcije oksidacije i redukcije se odvijaju istovremeno, ali su prostorno odijeljene, a elektroda na kojoj se zbiva reakcija oksidacije zove se anoda, a elektroda na kojoj se zbiva redukcija jest katoda.
elektrodni potencijal → electrode potential
Elektrodni potencijal je potencijal elektrokemijske ćelije u kojoj je ispitivana elektroda spojena kao katoda a standardna vodikova elektroda (E = 0.000 V) kao anoda. Na katodi se uvijek događa redukcija a na anodi oksidacija.
Elektrodni potencijal je po definiciji redukcijski potencijal. Prema IUPAC-ovu dogovoru, izraz elektrodni potencijal namijenjen je isključivo za polureakcije napisane kao redukcije. Predznak elektrodnog potencijala određen je predznakom dotičnog polučlanka spojenog sa standardnom vodikovom elektrodom. Pozitivni predznak upućuje na to da je reakcija spontana u odnosu na standardnu vodikovu elektrodu, tj. da se polučlanak spontano ponaša kao katoda.
Članak za mjerenje elektrodnog potencijala sastoji se od standardne vodikove elektrode (dogovorno se piše lijevo)
i elektrode ispitivanog redoks-sustava (dogovorno se piše desno)
i može se shematski napisati kao
Elektromotorna sila (e.m.f.) ispitivanog redoks sustava jednaka je
Dogovorno je uzeto da je pri p(H2) = 101325 Pa i a(H+) = 1.00, potencijal vodikove elektrode jednak je 0.000 V pri svim temperaturama. Posljedica je takve definicije da se ukupni potencijal svakoga galvanskog članka koji sadrži standardnu vodikovu elektrodu pripisuje drugoj elektrodi
elektrodijaliza → electrodialysis
Elektrodijaliza je postupak dijalize ubrzan djelovanjem električnog polja. Dijalizator je podijeljen u tri dijela. Otopina koja se dijalizira teče kroz srednji odjeljak, između dviju polupropusnih membrana za pozitivne i negativne ione. Elektrode su smještene u pokrajnje odjeljke. Pod utjecajem električnog polja pozitivni ioni putovat će prema katodi (negativnoj elektrodi), a negativni ioni prema anodi (pozitivnoj elektrodi) čime se ubrzava putovanje iona kroz membranu. Tijekom dijalize čista voda nakuplja se uz elektrode a između membrana ostaje slana.
electrogravimetrija → electrogravimetry
Elektrogravimetrija je elektroanalitička tehnika kojom se tvar koja treba biti određena (obično metal) elektrodeponira na elektrodu izvaganu prije i poslije eksperimenta. Potencijal elektrode treba se pažljivo odabrati kako bi bili sigurni da će se na elektrodi istaložiti samo ona tvar koju određujemo.
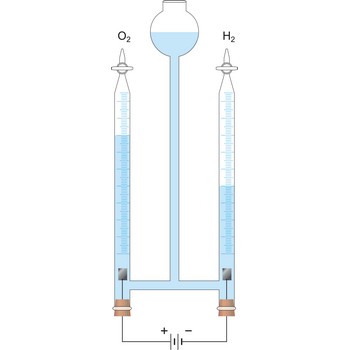
elektroliza → electrolysis
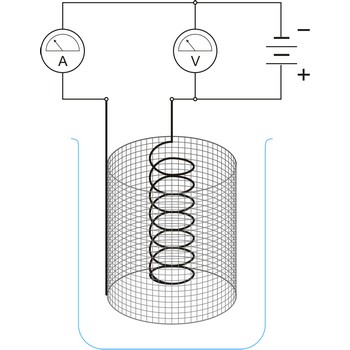
Elektroliza je elektrokemijski proces pri kojem se uz pomoć vanjskog izvora struje na elektrodama (katodi i anodi) vrše reakcije oksidacije i redukcije.
elektrolitska ćelija → electrolytic cell
Elektrolitska ćelija je ćelija u kojoj se električna energija pretvara u kemijsku. Kemijske reakcije se ne dešavaju spontano, već se odvijaju na račun struje koju u ćeliju šalje vanjski izvor i vrši elektrolizu. Promjena slobodne Gibbsove energije ukupnog procesa pozitivna je. Koriste se za elektrolizu tvari ili za spremanje električne energije pretvorbom u kemijsku (akumulatori).
Citiranje ove stranice:
Generalić, Eni. "Rare earth elements." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav