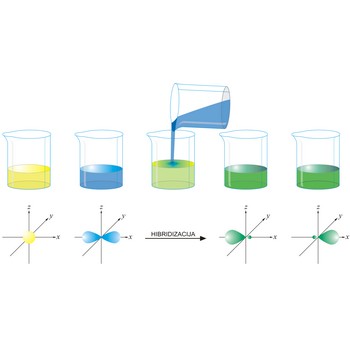
hibridne orbitale → hybrid orbital
Hibridne orbitale predstavljaju istovrsne orbitale nastale miješanjem različitih atomskih orbitala. Broj nastalih orbitala jednak je broju atomskih orbitala. Primjerice, kod sp3 hibridizacije dolazi do miješanja jedne s orbitale s tri p orbitale pri čemu nastaju četiri nove orbitale iste energije, manje od energije p ali veće od energije s orbitale.
sp hibridna orbitala → sp hybrid orbital
sp hibridna orbitala jest orbitala nastala linearnom kombinacijom jedne s i jedne p orbitale usporedive energije (kao što su 2s i 2p orbitale) u istom atomu. Dvije sp hibridne orbitale linearno su simetrične i usmjerene u suprotnom smjeru, tj. međusobno zatvaraju kut od 180°. Preostale dvije nehibridizirane p orbitale i sp hibridne orbitale međusobno su okomite.
sp2 hibridna orbitala → sp2 hybrid orbital
sp2 hibridna orbitala jest orbitala nastala linearnom kombinacijom jedne s i dvije p orbitale usporedive energije (kao što su 2s i 2p orbitale) u istom atomu. Tri sp2 hibridne orbitale leže u istoj ravnini i međusobno zatvaraju kut od 120°. Nehibridizirana treća p orbitala stoji okomito na ravninu sp2 hibridnih orbitala.
sp3 hibridna orbitala → sp3 hybrid orbital
sp3 hibridna orbitala jest orbitala nastala linearnom kombinacijom jedne s i tri p orbitale usporedive energije (kao što su 2s i 2p orbitale) u istom atomu. Četiri sp3 hibridne orbitale usmjerene su prema uglovima tetraedra i međusobno zatvaraju kut od 109.5°.
hibridizacija → hybridization
Hibridizacija atomskih orbitala je postupak u kojem se linearnim kombiniranjem valnih funkcija energijski bliskih orbitala stvaraju nove hibridne valne funkcije. Novonastale orbitale su hibridi originalnih i imaju svojstva (oblik, veličinu i energiju) koja se nalaze negdje između svojstava orbitala iz kojih su nastale.
Gaussov sustav jedinica → Gaussian system of units
Gaussov sustav jedinica je hibridni sustav koji kombinira elektrostatski cgs podsustav (esu) and elektromagnetski cgs podsustav (emu).
linearna geometrija molekule → linear molecular geometry
Linearna molekula je molekula u kojoj su atomi raspoređeni u ravnoj liniji (pod kutom od 180°). Primjerice, molekule ugljikova dioksida (O=C=O) i BeH2 su linearne. Smještanje elektronskih orbitala na pravac posljedica je sp hibridizacije na centralnom atomu.
teorija valentne veze → valence bond theory
Teorija valentne veze jest teorija koja objašnjava oblik molekule pomoću preklapanja polupopunjenih atomskih orbitala ili polupopunjenih hibridiziranih orbitala.
oblik molekule → molecular shape
Oblik molekule je trodimenzionalni razmještaj atoma u prostoru oko centralnog atoma. Molekularna formula spoja ne može nam ukazati na njegov oblik. Na primjer, CO2 je linearna molekula a SO2 savijena.
Trodimenzionalni oblik mnogih malih molekula može se predvidjeti teorijom odbijanje elektronskih parova valentne ljuske (VSEPR). Kada se atomi kombiniraju u molekulu, parovi valentnih elektrona razmještaju se na najvećoj mogućoj udaljenosti jedan od drugoga. Drugi način za opisivanje oblika molekula je pomoću hibridiziranih orbitala.
oktaedarska geometrija molekule → octahedral molecular geometry
Oktaedarska geometrija molekule (kvadratni bipiramidalni oblik) opisuje onaj oblik molekule kod kojeg su šest atoma ili liganada simetrično vezani na centralni atom. Molekula sumporovog heksafluorida (SF6) ima oktaedarsku geometriju molekule. Sumporov atom i četiri atoma fluora smješteni su u jednoj ravnini s kutom od 90° među vezama. Preostala dva fluorova atoma smještena su okomito na ovu ravninu s obje njene strane. Oktaedarski raspored elektronskih orbitala posljedica je sp3d2 (ili d2sp3) hibridizacije na centralnom atomu.
Citiranje ove stranice:
Generalić, Eni. "Toyota harrier hybrid." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav