heksagonska gusta slagalina → hexagonal close-packed structure
U heksagonskoj gustoj slagalini (hcp) jedinična ćelija sastoji se od tri sloja atoma. U prvom i trećem sloju svaki atom zbijeno je okružen sa šest drugih atoma u istoj ravnini (a). Tri atoma u srednjem sloju smještena su u udubine između prvog i drugog sloja atoma (b). Struktura heksagonske guste slagaline dobiva se naizmjeničnim slaganjem a i b slojeva atoma (a-b-a-b-a-b...).
Hessov zakon → Hesse’s law
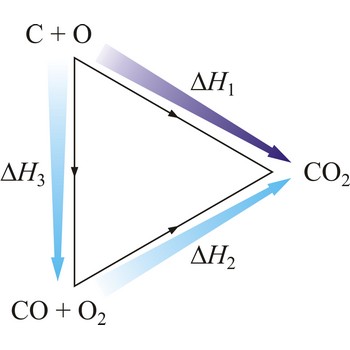
Zakonitost termokemijskih pojava otkrio je 1840. ruski kemičar švicarskog porijekla Germain Henri Hess (1802.-1850.). Njegov zakon glasi: Reakcijska toplina neke kemijske promjene ne ovisi o putu kojim reakciju vodimo, već samo o početnom i konačnom stanju sustava. Hessov zakon poznat je i kao zakon o stalnosti zbroja toplina reakcije.
Na primjer, eksperimentalno je određena entalpija oksidacije grafita u ugljikov dioksid i ugljikova monoksida u ugljikov dioksid. Zbog ravnoteže
nije moguće odrediti entalpiju oksidacije grafita u ugljikov monoksid. Međutim, reakcijska toplina te reakcije može se izračunati primjenom Hessovog zakona.
| C(s) + O2(g) →← CO2(g) | ΔrH1 = -393 kJ mol-1 |
| CO(g) + 1/2O2(g) →← CO2(g) | ΔrH2 = -283 kJ mol-1 |
| C(s) + 1/2O2(g) →← CO(g) | ΔrH3 = -110 kJ mol-1 |
heksagonski kristalni sustav → hexagonal crystal system
Heksagonski kristalni sustav temeljen je na četiri kristalografske osi. Tri kristalografske osi se smještene su u jednoj ravnini i sijeku se pod kutom od 120°. Obično se označavaju s a, b i d. Četvrta os (c) okomita je na njih i obično je kraća ili duža od ostale tri.
heksagonska rešetka → hexagonal lattice
Heksagonska rešetka ima po jedan čvor kristalne rešetke u svakom uglu jedinične ćelije i po jedan čvor u središtu svake šesterokutne baze. Kristalografski vektori jedinične ćelije su a=b≠c a kutovi među njima α=β=90° i γ=120°.
Hirschov lijevak → Hirsch funnel
Hirschov lijevak je smanjena verzija Büchnerovog lijevka za vakuum filtraciju koji se koristi za filtraciju malih volumena tekućine (1-10 mL). Osnovna razlika je u mnogo manjoj ploči za filtar papir i nagnutim stjenkama lijevka. Ime je dobio po njemačkom kemičaru Robertu Hirschu (1856.-1913.).
histidin → histidine
Histidin je nabijena aminokiselina s baznim pobočnim lancem. To je esencijalna aminokiselina koju ljudski organizam ne može sintetizirati te se mora unijeti preko hrane. Konstanta imidazolnog lanca histidina je otprilike 6 što znači da mala promjena pH fiziološke otopine može promijeniti njen naboj. Protonirani imidazol ponaša se kao kiselina a neprotonirani kao baza. Histidin se često sreće kao ligand u kompleksima željeza i cinka.
- Kratice: His, H
- IUPAC ime: 2-amino-3-(1H-imidazol-5-il)propanska kiselina
- Molekularna formula: C6H9N3O2
- Molekularna masa: 155.15 g/mol
hibridne orbitale → hybrid orbital
Hibridne orbitale predstavljaju istovrsne orbitale nastale miješanjem različitih atomskih orbitala. Broj nastalih orbitala jednak je broju atomskih orbitala. Primjerice, kod sp3 hibridizacije dolazi do miješanja jedne s orbitale s tri p orbitale pri čemu nastaju četiri nove orbitale iste energije, manje od energije p ali veće od energije s orbitale.
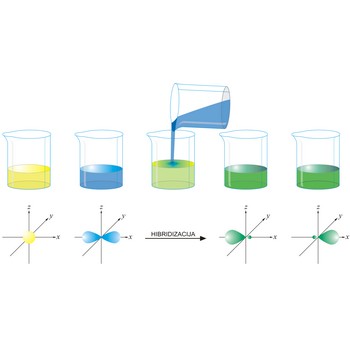
hibridizacija → hybridization
Hibridizacija atomskih orbitala je postupak u kojem se linearnim kombiniranjem valnih funkcija energijski bliskih orbitala stvaraju nove hibridne valne funkcije. Novonastale orbitale su hibridi originalnih i imaju svojstva (oblik, veličinu i energiju) koja se nalaze negdje između svojstava orbitala iz kojih su nastale.
vodik → hydrogen
Vodik je 1766. godine otkrio Sir Henry Cavendish (Engleska). Ime mu je dao Lavoisie od grčkih riječi hydro što znači voda i genes što znači tvoriti. To je plin bez boje i mirisa, netopljiv u vodi. Lako difundira kroz sve materijale. Zapaljiv je i pravi eksplozivne smjese u zraku. Zapaljen na zraku gori svijetlim vrućim plamenom dajući vodenu paru. Na povišenoj temperaturi lako se spaja s kisikom, sumporom i halogenim elementima. Procjenjuje se da 90 % svih atoma, odnosno skoro 3/4 mase svemira, otpada na vodik. Sve zvijezde, pa i Sunce, sastavljene su uglavnom od vodika (w>90 %). Vodik se u prirodi rijetko nalazi u elementarnom stanju, samo u višim slojevima atmosfere ili u vulkanskim plinovima. Uglavnom je vezan u spojevima od kojih su najrašireniji voda (H2O), amonijak (NH3) i razni organski spojevi. Čisti vodik se najčešće dobiva elektrolizom vode. Laboratorijski se dobiva reakcijom sulfatne kiseline i elementarnog cinka. Industrijski se dobiva prevođenjem vodene pare preko užarenog koksa. Upotrebljava se za sintezu amonijaka, hidriranje ugljena i ulja, proizvodnju kloridne kiseline i kao redukcijsko sredstvo.
vodikova veza → hydrogen bond
Vodikova veza formira se između atoma vodika i nekog elektronegativnog atoma te se označava isprekidanom crticom H-X---H-B. U molekuli vode dva su vodikova atoma međusobno tako raspoređena da zatvaraj kut od 105°. Svaki atom vodika ima slab pozitivan naboj a kisik negativan. Nastali dipoli uzajamno se elektrostatski privlače. Vodikova veza jaka je otprilike kao jedna desetina σ-veze a dvostruko je duža od nje.
Citiranje ove stranice:
Generalić, Eni. "S visc chemistry." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav