sol → sol
Solovi su disperzije čvrstih čestica u tekućini. Ove čestice mogu biti makromolekule ili nakupine malih molekula. Liofobni solovi su takvi solovi kod kojih ne postoji afinitet između dispergirane faze i tekućine (npr. srebrov klorid u vodi). Liofobni solovi su po prirodi nestabilni i s vremenom koaguliraju i istalože se. Liofilni solovi, u drugu ruku, mnogo su sličniji pravim otopinama. Stabilni su i teško se koaguliraju (npr. škrob u vodi).
sunčeva ćelija → solar cell
Sunčeva ili fotonaponska ćelija jest naprava koja sunčevu svjetlost pretvara u elektricitet. Sve sunčeve ćelije koriste se fotonaponskom pojavom, pa se često zovu fotonaponskim napravama. U većini ovih ćelija osnovni materijal čine poluvodiči, a najčešći je silicij.
Fotonaponska pojava zasniva se na stvaranju pokretnih nositelja naboja - elektrona i šupljina - uslijed apsorpcije fotona svjetlosti. Ovaj par naboja stvara se kad elektron u najvišoj popunjenoj elektronskoj vrpci poluvodiča (valentnoj vrpci) apsorbira foton dostatne energije i prijeđe u praznu elektronsku vrpcu (vodljivu vrpcu). Ovo pobuđenje može se inducirati samo fotonom čija energija odgovara širini energijskog procjepa koji razdvaja valentnu i vodljivu vrpcu. Stvaranje para naboja elektron-šupljina može se pretvoriti u električnu struju u poluvodičkoj napravi, u kojoj je sloj jednog poluvodiča spojen sa slojem drugačijeg poluvodiča ili pak metala. U većini poluvodičkih ćelija ovaj je spoj takozvani p-n spoj, tj. sučeljavaju se p-dopirani i n-dopirani poluvodič. Na sučelju višak pozitivnog naboja (šupljina) u p-dopiranom poluvodičkom sloju i višak negativnog naboja (elektrona) u n-dopiranom poluvodičkom sloju stvara električno polje, koje se prostire s obje strane sučelja. Kad se apsorpcijom fotona u ovom području stvori par elektron-šupljina, ovi naboji se, zbog djelovanja polja, udaljuju od sučelja krećući se u suprotnim smjerovima prema vrhu i dnu ćelije, gdje se nalaze metalne elektrode za skupljanje struje. Elektroda na vrhu (kroz koju se apsorbira svjetlost ) podijeljena je na trake tako da ne zaklanja poluvodički sloj. U većini komercijalnih ćelija p-n spoj se formira unutar monolitnog komada kristalnog silicija. Silicij apsorbira sunčevu svjetlost onih valnih duljina pri kojima je najintenzivnija, od bliskog infracrvenog područja (valnih duljina oko 1200 nm) do ljubičastog (valnih duljina oko 350 nm).
Solvayev postupak → Solvay’s process
Solvayev postupak je industrijski proces proizvodnje natrijeva karbonata iz natrijeva klorida, amonijaka i ugljikova dioksida.
Postupak započinje žarenjem vapnenca, CaCO3(s) i proizvodnjom ugljikovog dioksida.
Živo vapno, dobiveno kao nusprodukt, gasi se s vodom kako bi se dobio kalcijev hidroksid.
Kalcijev hidroksid se zagrijava s amonijevim kloridom pri čemu nastaje amonijak i kalcijev klorid (koji je sporedni proizvod postupka).
Nastali amonijak reagira s ugljikovim dioksidom dajući amonijev karbonat.
Amonijev karbonat i sam reagira s ugljikovim dioksidom dajući amonijev bikarbonat.
Reakcijom amonijevog bikarbonata s natrijevim kloridom nastaje natrijev bikarbonat.
Natrijev bikarbonat se žari u rotacijskim pećima i raspada se na natrijev karbonat i ugljikov dioksid.
Ovaj ugljikov dioksid vraća se nazad u proces.
spontani proces → spontaneous process
Spontani procesi oni su procesi koji se odvijaju bez vanjskog utjecaja. Vanjske sile nisu potrebne za održavanje procesa iako su ponekad potrebne da bi sam proces započeo. Npr. gorenje drva postaje spontani proces onog trena kad se zapali vatra. Spajanje vode i ugljikova dioksida u drvo i kisik nije spontani proces.
standardni elektrodni potencijal → standard electrode potential
Standardni elektrodni potencijal (E°) (standardni redukcijski potencijl) definiran je mjerenjem relativnih elektrodnih potencijala uz standardne uvjete (aktivitet 1, tlak 101 325 Pa i temperatura 25 °C) prema standardnoj vodikovoj elektrodi. Po konvenciji članak se piše tako da se oksidirani oblik piše prvi. Na primjer,
Elektromotorna sila gornjeg članka je -0.76 V pa je standardni elektrodni potencijal Zn2+|Zn polućelije -0.76 V.
Kada su aktiviteti oksidiranog i reduciranog oblika jednaki 1, tada je logaritamski član u Nernstovoj jednadžbi za elektrodni potencijal jednak nuli i imamo
stehiometrija → stoichiometry
Odnosi množina između reaktanata i produkata u kemijskoj reakciji predstavljaju stehiometriju kemijske reakcije, a temelji se na zakonu o održanju mase. Svaka kemijska reakcija ima svoje karakteristične odnose.
Primjerice, pri potpunom izgaranju metana
vidimo da jedan mol metana reagira s dva mola kisika dajući jedan mol ugljikova dioksida i dva mola vode.
Isto tako možemo napisati da 16 g metana reagira s 64 g kisika dajući 44 g ugljikova dioksida i 36 g vode.
Kemijska jednadžba nam simbolički prikazuje kvantitativan odnos između reaktanata i produkata. Svaka kemijska jednadžba mora biti uravnotežena. Poznavanje jednadžbe kemijske reakcije omogućuje nam da odredimo količine međusobno ekvivalentnih tvari.
škrob → starch
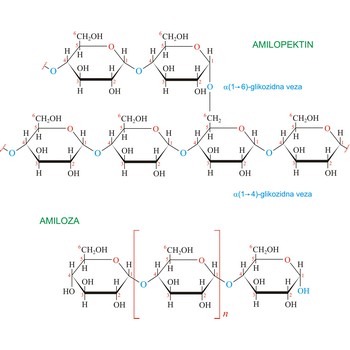
Škrob C6H10O5)x je polisaharid koji biljke koriste za skladištenje molekula glukoze. Nakuplja se u plodovima, sjemenkama, gomoljima i korijenju. Škrob je smjesa dvaju različitih polimera, amiloze (oko 20 %) i amilopektina (oko 90 %). Amiloza je netopljiva u hladnoj vodi, dok je amilopektin topljiv. Amiloza se sastoji od nekoliko stotina ostataka glukoze međusobno povezanih α(1→4)-glikozidnim vezama. Amilaza s jodom daje karakteristično intenzivno ljubičasto obojenje. Amilopektin je razgranati polimer sastavljen od dugog lanca, od nekoliko tisuća, ostataka glukoze međusobno povezanih α(1→4)-glikozidnim vezama i pobočnih lanaca koji su s njima povezani α(1→6)-glikozidnim vezama (prosječno na svakih 25 ostataka glukoze). Amilopektin s jodom daje blijedocrveno obojenje.
Probava škroba započinje u ustima djelovanjem amilaze, probavnog enzima prisutnog u slini. Razgradnja se nastavlja u tankom crijevu enzimima što ih izlučuje gušterača. Konačni produkt, molekule glukoze, apsorbiraju se u krvotok i prenose do jetre. Glikozidaze su u svom djelovanju jako specifične. One mogu hidrolizirati α-glikozidnu vezu u škrobu i glikogenu ali ne i β-glikozidnu vezu u celulozi. Škrob je važan sastojak u prehrani a široko se upotrebljava i u proizvodnji ljepila, farmaciji i medicini.
stroncij → strontium
Stroncij je 1808. godine otkrio Sir Humphry Davy (Engleska). Ime je dobio prema rudniku olova kod mjesta Strontian u Škotskoj. To je mekani, srebrno bijeli metal čija se izložena površina prekrije zaštitnim oksidnim filmom. Na zraku se zapali uslijed reakcije s vodom. Burno reagira s vodom i oksidansima. U prirodi se javlja kao mineral celestit (SrSO4) i stroncijanit (SrCO3). Glavna primjena mu je u pirotehnici jer boji plamen lijepom crvenom bojom.
šećer → sugar
Šećeri su skupina u vodi topljivih ugljikohidrata relativno niske molekularne mase i karakterističnog slatkog okusa. Skupinu čine uglavnom monosaharidi (glukoza, fruktoza, galaktoza), disaharidi (saharoza, laktoza, maltoza) i trisaharidi (rafinoza). Mnogi od njih se često nalaze u prirodi i nose imena koja odražavaju odakle su prvi put izolirani. Primjerice glukoza je također poznata i kao grožđani šećer, fruktoza kao voćni šećer, laktoza kao mliječni šećer a maltoza kao sladni šećer. U svakodnevnoj upotrebi ime šećer se obično odnosi na saharozu (obični stolni šećer iz šećerne trske ili šećerne repe).
Citiranje ove stranice:
Generalić, Eni. "Omekšivač vode." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav