referentna elektroda → referent electrode
Referentna elektroda je elektroda čiji je potencijal poznat i potpuno neovisan o koncentraciji analita. Kao referentne elektrode najčešće se koriste kalomel i srebro/srebrov klorid elektroda.
Tablica: Ovisnost potencijala referentnih elektroda o temperaturi i koncentraciji KCl
| Potencijal prema SHE / V | |||||
| kalomel elektroda | Ag/AgCl elektroda | ||||
| t / °C | 0.1 mol dm-3 | 3.5 mol dm-3 | zasić. otopina | 3.5 mol dm-3 | zasić. otopina |
| 15 | 0.3362 | 0.254 | 0.2511 | 0.212 | 0.209 |
| 20 | 0.3359 | 0.252 | 0.2479 | 0.208 | 0.204 |
| 25 | 0.3356 | 0.250 | 0.2444 | 0.205 | 0.199 |
| 30 | 0.3351 | 0.248 | 0.2411 | 0.201 | 0.194 |
| 35 | 0.3344 | 0.246 | 0.2376 | 0.197 | 0.189 |
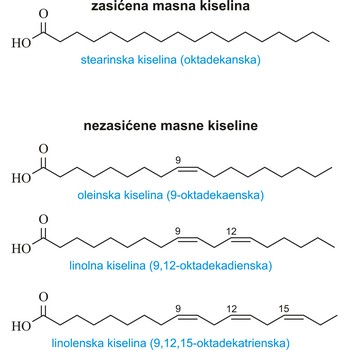
zasićena masna kiselina → saturated fatty acid
Zasićene masne kiseline su kiseline koje imaju maksimalni broj vodikovih atoma vezan za ugljikovodični lanac (nemaju dvostrukih veza između ugljikovih atoma). Najvažnije od njih su:
| maslačna (butanska kiselina) | CH3(CH2)2COOH |
| laurinska (dodekanska kiselina) | CH3(CH2)10COOH |
| miristinska (tetradekanska kiselina) | CH3(CH2)12COOH |
| palmitinska (heksadekanska kiselina) | CH3(CH2)14COOH |
| stearinska (oktadekanska kiselina) | CH3(CH2)16COOH |
| arahinska (eikosanoidna kiselina) | CH3(CH2)18COOH |
salinitet → salinity
Salinitet (S) je mjera za količinu otopljenih soli u morskoj vodi. Salinitet je definiran kao ukupna količina otopljenih soli u morskoj vodi u promilima, ‰, (djelovima na tisuću) kada se svi karbonati pretvore u okside, bromidi i jodidi u kloride i kada se sve organske tvari kompletno oksidiraju.
Klorinitet je najstarija metoda za mjerenje saliniteta koja, temeljem ideje o stalnom omjeru otopljenih komponenti morske vode, pruža uvid u ukupnu količinu otopljenih soli u morskoj vodi mjerenjem koncentracije halida (klorida, bromida i jodida). Odnos između kloriniteta (Cl) i saliniteta dan u Knudsenovim tablicama jest
Ova formula koristila se do 1962., kada je JPOTS (Joint Panel for Oceanographic Tables and Standards) odredilo novu konstantu proporcionalnosti u Knudsenovoj formuli
U međuvremenu, razvoj uređaja za mjerenje električne vodljivosti doveo je do brze, jeftine i precizne metode za određivanja slanosti morske vode. Uveden je Praktični salinitet (SP) kao zamjena za salinitet dobiven mjerenjem kloriniteta. Skala praktičnog saliniteta (Practical Salinity Scale 1978, PSS-78) definirana je preko K15, odnosno odnosa električne vodljivosti uzorka mora pri t68 = 15 °C i tlaku od jedne standardne atmosfere i otopine kalijevog klorida (KCl) u kojoj je maseni udio KCl točno 0.0324356 (32.4356 g KCl otopljeno je u 1 kg otopine) pri istom tlaku i temperaturi.
Praktični salinitet je bezdimenzijska veličina iako mu ponekad (pogrešno) pripisuju jedinicu "psu". U većini slučajeva može se pretpostaviti da su psu i ‰ sinonimi.
Prosječni salinitet morske vode je 35 ‰, što je oko 35 g soli otopljeno u 1 kg morske vode.
značajne znamenke → significant figures
Mjerenja nikad nisu beskrajno točna i mora se procijeniti mjera njihove neizvjesnosti. U nekom podatku mjerenja sve sigurne i prva nesigurna znamenka značajne su.
Pravila za određivanje značajnih znamenki jesu:
- Sve nule na početku broja zanemaruju se
- Sve nule na kraju broja zanemaruju se osim ako nisu iza decimalnog zareza
- Sve ostale znamenke, uključujući nulu između brojaka koje nisu nule, značajne su
Tako npr. broj
| 0.0023 | ima dvije značajne znamenke |
| 0.109 | ima tri značajne znamenke |
| 2.00 | ima tri značajne znamenke |
| 70 | ima jednu značajnu znamenku |
Rezultat treba imati samo značajne znamenke.
Prilikom zbrajanja i oduzimanja rezultat može imati onoliko znamenki iza decimalnog zareza koliko ih ima podatak s najmanjim brojem decimala (s najvećom apsolutnom pogreškom).
U množenju i dijeljenju rezultat treba imati onoliko značajnih znamenki koliko ih ima podatak s najmanjim brojem značajnih znamenki (s najvećom relativnom pogreškom). Ovo pravilo valja primijeniti s oprezom.
U logaritmu broja zadrži se onoliko znamenki desno od decimalnog zareza koliko je značajnih znamenki u izvornom broju
U antilogaritmu broja zadrži se onoliko znamenki koliko je znamenki desno od decimalnog zareza u izvornom broju.
titar → titar
Titar (T) je masa titrirane tvari koja je ekvivalentna 1 cm3 otopine. Prikazuje se kao T = 2.356 mg HCl / 1.0 cm3 NaOH, 0.1000 moldm-3, a obično se daje u obliku tablica. Ako se koncentracija upotrijebljene standard otopine (c) razlikuje od one navedene u tablicama (c0), uvodi se faktor korekcije (f)
Titar se obično koristi u tvorničkim pogonskim laboratorijima gdje se iz tablica za titre izravno očitava masa ili postotak traženog sastojka.
nezasićena masna kiselina → unsaturated fatty acid
Nezasićene masne kiseline su kiseline koje mogu adirati vodikove atome. Njihov ugljikovodični lanac ima jednu ili više dvostrukih ili trostrukih veza između ugljikovih atoma. Najvažnije od njih su:
| oleinska (9-oktadekaenska kiselina) | CH3(CH2)7CH=CH(CH2)7COOH |
| linolna (9,12-oktadekadienska kiselina) | CH3(CHCH2)3(CH2CH=CH)2(CHCH2)7COOH |
| linolenska (9,12,15-oktadekatrienska kiselina) | CH3(CH2CH=CH)3(CHCH2)7COOH |
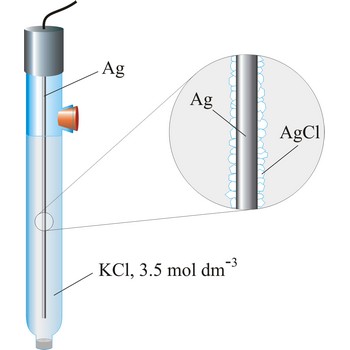
srebro/srebrov klorid elektroda → silver/silver-chloride electrode
Srebro/srebrov klorid elektroda je najčešće korištena referentna elektroda zbog svoje jednostavnosti, neotrovnosti, niske cijene i stabilnosti. Najčešći se puni zasićenim kalijevim kloridom ali može biti punjena i kalijevim kloridom nižih koncentracija, npr. 3.5 mol dm-3 ili 1 mol dm-3. Rad srebro/srebrov klorid elektrode temelji se na polureakciji
Tablica: Ovisnost potencijala srebro/srebrov klorid elektrode o temperaturi i koncentraciji KCl prema standardnoj vodikovoj elektrodi
| potencijal prema SHE / V | ||
|---|---|---|
| t / °C | 3.5 mol dm-3 | zasić. otop. |
| 15 | 0.212 | 0.209 |
| 20 | 0.208 | 0.204 |
| 25 | 0.205 | 0.199 |
| 30 | 0.201 | 0.194 |
| 35 | 0.197 | 0.189 |
vidljivo zračenje → visible radiation
Ljudsko oko zapaža samo elektromagnetsko zračenje u području valnih duljina od 400 nm do 760 nm. Taj uski dio elektromagnetskog spektra naziva se vidljivo zračenje. Vidljiva (bijela) svjetlost smjesa je svjetlosti svih boja koja se, pomoću staklene prizme, može rastaviti na sastavne boje - spektar vidljive svjetlosti, a svaka boja odgovara određenom području valnih duljina:
| boja | valna duljina / nm |
|---|---|
| ljubičasta | 400 - 450 |
| plava | 450 - 500 |
| zelena | 500 - 570 |
| žuta | 570 - 590 |
| narančasta | 590 - 620 |
| crvena | 620 - 760 |
tvrdoća vode → water hardness
Tvrdoća vode potječe od otopljenih soli kalcija i magnezija. Kalcij i magnezij nalaze se u prirodnim vodama u obliku hidrogenkarbonata, sulfata, klorida ili nitrata. Ove soli su štetne u vodama jer reagiraju sa sapunima, stvarajući netopive spojeve, a uz to se i talože na zagrijanim površinama kotlova i cijevi.
Prolazna tvrdoća, koju čine hidrogenkarbonati kalcija i magnezija, može se ukloniti zagrijavanjem vode duže vrijeme pri 90 °C do 100 °C, pri čemu se hidrogenkarbonat raspada na karbonat, ugljikov dioksid i vodu:
Stalnu tvrdoću čine pretežno sulfati, kloridi i nitrati kalcija i magnezija. Ona se ne može ukloniti zagrijavanjem vode na temperaturu vrenja. Ukupna tvrdoća jednaka je zbroju prolazne i stalne tvrdoće. Prolaznu tvrdoću čini karbonatna tvrdoća (hidrogenkarbonati), a stalnu nekarbonatna tvrdoća.
Tvrdoća vode izražava se u njemačkim, engleskim ili francuskim stupnjevima ili u mg CaCO3 u 1 dm3 vode.
| Klasifikacija voda | |
|---|---|
| Tvrdoća | Koncentracija kalcijevog karbonata (mg/L) |
| Meka voda | 0 to 75 |
| Srednje tvrda voda | 75 to 150 |
| Tvrda voda | 150 to 300 |
| Jako tvrda voda | over 300 |
Citiranje ove stranice:
Generalić, Eni. "Create table if not exists postgresql." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav