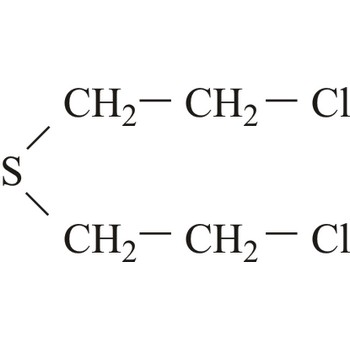monoklinski kristalni sustav → monoclinic crystal system
U monoklinskom kristalnom sustavu sve tri kristalografske osi različite su duljine. Dvije od njih (a i c) sijeku se pod šiljatim kutom i obično su smještene uspravno. Treća os (b) siječe pod pravim kutom druge dvije osi i naziva se orto os.
a ≠ b ≠ c
α = γ = 90° ≠ β
plikavac → mustard agent
Plikavci su dobili ime zbog sličnosti rana uzrokovanih onima koje izazivaju opekline. Međutim, plikavci također uzrokuju i velika oštećenja očiju, dišnog sustava i unutrašnjih organa. Uobičajeni plikavac (iperit), 1,1-tio-bis-[2-kloroetan], reagira s velikim brojem bioloških molekula. Učinak plikavaca javlja se sa zadrškom: prvi simptomi se javljaju između 2 i 24 sata nakon izloženosti. Pri sobnoj temperaturi plikavci su tekućine niske hlapljivosti i stabilne su tijekom skladištenja.
monosaharid → monosaccharide
Monosaharidi su ugljikohidrati, opće formule Cn(H2O)n, koji se hidrolizom ne mogu rastaviti na jednostavnije ugljikohidrate.
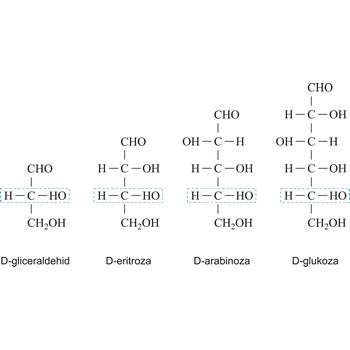
Ovisno o tome sadrže li aldehidnu (RCHO) ili keto skupinu (RCOR’) monosaharidi mogu biti polihidroksi aldehidi ili polihidroksi ketoni. Aldehidna odnosno keto skupina odgovorne su za redukcijska svojstva monosaharida. Monosaharidi se mogu podijeliti i prema broju ugljikovih atoma u ugljikovodičnom lancu pa tako imamo trioze s tri ugljikova atoma, tetroze s četiri, pentoze s pet, heksoze sa šet, heptoze sa sedam itd. Ova dva sustava podjele često se kombiniraju. Primjerice, D-glukoza, polihidroksi aldehid, je aldoheksoza a fruktoza, polihidroksi keton, je ketoheksoza.
Oznake D i L često se koriste da opišu konfiguraciju ugljikohidrata. U Fischerovoj projekcijskoj formuli, karbonilna skupina je uvijek smještena na vrh (u slučaju aldoza) ili što je moguće bliže vrhu (u slučaju ketoza). Ako se OH skupina na asimetričnom ugljikovom atomu najudaljenijem od karbonilne skupine (drugom odozdo) nalazi s desne strane imamo D-šećer, a ako je s lijeve strane, L-šećer. Uz rijetke iznimke svi šećeri u prirodi su D-šećeri.
Otvoreni lanac monosaharida može intramolekularnom ciklizacijom preći u prstenastu strukturu. Ciklizacijom nastaju dva konfiguracijska izomera, točnije dijastereomera (anomera), jer se ciklizacijom planarna karbonilna skupina pretvara u asimetrični ugljikov atom. Anomer kod kojeg je konfiguracija anomernog ugljika ista kao konfiguracija referentnog asimetričnog ugljika u Fischerovoj projekciji označava se kao α-anomer, a ako je konfiguracija različita radi se o β-anomeru.
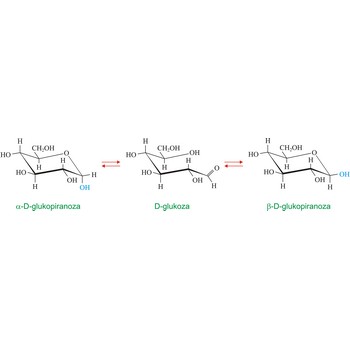
mutarotacija → mutarotation
Mutarotacija je promjena optičke aktivnosti uzrokovana epimerizacijom. U kemiji ugljikohidrata ovaj termin obično se odnosi na epimerizaciju anomernog ugljikovog atoma. U vodenoj otopini postiže se ravnotežna smjesa dvaju anomera koji prelaze jedan u drugi preko otvorenog aldehidnog oblika. Otapanjem čiste α-D-glukopiranoze ([α]D = +112.2°) ili čiste β-D-glukopiranoze ([α]D = +18.7°)u vodi dolazi do promjene zakretanja svjetlosti koje na kraju uvijek iznosi [α]D = +52.6deg;. U ravnoteži se nalazi 36 % α- i 64 % β-oblika dok je aldehidni oblik prisutan u jako niskoj koncentraciji. Mutarotaciju je 1846. otkrio francuski kemičar Augustin-Pierre Dubrunfaut (1797.-1881.).Nernstova jednadžba za elektrodni potencijal → Nernst’s electrode potential equation
Za opću reakciju nekog redoks-sustava
ovisnost elektrodnog potencijala redoks sustava o aktivitetu oksidiranog i reduciranog oblika u otopini daje nam Nernstova jednadžba za elektrodni potencijal:
gdje je E = elektrodni potencijal redoks-sustava
E° = standardni elektrodni potencijal redoks-sustava
R = univerzalna plinska konstanta
T = termodinamička temperatura
F = Faradayeva konstanta
z = broj elektrona koji se izmjenjuju u redoks-reakciji
aO = aktivitet oksidiranog oblika
aR = aktivitet reduciranog oblika
n = stehiometrijski koeficijent oksidiranog oblika
m = stehiometrijski koeficijent reduciranog oblika
živčani bojni otrov → nerve poison
Živčani su bojni otrovi imali dominantnu ulogu u Drugom svjetskom ratu. Ime im dolazi po tome što utječu na prijenos impulsa u živčanom sustavu. Svi živčani bojni otrovi spadaju u grupu organo-fosfornih spojeva. Stabilni su i lako se raspršuju, vrlo su toksični i imaju brz učinak bilo da se apsorbiraju kroz kožu ili udisanjem. Živčani bojni otrovi mogu se proizvesti prilično jednostavnim kemijskim tehnikama, a sirovine su jeftine i općenito lako dostupne.
Najvažniji živčani bojni otrovi uključeni u moderne arsenale jesu:
| Tabun | (o-etil dimetilamidofosforilcijanid) |
| Sarin | (izopropil metilfosfonofluoridat) |
| Soman | (pinakolil metilfosfonofluoridat) |
| GF | (cikloheksil metilfosfonofluoridat) |
| VX | (o-etil-diizopropilaminometil metilfosfonotiolat) |
Živčani bojni otrovi lako su hlapljive tekućine bez boje, okusa i mirisa. Antidote za njih su atropin sulfat i pralidoksim jodid.
Newmanova projekcija → Newman’s projection
Newmanova projekcija je slika koja se dobije promatranjem modela molekule uzduž C-C veze.
plemeniti plin → noble gas
U 18. skupinu periodnog sustava spadaju helij (He), neon (Ne), argon (Ar), kripton (Kr), ksenon (Xe) i radon (Rn). Zbog svoje kemijske inertnosti nazvani su plemeniti plinovi. Za razliku od većine ostalih elemenata plemeniti plinovi se u prirodi javljaju kao monoatomni.
Pod normalnim okolnostima plemeniti plinovi ne rade spojeve s drugim elementima. Prvi stabilni spoj plemenitog plina s nekim elementom, ksenonov tetrafluorid (XeF4), pripravljen je tek 1962.
nemetal → non-metal
Nemetali su elementi koji ne pokazuju metalna svojstva (slabi su vodiči topline i električne struje, ne daju se kovati itd.). Njihove se molekule uglavnom sastoje od kovalentno vezanih atoma osim kod idealnih plinova koji su monoatomni.
Smješteni su skroz desno u periodnom sustavu. Oksidi nemetala otapanjem u vodi daju kiseline. Nemetali imaju skoro popunjenu vanjsku ljusku s elektronima i lako se spajaju jedan s drugim ili s metalima. Kod mnogih elemenata ove grupe susrećemo alotropiju.
nuklearni reaktor → nuclear reactor
Nuklearni reaktori su postrojenja koja su projektirana za proizvodnju električne energije. Lančana reakcija fisibilnog materijala (uranij-235 ili plutonij-239) provodi se kontinuirano i pod kontrolom. Od sekundarnih neutrona samo jedan jedini smije izazvati daljnje cijepanje.
Osnovni dijelovi nuklearnog reaktora jesu:
- Jezgra, metalne šipke koje sadrže dovoljno fisibilnog materijala da održe lančanu reakciju na željenom nivou (može biti potrebno i preko 50 t uranija).
- Izvor neutrona koji će pokrenuti reakciju (kao što je mješavina polonija i berilija)
- Moderator koji će smanjiti energiju brzih neutrona za učinkovitiju fisiju (materijali kao što su grafit, berilij, teška voda i laka voda)
- Sredstvo za hlađenje kojim se uklanja fisijom stvorena toplina (obično voda, natrij, helij ili dušik)
- Sustav kontrole kao što su primjerice šipke bora ili kadmija koji imaju visoki udarni profil (da apsorbiraju neutrone)
- Adekvatna zaštita, kontrolna oprema i odgovarajuća instrumentacija neophodna za sigurnost osoblja i učinkoviti rad.
Citiranje ove stranice:
Generalić, Eni. "Rare earth elements." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav