benzen → benzene
Benzen (benzol), C6H6, najjednostavniji je aromatski ugljikovodik, lako hlapiva tekućina karakteristična mirisa, vrelišta 80 °C, netopljiva u vodi, topljiva u benzinu, alkoholu i eteru. Gori jako čađavim plamenom, a pomiješan sa zrakom stvara eksplozivnu smjesu. Pare su mu vrlo otrovne.
Njemački kemičar Friedrich August Kekulé je, 1865., predložio strukturu molekule benzena kao heksagonalni prsten koji se sastoji od šest atoma ugljika s naizmjeničnim jednostrukim i dvostrukim ugljik-ugljik vezama. Takva struktura kaže da bi benzen trebao biti vrlo reaktivan ali to nije slučaj. Mi danas znamo da je struktura benzena doista šesterokutna, kod koje su sve C-C veze jednake i čija se duljina nalazi između onih za jednostruku i dvostruku vezu. To je objašnjeno time da se π-orbitale susjednih ugljikovih atoma preklapaju i tvore delokaliziranu molekulsku orbitalu koja se proteže oko prstena, dajući mu dodatnu stabilnost i sukladno tomu smanjenu reaktivnost. To je razlog zašto se strukturna formula benzena predstavlja kao šesterokut s krugom u sredini koji predstavlja delokalizirane elektrone.
aromatski ugljikovodici → aromatic compounds
Aromatski ugljikovodici velika su skupina nezasićenih cikličkih ugljikovodika koji sadrže jedan ili više benzenovih prstenova. Prema Kekuléovoj formuli u benzenovom prstenu (C6H6) nalaze se tri dvostruke veze i može se prikazati kao cikloheksatrien. Kemijska svojstva benzena se, međutim, znatno razlikuju od spojeva koji sadrže dvostruke veze. Sve veze u benzenu su iste dužine i nalaze se između dvostruke i jednostruke C-C veze.
azo-spojevi → azo compounds
Azo-spojevi organski su spojevi kod kojih su dvije skupine povezane -N=N- skupinom. Mogu nastati reakcijom diazonijeva iona s benzenskim prstenom.
ugljeni katran → coal tar
Ugljeni katran je materijal koji se dobiva destruktivnom destilacijom ugljena kod proizvodnje ugljenog plina. Sirovi katran sadrži velik broj organskih spojeva (npr. benzena, naftalena, metilbenzena itd.) koji se mogu razdvojiti frakcijskom destilacijom.
ciklički spoj → cyclic compound
Ciklički spojevi (grč. krug) organski su kemijski spojevi kod kojih se jezgra sastoji od atoma sastavljenih u prsten. Dijele se na homocikličke (karbocikličke) spojeve u kojima je prsten sastavljen samo od atoma ugljika, npr. benzen (C6H6) i cikloheksan (C6H12), i na heterocikličke spojeve koji u prstenu sadrže i druge elemente, npr. piridin (C5H5N). Ciklički spojevi s dva ili više prstena biciklički su, odnosno policiklički spojevi.
dielektrična konstanta → dielectric constant
Dielektrična konstanta ili permitivnost (ε) jest mjera sposobnosti tvari da smanji elektrostatske sile između dva nabijena tijela. Što je vrijednost manja, smanjenje je veće.
Dielektrična konstanta za različite materijale pri 20 °C iznosi:
| vakuum | 1 |
| zrak | 1.00058 |
| staklo | 3 |
| benzen | 2.3 |
| octena kiselina | 6.2 |
| amonijak | 15.5 |
| etanol | 25 |
| glicerol | 56 |
| voda | 81 |
Vrijednost dielektrične konstante opada s porastom temperature.
meta položaj → meta position
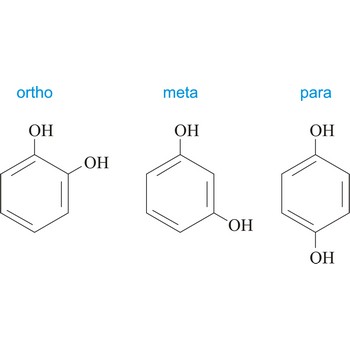
Meta položaj u organskoj kemiji onaj je položaj kada su na benzenovom prstenu vezane dvije skupine u položaju 1 i 3. Upotrebljava se kratica m-, npr. m-hidrokinon je 1,3-dihydroxybenzene.
ortho položaj → ortho position
Ortho položaj u organskoj kemiji položaj je u kojem su na benzenovom prstenu vezane dvije skupine u položajima 1 i 2. Upotrebljava se kratica o-, npr. o-hidrokinon je 1,2-dihydroxybenzene.
para položaj → para position
Para položaj u organskoj kemiji je onaj položaj u kojem su na benzenov prsten vezane dvije skupine u položaju 1 i 4. Upotrebljava se kratica p-, npr. p-hidrokinon je 1,4-dihydroxybenzene.
Citiranje ove stranice:
Generalić, Eni. "Benzene." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav