galvanski članak → galvanic celll
Galvanski članak (naponski članak, Voltin članak) jest elektrokemijski članak u kojem se kemijska energija spontano pretvara u električnu. Galvanski članak sastoji se od dva polučlanka, a svaki polučlanak od elektrode uronjene u elektrolit. Elektrolit može biti zajednički za obje elektrode ili različit za svaku elektrodu. Dva elektrolita odvajamo polupropusnom membranom ili ih spajamo elektrolitskim mostom. Ako se elektrode povežu nekim vodičem, elektroni putuju kroz vodič od negativnog pola prema pozitivnom polu.
Danielov članak je primjer galvanskog članka. Sastoji se od bakrene i cinkove elektrode, a kao elektrolit služe otopine bakrova(II) sulfata i cinkova sulfata odijeljene polupropusnom membranom. Kada se elektrode spoje električnim vodičem kroz strujni krug će proteći električna struja. Na negativnom polu (cinkovoj elektrodi) zbiva se proces oksidacije A na pozitivnom polu (bakrenoj elektrodi) zbiva se proces redukcije.
Elektromotornu silu galvanskog članka možemo izračunati iz razlike redoks potencijala tvari koja se reducirala (bakra) i tvari koja se oksidirala (cinka).
Galvanski članak može se shematski prikazati upotrebom okomite crte. Uobičajeno je da se oksidirana vrsta piše s lijeve strane.
Ime je dobila u čast talijanskog znanstvenika i liječnika Luigia Galvania (1737.-1798.).
Geigerov brojač → Geiger counter
Geigerov brojač (Geiger Millerov brojač) uređaj je za određivanje i mjerenje ionizirajuće radijacije. Sastoji se od cijevi s plinom pri niskom tlaku (obično argon ili neon s metanom) u kojoj se nalaze cilindrična katoda kroz čiji centar prolazi anoda u obliku tanke žice. Između elektroda narinuta je razlika potencijala od oko 1 000 V. Kroz prikladan otvor (prozor) u cijev ulazi ionizirana čestica ili foton izazivajući nastanak iona a jaka potencijalna razlika će ga usmjeriti na odgovarajuću elektrodu što će izazvati lančanu ionizaciju. Konačni strujni puls može se brojati odgovarajućim elektronskim krugom ili jednostavno preusmjeriti na zvučnik instrumenta. Uređaj je izmislio 1908. njemački fizičar Hans Geiger (1882.-1945.), a 1928. zajedno s W. Mullerom ga je unaprijedio.
Ilkovičeva jednadžba → Ilkovic equation
Ilkovičeva jednadžba je relacija koja se koristi u polarografiji a daje odnos između difuzijske struje (id) i koncentracije (c) depolarizatora, tj difundirajuće elektroaktivne vrste koja se reducira ili oksidira na kapajućoj živinoj elektrodi. Jednadžbu je 1934. izveo slovački fizičar Dionýz Ilkovič (1907.-1980.) primjenom Fickovih zakona difuzije.
gdje je k konstanta Ilkovičeve jednadžbe koja uključuje Faradayevu konstantu, π i gustoću žive i iznosi 708 za maksimalnu a 607 za prosječnu graničnu struju, D je koeficijent difuzije depolarizatora u danom mediju (cm2/s), n je broj elektrona izmijenjenih na elektrodi, m je brzina istjecanja žive kroz kapilaru (mg/sec), t je vrijeme kapanja a c je koncentracija depolarizatora (mol/cm3).
Gratzelova sunčeva ćelija → Gratzel solar cell
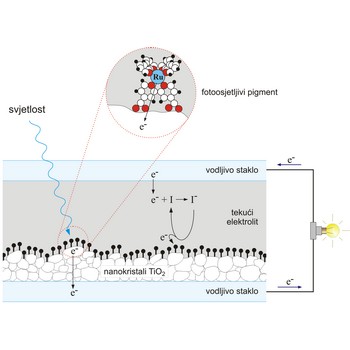
Grätzelova sunčeva ćelija je fotoelektrokemijska ćelija koju je razvio Michael Grätzel sa suradnicima. Oponaša djelomice prirodnu sunčevu ćeliju, koja omogućava biljkama da ostvare fotosintezu. U prirodnoj sunčevoj ćeliji molekule klorofila apsorbiraju svjetlost i to najjače u crvenom i plavom dijelu spektra, dok se zelena svjetlost reflektira. Apsorbirana energija dovoljna je za izbacivanje elektrona iz pobuđenog klorofila. U prijenosu tog naboja, sudjeluju potom druge molekule. U Grätzelovoj ćeliji su, također, za stvaranje naboja apsorpcijom svjetlosti i prijenos tog naboja "zaduženi" različiti dijelovi ćelije.
Na vodljivo staklo nanesen je sloj nanokristala poluvodiča TiO2 čija je površina jako velika. Na TiO2 nanesen je fotoosjetljivi pigment koji čine rutenijevi ioni povezani s organskim molekulama koje jako apsorbiraju vidljivu svjetlost. Fotopobuđeni elektroni prelaze s rutenijevih iona na kristalite TiO2, koji ih odvode daleko od iona-donora. Čitav sustav uronjen je u tekući jodidni elektrolit koji preuzima elektrone s elektrode i prenosi ih na rutenijeve ione kako bi se nastavio proces apsorpcije svjetlosti.
Efikasnost ovih ćelija iznosi oko 10 % i raste u difuznoj svjetlosti, tj. za oblačna vremena.
lantan → lanthanum
Lantan je 1839. godine otkrio Carl Gustaf Mosander (Švedska). Ime je dobio od grčke riječi lanthano što znači biti skriven. To je srebrno bijeli, kovki metal. Dovoljno je mekan da se može rezati nožem. Brzo oksidira na zraku dok s hladnom vodom reagira sporo uz razvijanje vodika. Glavni izvor lantana je mineral monacit (Ce, La, Nd, Pr fosfat) koji se nalazi u monacitnim pijescima. Koristi se kod izrade studijskih reflektora i projektora, TV-prijemnika u boji i za bojanje stakla.
fotomultiplikator → photomultiplier
Fotomultiplikator (fotomultiplikatorska cijev ili PMT) je svestrani i vrlo osjetljivi detektor elektromagnetnog zračenja u ultraljubičastom, vidljivom i bliskom infracrvenom području elektromagnetskog spektra. Tipični fotomultiplikator sadrži fotoosjetljivu katodu (fotokatodu) iza koje slijede fokusirajuće elektrode, elektrode za pojačavanje (dinode) i elektroda za skupljanje elektrona (anoda) smještene u vakuumsku cijev.
polarografija → polarography
Polarografija je voltametrijska tehnika koja se temelji na difuzijom kontroliranom putovanju analita do površine kapajuće živine elektrode. Površina radne elektrode se stalno obnavlja kako živa istječe pa su uvjeti tijekom mjerenja reproducibilni. Depolarizacijski potencijal omogućava identifikaciju iona prisutnih u otopini, a mjerenjem difuzijske struje može se izračunati njihova koncentracija. Polarografiju je izmislio češki kemičar Jaroslav Heyrovský (1890.-1967.).
potenciometrijska titracija → potentiometric titration
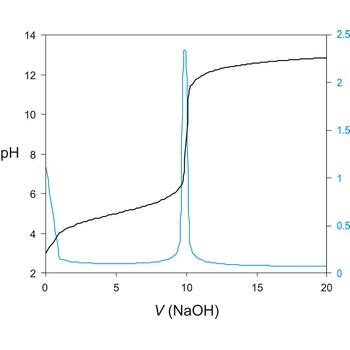
Potenciometrijska titracija je volumetrijska metoda kojom se mjeri potencijal između dvije elektrode (referentne i indikatorske elektrode) kao funkcija dodanog volumena reagensa. Temeljni princip potenciometrijske titracije je određivanje nepoznate koncentracije ispitivane otopine titracijom s nekom standardnom otopinom pri čemu skokovita (nagla) promjena potencijala indikatorske elektrode ukazuje i određuje završnu točku titracije.
Instrumentalno određivanje završne točke ima niz prednosti u odnosu na korištenje indikatora. Vizualno određivanje završne točke opterećeno je subjektivnim faktorima, a ne može se koristiti u mutnim i obojenim otopinama. Potenciometrijske metode određivanja završne točke mogu se primijeniti, ne samo za kiselo-bazne titracije već i kod taložnih, redoks i drugih titracija.
Titracijska krivulja ima karakterističan sigmoidalni oblik. Dio krivulje s maksimalnom promjenom potencijala je ekvivalentna točka titracije. Točku ekvivalencije možemo točnije odrediti iz diferencijalne krivulje ΔE/ΔV gdje maksimum krivulje određuje točku ekvivalencije.
redoks potencijal → redox potential
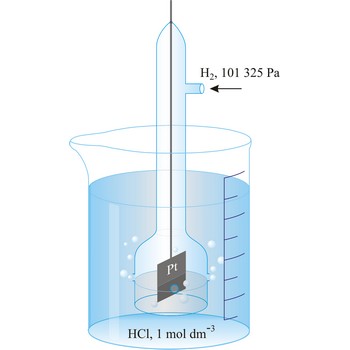
Elektrodni ili redoks potencijal je potencijal reverzibilne oksidacijsko-redukcijske elektrode mjeren s obzirom na referentnu elektrodu te korigiran s obzirom na standardnu vodikovu elektrodu u danom elektrolitu.
sunčeva ćelija → solar cell
Sunčeva ili fotonaponska ćelija jest naprava koja sunčevu svjetlost pretvara u elektricitet. Sve sunčeve ćelije koriste se fotonaponskom pojavom, pa se često zovu fotonaponskim napravama. U većini ovih ćelija osnovni materijal čine poluvodiči, a najčešći je silicij.
Fotonaponska pojava zasniva se na stvaranju pokretnih nositelja naboja - elektrona i šupljina - uslijed apsorpcije fotona svjetlosti. Ovaj par naboja stvara se kad elektron u najvišoj popunjenoj elektronskoj vrpci poluvodiča (valentnoj vrpci) apsorbira foton dostatne energije i prijeđe u praznu elektronsku vrpcu (vodljivu vrpcu). Ovo pobuđenje može se inducirati samo fotonom čija energija odgovara širini energijskog procjepa koji razdvaja valentnu i vodljivu vrpcu. Stvaranje para naboja elektron-šupljina može se pretvoriti u električnu struju u poluvodičkoj napravi, u kojoj je sloj jednog poluvodiča spojen sa slojem drugačijeg poluvodiča ili pak metala. U većini poluvodičkih ćelija ovaj je spoj takozvani p-n spoj, tj. sučeljavaju se p-dopirani i n-dopirani poluvodič. Na sučelju višak pozitivnog naboja (šupljina) u p-dopiranom poluvodičkom sloju i višak negativnog naboja (elektrona) u n-dopiranom poluvodičkom sloju stvara električno polje, koje se prostire s obje strane sučelja. Kad se apsorpcijom fotona u ovom području stvori par elektron-šupljina, ovi naboji se, zbog djelovanja polja, udaljuju od sučelja krećući se u suprotnim smjerovima prema vrhu i dnu ćelije, gdje se nalaze metalne elektrode za skupljanje struje. Elektroda na vrhu (kroz koju se apsorbira svjetlost ) podijeljena je na trake tako da ne zaklanja poluvodički sloj. U većini komercijalnih ćelija p-n spoj se formira unutar monolitnog komada kristalnog silicija. Silicij apsorbira sunčevu svjetlost onih valnih duljina pri kojima je najintenzivnija, od bliskog infracrvenog područja (valnih duljina oko 1200 nm) do ljubičastog (valnih duljina oko 350 nm).
Citiranje ove stranice:
Generalić, Eni. "CO2 ion selective electrode." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav