vodik → hydrogen
Vodik je 1766. godine otkrio Sir Henry Cavendish (Engleska). Ime mu je dao Lavoisie od grčkih riječi hydro što znači voda i genes što znači tvoriti. To je plin bez boje i mirisa, netopljiv u vodi. Lako difundira kroz sve materijale. Zapaljiv je i pravi eksplozivne smjese u zraku. Zapaljen na zraku gori svijetlim vrućim plamenom dajući vodenu paru. Na povišenoj temperaturi lako se spaja s kisikom, sumporom i halogenim elementima. Procjenjuje se da 90 % svih atoma, odnosno skoro 3/4 mase svemira, otpada na vodik. Sve zvijezde, pa i Sunce, sastavljene su uglavnom od vodika (w>90 %). Vodik se u prirodi rijetko nalazi u elementarnom stanju, samo u višim slojevima atmosfere ili u vulkanskim plinovima. Uglavnom je vezan u spojevima od kojih su najrašireniji voda (H2O), amonijak (NH3) i razni organski spojevi. Čisti vodik se najčešće dobiva elektrolizom vode. Laboratorijski se dobiva reakcijom sulfatne kiseline i elementarnog cinka. Industrijski se dobiva prevođenjem vodene pare preko užarenog koksa. Upotrebljava se za sintezu amonijaka, hidriranje ugljena i ulja, proizvodnju kloridne kiseline i kao redukcijsko sredstvo.
hipsometrijska krivulja → hypsometric curve
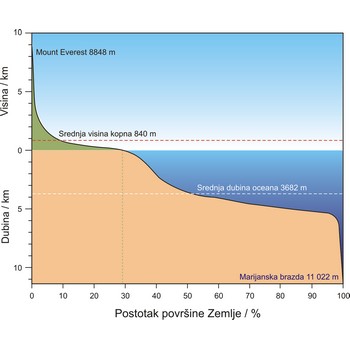
Hipsometrijska krivulja (ili hipsografska krivulja) pokazuje koliki je udio pojedinih visina (na kopnu) i dubina (na moru) na Zemlji. Pojam potječe od grčke riječi hypsos što znači visina. Dio krivulje koji pokazuje presjek dna oceana ima posebno ime i naziva se batimetrijska krivulja.
Horizontalne isprekidane linije označavaju prosječnu visinu kontinenata (840 m nadmorske visine) i prosječnu dubinu oceana (3.800 metara ispod razine mora). Kad bi se sve kopno iznad morske razine (zeleno) nasulo u more oceani bi i dalje bili prosječno 3 km duboki.
jednadžba stanja idealnog plina → ideal gas law
Jednadžba stanja idealnog plina izvedena je kombinacijom Boyle-Mariotteova, Charles-Gay-Lussacova i Avogadrova zakona. Stanje idealnog plina određeno je tlakom, volumenom, množinom i temperaturom. Njihova međusobna ovisnost dana je jednadžbom
gdje je p tlak, V molarni volumen, T temperatura a R opća plinska konstanta s vrijednošću 8.314 JK-1mol-1).
Ilkovičeva jednadžba → Ilkovic equation
Ilkovičeva jednadžba je relacija koja se koristi u polarografiji a daje odnos između difuzijske struje (id) i koncentracije (c) depolarizatora, tj difundirajuće elektroaktivne vrste koja se reducira ili oksidira na kapajućoj živinoj elektrodi. Jednadžbu je 1934. izveo slovački fizičar Dionýz Ilkovič (1907.-1980.) primjenom Fickovih zakona difuzije.
gdje je k konstanta Ilkovičeve jednadžbe koja uključuje Faradayevu konstantu, π i gustoću žive i iznosi 708 za maksimalnu a 607 za prosječnu graničnu struju, D je koeficijent difuzije depolarizatora u danom mediju (cm2/s), n je broj elektrona izmijenjenih na elektrodi, m je brzina istjecanja žive kroz kapilaru (mg/sec), t je vrijeme kapanja a c je koncentracija depolarizatora (mol/cm3).
indikator → indicator
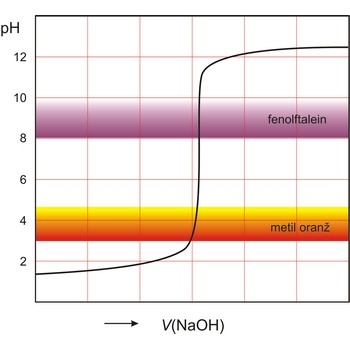
Indikator je tvar koja u otopini daje vidljivu promjenu (obično promjenu boje) u prisutnosti kemijske vrste. Koriste se za označavanje završetka kemijske reakcije. Indikatori se dijele prema vrstama kemijskih reakcija u kojima se primjenjuju (kiselo-lužnate, redoks, taložne, kompleksirajuće i adsorpcijske).
Kiselo-bazni indikatori su spojevi, kao npr. fenolftalein i metil oranž, koji reverzibilno mijenjaju boju ovisno o tome je li otopina kisela ili bazna. Oksidacijsko-redukcijski indikatori su tvari koje reverzibilno mijenjaju boju između svog oksidiranog i reduciranog oblika.
indij → indium
Indij su 1863. godine otkrili Ferdinand Reich i Hieronymus Theodor Richter (Njemačka). Ime je dobio po karakterističnoj indigoplavoj liniji u vidljivom dijelu atomskog spektra. To je srebrno bijeli metal, mekan poput voska koji je stabilan na zraku i u vodi. Topljiv je u kiselinama uz razvijanje vodika. Spojevi indija, naročito ako su u koloidnom stanju, su toksični ako se progutaju. Indij je rijedak metal koji se nigdje ne javlja u većim količinama. Dobiva se kao nusproizvod prerade sulfidnih ruda cinka, željeza i bakra. Upotrebljava se u elektronici, legura In-Cd-Ag se koristi za izradu kontrolnih šipki u nuklearnom reaktoru. Spojevi indija upotrebljavaju se za proizvodnju infracrvenih detektora.
inercija → inertia
Inercija ili tromost je izraz za tendenciju svih tijela da se odupru gibanju ukoliko miruju, odnosno da nastave s gibanjem ukoliko se gibaju. Pri razmatranju translacije tijela, tromosti odgovara masa tijela (troma masa), a pri razmatranju rotacije definira se fizikalna veličina nazvana moment tromosti. Masa i moment tromosti, dakle, mjere tromost tijela. Kugla za kuglanje ima mnogo veću inerciju od teniske loptice jer joj je masa veća.
međunarodni sustav jedinica → international system of units
Međunarodni sustav jedinica nadograđen je na sustav metar - kilogram - sekunda - amper i kratko se obilježava sa SI (System International d’Unites). Međunarodni sustav (SI) dopušta i upotrebu višekratnika jedinica. Takve jedinice zovemo decimalnim jedinicama a nazivi im se tvore tako da se ispred naziva Si jedinice stavi predmetak (prefiks). Predmetak predstavlja broj koji pomnožen jedinicom daje njezin višekratnik. SI jedinice s predmetcima također se smatraju jedinicama međunarodnog sustava.
ionska jakost otopine → ionic strength
Ionska jakost (μ ili I) otopine mjera je jakosti električnog polja koje daju ioni u otopini. Ionska jakost jednaka je polovini zbroja produkata koncentracije (c) i kvadrata naboja (z) svakog iona u otopini
željezo → iron
Željezo je poznato od davnih vremena (~2500. godine prije Krista). Simbol elementa dolazi od latinskog naziva za željezo - ferrum. To je sjajni, srebrni, tvrdi i krti metal. Zajedno s kobaltom i niklom čini trijadu željeza. Izložena površina brzo korodira naročito u vlažnom zraku i pri povišenoj temperaturi. Na površini se stvara crveno-smeđi oksid (hrđa). Otapa se u neoksidirajućim kiselinama. U koncentriranoj sulfatnoj i nitratnoj kiselini željezo se pasivira. Feromagnetično je sve do 768 °C. Željezo je najvažniji metal. Proizvodnja mu je veća nego svih ostalih metala zajedno. Glavne rude željeza su magnetit (Fe3O4), hematit (Fe2O3), limonit (FeOOH) i siderit (FeCO3). Željezo se dobiva redukcijom oksida željeza koksom u visokim pećima. Kao čisti metal se malo upotrebljava već se legira s drugim metalima u razne vrste čelika, koji su osnova moderne civilizacije.
Citiranje ove stranice:
Generalić, Eni. "Truyện hoạt hình hiếp dâm mutsuzy kimetsu no yaiba." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav