kontrakcija lantanoida → lanthanides contraction
Kontrakcija lantanoida je smanjenje metalnih i ionskih radijusa od lantana do lutecija, a uzrokovana je porastom naboja jezgre unutar iste ljuske. Elementi koji u periodnom sustavu dolaze poslije lantanoida imaju, zbog kontrakcije lantanoida, manji radijus nego što bi ga po svom položaju u periodnom sustavu morali imati.
elektronska konfiguracija → electron configuration
Elektronska konfiguracija nam kaže broj elektrona u atomu ili ionu i njihov razmještaj po orbitalama (Vidi Tablica elektronskih konfiguracija elemenata). Struktura i sve zakonitosti u periodnom sustavu ovise o elektronskoj konfiguraciji atoma elemenata. Svojstva elementa uglavnom ovise o elektronskoj konfiguraciji vanjske ljuske. Popunjavanjem nove elektronske ljuske nastaju atomi elemenata slične elektronske konfiguracije kao i u prethodnoj ljuski, što dovodi do periodičnosti svojstava elemenata.
energija → energy
Energija (E, U) je karakteristika sustava i definirana je kao sposobnost sustava da vrši rad. Jedinica za energiju je džul (J).
Unutrašnja energija tijela zbir je potencijalne i kinetičke energije atoma i molekula koji ga sačinjavaju.
Potencijalna energija jest energija pohranjena unutar tijela ili sustava kao posljedica mjesta, oblika ili stanja (uključuje gravitacijsku, električnu, nuklearnu i kemijsku energiju).
Kinetička energija jest energija kretanja i za tijelo mase m koje ima brzinu v, iznosi mv2/2. Doprinos kinetičke energije je mnogo veći kod plinova, čije molekule imaju vrlo veliku slobodu kretanje, nego kod tekućina i čvrstih tvari.
U izoliranom sustavu energija se može pretvarati iz jednog oblika u drugi, ali ukupna energija ostaje konstantna.
entalpija → enthalpy
Entalpiju (H) uveo je J.W. Gibbs 1902. kao toplinsku funkciju stanja
gdje je U unutrašnja energija sustava, p je tlak a V volumen. U kemijskim reakcijama koje se odvijaju u atmosferi tlak ostaje konstantan i entalpija reakcije (ΔH) jednaka je
Za egzotermne reakcije ΔH je negativan.
entropija → entropy
Entropija (S) je termodinamička funkcija koja govori o iskoristivosti toplinske energije. Promjena entropije nekog sustava ovisi samo o početnom i konačnom stanju sustava i definirana je izrazom
Ako je sustav izoliran, njegova se entropija neće mijenjati kada se odvija reverzibilni proces, dok će rasti ako se odvija ireverzibilan (nepovratljiv) proces. Ireverzibilnost procesa mjeri se entropijom.
Najveću entropiju imaju plinovi a najmanju kristali. Prema tome, entropija se može smatrati mjerom za nered u nekom sustavu. Pri apsolutnoj nuli u savršenom kristalu entropija je jednaka nuli.
konstanta ravnoteže → equilibrium constant
Konstanta ravnoteže (K) prvi put se pojavljuje u zakonu o djelovanju masa koji su 1863. formulirali norveški kemičari C.M. Guldberg i P. Waage. Reverzibilna kemijska reakcija prikazana jednadžbom
u ravnoteži je onda kada je brzina napredne reakcije jednaka brzini povratne reakcije.
Konstanta ravnoteže definirana je odnosom ravnotežnih aktiviteta produkata i reaktanata
Kod praktičnih mjerenja često se aktiviteti zamjenjuju koncentracijama
Za reakcije u plinskoj fazi umjesto koncetracija upotrebljavaju se parcijalni tlakovi
Termodinamička konstanta K nema jedinicu, dok jedinica za Kp i Kc ovisi o broju molekula koje se pojavljuju u stehiometrijskoj jednadžbi (a, b, c i d).
Veličina konstante ravnoteže ovisi o temperaturi. Ako je napredna reakcija egzotermna, konstanta ravnoteže smanjuje se povećanjem temperature. Što je veća konstanta ravnoteže neke kemijske reakcije, to je ravnoteža više pomaknuta na stranu stvaranja produkata reakcije. Položaj uspostavljene ravnoteže može se mijenjati, ali ne i konstanta. Sustav u ravnoteži brani se od promjene tako da nastoji poništiti vanjski utjecaj (Le Chatelierov princip).
Konstanta ravnoteže kemijske reakcije izravno je proporcionalna promjeni standardne Gibbsove slobodne energije
zakon o očuvanju energije → law of conservation of energy
Zakon o očuvanju energije: U izoliranom sustavu energija se može pretvarati iz jednog oblika u drugi, ali ukupna energija ostaje konstantna.
Le Chatelierov princip → Le Chatelier’s principle
Promijene li se vanjski uvjeti sustava, koji se nalazi u ravnoteži, tada se ravnoteža pomiče u smjeru ponovnog uspostavljanja prvobitnih uvjeta. Princip je prvi put iznio 1888. francuski kemičar Henri Le Chatelier (1850.-1936.).
tekući kristal → liquid crystal
Tekući kristali su tvari u fizikalnom stanju koje je između kristalnog stanja i taline. To stanje se zove mezofaza, a nastaje pri točki taljenja. Najvažnije mezofaze su nematična, holesterična i smektična koje se razlikuju po molekulskim orijentacijama.
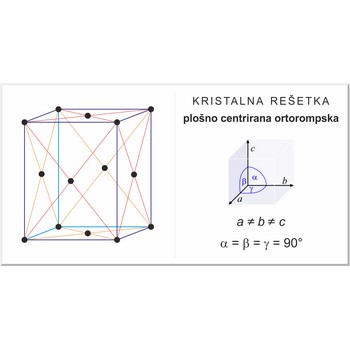
plošno centrirana ortorompska rešetka → face-centered orthorhombic lattice
Plošno centrirana ortorompska rešetka (označava se sa F), kao i sve ostale rešetke ima po jedan čvor kristalne rešetke u svakom uglu jedinične ćelije plus po jedan dodatni čvor u sredini svake stranice jedinične ćelije. Kristalografski vektori jedinične ćelije su a≠b≠c a kutovi među njima α=β=γ=90°.
Citiranje ove stranice:
Generalić, Eni. "Romboedarski kristalni sustav." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav