reakcije adicije → addition reactions
Reakcije adicije obično se pojavljuju kod nezasićenih spojeva i uključuju adiciju jedne molekule (reaktanta) preko nezasićene veze (npr. dvostruka ili trostruka veza) na drugu molekule (supstrata) čime se dobije jedinstven produkt koji je formiran kombinacijom obadviju reagirajućih molekula.
Npr. adicija broma preko dvostruke veze etena u reakciji adicije da nastane dibrometan.
povrativi članak → reversible cell
Povrativi članak je elektrokemijski članak kod kojeg su kemijske reakcija na elektrodama reverzibilne. Akumulatori su primjer povrativog članka.
reakcije drugog reda → second-order reactions
Reakcije drugog reda reakcije su u kojima je brzina proporcionalna ili koncentraciji reaktanta na kvadrat ili umnošku koncentracija dvaju reaktanata.
Za opću unimolekularnu reakciju
izraz za reakciju drugog reda se može napisati
Ako uzmemo da je koncentracija reaktanta A u vremenu t=0 jednaka [A]o a u vremenu T jednaka [A], integriranjem gornjeg izraza može se jednostavno izračunati red reakcije
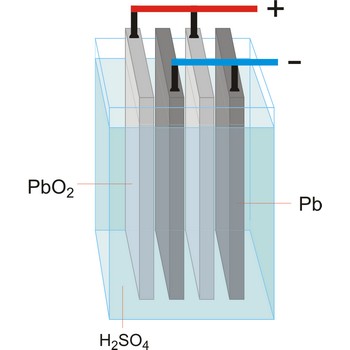
akumulator → accumulator
Akumulator (lat. accumulare - nakupljati, nagomilati) jeste naprava za sakupljanje električne energije. Električna energija se tijekom punjenja pretvara u kemijsku energiju produkata koji nastaju u akumulatoru. Najčešće vrste su olovni akumulatori i nikal-kadmijevi akumulatori.
kemijska ravnoteža → chemical balance
Kemijska ravnoteža je stupanj reverzibilne reakcije u zatvorenom sustavu kad se napredna i povratna reakcija događaju istom brzinom, a njihovi se učinci međusobno poništavaju, dok se koncentracije reaktanata i produkata ne mijenjaju.
kemijska jednadžba → chemical equation
Kemijska jednadžba je način prikazivanja kemijske reakcije upotrebom simbola za reagirajuće čestice (atome, molekule, ione itd.). Na lijevoj strani jednadžbe pišemo formule ili simbole čestica koje stupaju u kemijsku reakciju, reaktante. Na desnoj strani jednadžbe pišemo formule ili simbole čestica koje nastaju kemijskom reakcijom, produkte.
Kod reverzibilnih reakcija umjesto znaka jednakosti stavlja se dvostruka strelica a kod ireverzibilnih jednostruka. Ako reakcija sadrži više faza, uobičajeno je staviti oznaku faze u zagrade neposredno iz formule:
| s | = | čvrsto (solid) |
| l | = | tekuće (liquid) |
| g | = | plinovito (gas) |
| aq | = | vodena otopina (aqueous) |
Brojevi a, b, c i d pokazuju relativni broj molekula koje sudjeluju u reakciji i nazivaju se stehiometrijski koeficijenti. Dogovoreno je da je stehiometrijski koeficijent pozitivan za reaktante a negativan za produkte. Ako je suma stehiometrijskih koeficijenata jednaka nuli, reakcija je uravnotežena.
Da bi se napisala jednadžba kemijske reakcije, moraju biti poznati svi reaktanti i produkti kemijske reakcije kao i njihovi stehiometrijski odnosi. Poznavanje jednadžbe kemijske reakcije omogućuje nam da odredimo količine međusobno ekvivalentnih tvari.
ciklička voltametrija → cyclic voltammetry
Ciklička voltametrija je elektrokemijski postupak koji se koristi pri proučavanju kinetike i mehanizama elektrodnih reakcija. Potencijal radne elektrode kontrolira se i linearno mijenja u naprednom i povratnom smjeru, a pritom se mjeri struja koja protječe kroz ćeliju.
disocijacija → dissociation
Disocijacija je proces pri kojem se kemijska vrsta (molekula, ion i sl.) rastavlja na jednostavnije dijelove kao rezultat dodane energije (toplinska disocijacija) ili zbog djelovanja otapala (elektrolitička disocijacija). Disocijacija se može odvijati u plinovitoj, tekućoj ili krutoj fazi, ili se može dešavati u otopini. Primjer disocijacije je reverzibilna reakcija HI na visokoj temperaturi
Izraz disocijacija upotrebljava se i za reakcije ionizacije kiselina i baza u vodi. Primjerice, reakcija cijanovodične kiseline
često se piše kao disocijacija kiseline na ione
elektrokemijski članak → electrochemical cell
Elektrokemijski članak jest članak u kojem se pri odvijanju kemijske reakcije kemijska energija pretvara u električnu ili obrnuto. Sastoji se od dvije elektronski vodljive faze (metal ili poluvodič) koje se zovu elektrode, međusobno povezane ionski vodljivom fazom (vodene i nevodene otopine elektrolita, taline ili ionski vodljive čvrste tvari).
Pri svom prolazu kroz članak struja se mora mijenjati iz elektronske u ionsku i ponovo u elektronsku. Ove promjene vrste vodljivosti popraćene su oksido-redukcijskim reakcijama. Reakcije oksidacije i redukcije se odvijaju istovremeno, ali su prostorno odijeljene, a elektroda na kojoj se zbiva reakcija oksidacije zove se anoda, a elektroda na kojoj se zbiva redukcija jest katoda.
konstanta ravnoteže → equilibrium constant
Konstanta ravnoteže (K) prvi put se pojavljuje u zakonu o djelovanju masa koji su 1863. formulirali norveški kemičari C.M. Guldberg i P. Waage. Reverzibilna kemijska reakcija prikazana jednadžbom
u ravnoteži je onda kada je brzina napredne reakcije jednaka brzini povratne reakcije.
Konstanta ravnoteže definirana je odnosom ravnotežnih aktiviteta produkata i reaktanata
Kod praktičnih mjerenja često se aktiviteti zamjenjuju koncentracijama
Za reakcije u plinskoj fazi umjesto koncetracija upotrebljavaju se parcijalni tlakovi
Termodinamička konstanta K nema jedinicu, dok jedinica za Kp i Kc ovisi o broju molekula koje se pojavljuju u stehiometrijskoj jednadžbi (a, b, c i d).
Veličina konstante ravnoteže ovisi o temperaturi. Ako je napredna reakcija egzotermna, konstanta ravnoteže smanjuje se povećanjem temperature. Što je veća konstanta ravnoteže neke kemijske reakcije, to je ravnoteža više pomaknuta na stranu stvaranja produkata reakcije. Položaj uspostavljene ravnoteže može se mijenjati, ali ne i konstanta. Sustav u ravnoteži brani se od promjene tako da nastoji poništiti vanjski utjecaj (Le Chatelierov princip).
Konstanta ravnoteže kemijske reakcije izravno je proporcionalna promjeni standardne Gibbsove slobodne energije
Citiranje ove stranice:
Generalić, Eni. "Reverse reaction." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav