zlato → gold
Zlato je poznato od davnih vremena (~3000. godine prije Krista). Simbol elementa dolazi od latinskog naziva za zlato - aurum. To je sjajni, žuti metal. Mekan, kovak i savitljiv te se može izvući u listiće debele samo 10-5 mm. Ne zraku je stabilno i ne reagira s kisikom ni na kojoj temperaturi. Ne otapa se u kiselinama ni lužinama. Otapa se jedino u zlatotopci (HNO3:HCl=1:3) i u cijanidnim otopinama koje sadrže kisik, zbog stvaranja kompleksa s kloridom odnosno cijanidom. Zlato je rijedak element i ima ga deset puta manje od srebra. U prirodi se obično nalazi u elementarnom stanju u kremenim žilama ili pijesku rijeka. Upotrebljava se za izradu nakita, novca, zubnih proteza kao i za elektroničke krugove i kontakte.
hematit → haematite
Hematit, Fe2O3, najrašireniji je i najstabilniji željezov oksid te jedna od najzastupljenijih željezovih ruda u prirodi. U laboratorijskim uvjetima hematit se može pripraviti različitim metodama kemijske sinteze. Kontrolom uvjeta sinteze pripravljaju se čestice hematita različitih oblika i veličine. Oblik i veličina kristala hematita određuju njegova fizikalna svojstva, a time i komercijalnu primjenu, npr. kao pigmenata, senzora ili katalizatora.
Željezovi oksidi imaju značajnu tehnološku primjenu. Tradicionalno se upotrebljavaju kao pigmenti, pokrivaju široki raspon boja od žute do crne. Željezovi oksidi kao pigmenti otporni su na kiseline i lužine te visoke temperature. Osim u proizvodnji boja koriste se u gumarskoj i građevinskoj industriji te industriji papira. Budući da su željezovi oksidi netoksični kao pigmenti, koriste se i u prehrambenoj, kozmetičkoj i farmaceutskoj industriji.
vrijeme poluraspada → half-life
Za jednostavno radioaktivno raspadanje vrijeme poluraspada, t1/2, definirano je kao vrijeme potrebno da se aktivnost nekog radioaktivnog izotopa smanji na polovicu svoje prvobitne vrijednosti.
Što je brzina raspada veća, to je vrijeme poluraspada manje. Poluživot je karakteristično svojstvo za svaki radioaktivni izotop i neovisno je o početnoj količini radioaktivnog izotopa i uvjetima.
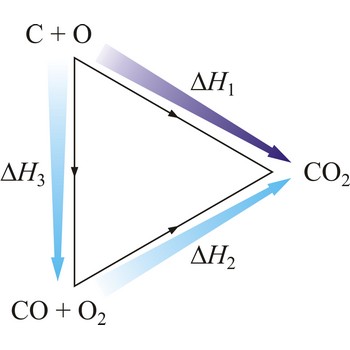
Hessov zakon → Hesse’s law
Zakonitost termokemijskih pojava otkrio je 1840. ruski kemičar švicarskog porijekla Germain Henri Hess (1802.-1850.). Njegov zakon glasi: Reakcijska toplina neke kemijske promjene ne ovisi o putu kojim reakciju vodimo, već samo o početnom i konačnom stanju sustava. Hessov zakon poznat je i kao zakon o stalnosti zbroja toplina reakcije.
Na primjer, eksperimentalno je određena entalpija oksidacije grafita u ugljikov dioksid i ugljikova monoksida u ugljikov dioksid. Zbog ravnoteže
nije moguće odrediti entalpiju oksidacije grafita u ugljikov monoksid. Međutim, reakcijska toplina te reakcije može se izračunati primjenom Hessovog zakona.
| C(s) + O2(g) →← CO2(g) | ΔrH1 = -393 kJ mol-1 |
| CO(g) + 1/2O2(g) →← CO2(g) | ΔrH2 = -283 kJ mol-1 |
| C(s) + 1/2O2(g) →← CO(g) | ΔrH3 = -110 kJ mol-1 |
Hirschov lijevak → Hirsch funnel
Hirschov lijevak je smanjena verzija Büchnerovog lijevka za vakuum filtraciju koji se koristi za filtraciju malih volumena tekućine (1-10 mL). Osnovna razlika je u mnogo manjoj ploči za filtar papir i nagnutim stjenkama lijevka. Ime je dobio po njemačkom kemičaru Robertu Hirschu (1856.-1913.).
Hookeov zakon → Hooke’s law
Hookeov zakon kaže da je deformacija tijela proporcionalna primijenjenoj sili pod uvjetom da se ne prijeđe granica elastičnosti tijela. Kada se sila ukloni tijelo će se vratiti u svoj prvobitni oblik. Zakon je otkrio engleski fizičar Robert Hook 1676.
Ako se tijelo na elastičnoj opruzi pomakne iz ravnotežnog položaja, tj. ako se opruga rastegne ili stisne, djelovat će povratna sila (elastična sila opruge), koja će nastojati tijelo vratiti u ravnotežni položaj. Iznos te sile je proporcionalan pomaku tijela iz ravnotežnog položaja. Dakle, ako je pomak x, povratna sila je:
a koeficijent proporcionalnosti k je konstanta opruge (ovisi o njenim dimenzijama, obliku i materijalu od kojega je izrađena).
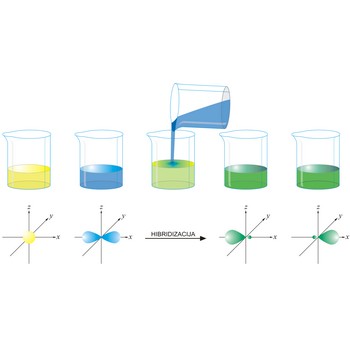
hibridne orbitale → hybrid orbital
Hibridne orbitale predstavljaju istovrsne orbitale nastale miješanjem različitih atomskih orbitala. Broj nastalih orbitala jednak je broju atomskih orbitala. Primjerice, kod sp3 hibridizacije dolazi do miješanja jedne s orbitale s tri p orbitale pri čemu nastaju četiri nove orbitale iste energije, manje od energije p ali veće od energije s orbitale.
Ilkovičeva jednadžba → Ilkovic equation
Ilkovičeva jednadžba je relacija koja se koristi u polarografiji a daje odnos između difuzijske struje (id) i koncentracije (c) depolarizatora, tj difundirajuće elektroaktivne vrste koja se reducira ili oksidira na kapajućoj živinoj elektrodi. Jednadžbu je 1934. izveo slovački fizičar Dionýz Ilkovič (1907.-1980.) primjenom Fickovih zakona difuzije.
gdje je k konstanta Ilkovičeve jednadžbe koja uključuje Faradayevu konstantu, π i gustoću žive i iznosi 708 za maksimalnu a 607 za prosječnu graničnu struju, D je koeficijent difuzije depolarizatora u danom mediju (cm2/s), n je broj elektrona izmijenjenih na elektrodi, m je brzina istjecanja žive kroz kapilaru (mg/sec), t je vrijeme kapanja a c je koncentracija depolarizatora (mol/cm3).
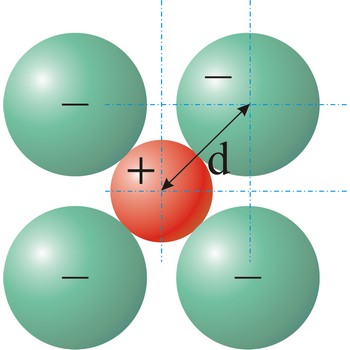
ionski radijus → ionic radius
Ionski radijus je radijus aniona i kationa u kristalnoj rešetki ionskog spoja, na osnovi pretpostavke da su ioni sfernog oblika određene veličine. Udaljenost između jezgara susjednih iona u kristalnoj rešetki određuje se difrakcijom x-zraka. Razmatranjem efekta zasjenjenja vanjskih elektrona unutarnjim moguće je odrediti vrijednosti ionskih radijusa pojedinih iona. Općenito vrijedi što je veći negativni naboj, ion je veći, a što je veći pozitivni naboj, ion je manji
Joule-Thomsonov efekt → Joule-Thomson’s effect
Temperatura idealnog plina ne mijenja se kod prigušenja na niži tlak, ali kod prigušenja realnih plinova pojavljuje se, pri višim tlakovima, veća ili manja promjena temperature. Promjena temperature koja se pojavljuje pri ekspanziji realnih plinova u sustavu u koji se ne dovodi energija naziva se Joule-Thomsonov efekt. Ustanovili su da se zraku prigušenom za 1 bar snižava temperatura za 0.25 °C. Taj je neznatni efekt, koji je za većinu tehničkih procesa posve nebitan, iskorišten je za ukapljivanje plinova.
Citiranje ove stranice:
Generalić, Eni. "How many oz in a gram." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav