elektrokemijski članak → electrochemical cell
Elektrokemijski članak jest članak u kojem se pri odvijanju kemijske reakcije kemijska energija pretvara u električnu ili obrnuto. Sastoji se od dvije elektronski vodljive faze (metal ili poluvodič) koje se zovu elektrode, međusobno povezane ionski vodljivom fazom (vodene i nevodene otopine elektrolita, taline ili ionski vodljive čvrste tvari).
Pri svom prolazu kroz članak struja se mora mijenjati iz elektronske u ionsku i ponovo u elektronsku. Ove promjene vrste vodljivosti popraćene su oksido-redukcijskim reakcijama. Reakcije oksidacije i redukcije se odvijaju istovremeno, ali su prostorno odijeljene, a elektroda na kojoj se zbiva reakcija oksidacije zove se anoda, a elektroda na kojoj se zbiva redukcija jest katoda.
frakcijska destilacija → fractional distillation
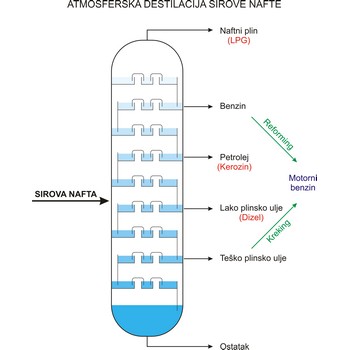
Frakcijska destilacija je postupak razdvajanja tekućina bliskog vrelišta. Provodi se u frakcijskim ili rektifikacijskim kolonama na način da se destilacijom nastala parna faza kondenzira, a dobiveni kondenzat ponovo destilira. Postupak se ponavlja više puta. Kako parna faza uvijek sadrži više lakše hlapljive komponente od tekuće faze, na vrhu kolone izlazi para čiste lakše hlapljive komponente a na dnu tekućina teže hlapljive komponente.
vertikalna energija ionizacije → vertical ionisation energy
Vertikalna energija ionizacije je energija potrebna da se ukloni elektron iz atoma, molekule ili iona u plinovitoj fazi bez da se ukloni bilo koja jezgra. Vertikalna energija ionizacije je veća ili jednaka adijabatskoj energiji ionizacije.
zeta potencijal → zeta potential
Zeta potencijal (ζ) jest potencijal preko granice faza svih čvrstih tijela i tekućina. Osobitose odnosi na potencijal difuznog sloja iona koji okružuju nabijenu koloidnu česticu, i koji je velikim dijelom odgovoran za stabilnost koloida. Također se naziva i elektrokinetički potencijal.
konstanta ravnoteže → equilibrium constant
Konstanta ravnoteže (K) prvi put se pojavljuje u zakonu o djelovanju masa koji su 1863. formulirali norveški kemičari C.M. Guldberg i P. Waage. Reverzibilna kemijska reakcija prikazana jednadžbom
u ravnoteži je onda kada je brzina napredne reakcije jednaka brzini povratne reakcije.
Konstanta ravnoteže definirana je odnosom ravnotežnih aktiviteta produkata i reaktanata
Kod praktičnih mjerenja često se aktiviteti zamjenjuju koncentracijama
Za reakcije u plinskoj fazi umjesto koncetracija upotrebljavaju se parcijalni tlakovi
Termodinamička konstanta K nema jedinicu, dok jedinica za Kp i Kc ovisi o broju molekula koje se pojavljuju u stehiometrijskoj jednadžbi (a, b, c i d).
Veličina konstante ravnoteže ovisi o temperaturi. Ako je napredna reakcija egzotermna, konstanta ravnoteže smanjuje se povećanjem temperature. Što je veća konstanta ravnoteže neke kemijske reakcije, to je ravnoteža više pomaknuta na stranu stvaranja produkata reakcije. Položaj uspostavljene ravnoteže može se mijenjati, ali ne i konstanta. Sustav u ravnoteži brani se od promjene tako da nastoji poništiti vanjski utjecaj (Le Chatelierov princip).
Konstanta ravnoteže kemijske reakcije izravno je proporcionalna promjeni standardne Gibbsove slobodne energije
talište → melting point
Talište je temperatura pri kojoj čvrsta tvar prelazi u tekuće stanje pri normalnom tlaku.
Mnogo točnija definicija tališta (ili ledišta) jest da je to temperatura pri kojoj su čvrsta i tekuća faza neka tvari pri određenom tlaku u ravnoteži. Čiste tvari, za razliku od smjesa, imaju oštro definirano talište karakteristično za tu tvar. Hoće li se koristiti naziv talište ili ledište, ovisi o tome da li se tvar zagrijava ili hladi.
papirna kromatografija → paper chromatography
Papirna kromatografija je tip planarne kromatografije kod koje se kao stacionarna faza koristi filter papir. Mobilna faza (otapalo ili smjesa otapala) u koju je uronjen rub filter papira kapilarnim silama širi se prema vrhu papira. Pojedini sastojci smjese putuju različitim brzinama u smjeru širenja otapala kroz filter papir.
faktor zaostajanja → retardation factor
Faktor zaostajanja, RF, (retardation factor) veličina je koja se upotrebljava u tankoslojnoj kromatografiji, a označava omjer udaljenosti središta mrlje do koje je došla neka tvar i udaljenosti fronte otapala od točke nanošenja uzorka.
RF-vrijednost karakteristična je za dani spoj za određenu stacionarnu i mobilnu fazu. Usporedbom RF-vrijednosti mogu se identificirati nepoznati spojevi.
sol → sol
Solovi su disperzije čvrstih čestica u tekućini. Ove čestice mogu biti makromolekule ili nakupine malih molekula. Liofobni solovi su takvi solovi kod kojih ne postoji afinitet između dispergirane faze i tekućine (npr. srebrov klorid u vodi). Liofobni solovi su po prirodi nestabilni i s vremenom koaguliraju i istalože se. Liofilni solovi, u drugu ruku, mnogo su sličniji pravim otopinama. Stabilni su i teško se koaguliraju (npr. škrob u vodi).
superkritični fluid → supercritical fluid
Superkritični fluid je bilo koja tvar iznad svoje kritične temperature i kritičnog tlaka (vidi fazni dijagram). On ima jedinstvena svojstva koja se razlikuju i od plinova i od tekućina. Superkritični fluid ima svojstvo plina da penetrira u svaku poru kao i svojstvo tekućine da otapa materijale. Topljivost tvari raste s porastom gustoće (tj. s porastom tlaka). Primjerice, naftalen je praktički netopiv u niskotlačnom tekućem ugljičnom dioksidu. Na 100 bar topljivost je 10 g/L a na 200 bar je 50 g/L. Brzom ekspanzijom superkritične otopine dolazi do taloženja otopljene krutine.
Citiranje ove stranice:
Generalić, Eni. "Faza." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav