lutecij → lutetium
Lutecij su 1907. godine otkrili neovisno jedan o drugom Georges Urbain (Francuska) i Carl Auer von Welsbach (Austrija). Ime je dobio po latinskom nazivu za Pariz - Lutetia. To je srebrno bijeli metal. Relativno je stabilan u suhom zraku. Topljiv je u kiselinama. Glavni izvor teških lantanoida je gadolinit (Y, Ce, Cr, Be, Fe silikat), euksenit (sadrži Y, Ce, Er, Nb, Ti, U) i ksenotim (YPO4 s nešto Th i lakih lantanoida). Nalaze se i u monacitnim pijescima. Koristi se za poboljšavanje mehaničkih svojstava nehrđajučih čelika i kao katalizator kod krekiranja nafte.
magnezij → magnesium
Magnezij je 1808. godine otkrio Sir Humphry Davy (Engleska). Ime mu potječe od grčkog naziva za magnezijev oksid (MgO) - magnesia alba, prema okrugu u Thessaly, Grčka. To je polutvrdi, sjajni, srebrno bijeli metal, koji na zraku potamni zbog zaštitne prevlake oksida. Može se kovati, lijevati i valjati. Gori na zraku uz pojavu vrlo intenzivne svjetlosti. Lako se otapa u kiselinama a reagira i s vodom na povišenim temperaturama uz oslobađanje vodika. Magnezij se upotrebljava kao snažno redukcijsko sredstvo koje može reducirati mnoge metalne okside. Najvažniji izvor magnezija su minerali dolomit (CaCO3·MgCO3) i magnezit (MgCO3), te morska voda. Glavno područje primjene magnezija je metalurgija, posebno za izradu lakih legura.
živa → mercury
Živa je poznata od davnih vremena (~1500. godine prije Krista). Ime je dobila od latinske riječi hydrargyrum što znači tekuće srebro. To je sjajni, srebrno bijeli metal. Pri sobnoj temperaturi je tekućina. Loše vodi toplinu i električnu struju. Stabilna je na zraku. Ne reagira s lužinama i većinom kiselina. Otapa se samo u oksidirajućim kiselinama. Tekuća živa otapa mnoge metale dajući amalgame. Ovisno o količini otopljenog metala, amalgami mogu biti tekući ili čvrsti. Živine pare su vrlo otrovne. Lako se resorbira čak i preko nepokrivenih dijelova kože. Imaju kronični kumulativni efekt. Organski spojevi žive, kao što je metil-živa, su također jaki otrovi. U prirodi žive ima dvadesetak puta više nego kadmija. Može se pronaći samorodna ili u mineralu cinabaritu (HgS). Klor-alkalne elektrolize su najveći potrošači žive gdje se živa upotrebljava kao katoda kod elektrolize, zbog velikog prenapona vodika na njoj i stvaranja amalgama s produktom. Sa živom se pune termometri, barometri ili se izrađuju lampe koje isijavaju svjetlost bogatu ultraljubičastim zrakama.
neodimij → neodymium
Neodimij je 1885. godine otkrio Carl F. Auer von Welsbach (Austrija). Ime je dobio po grčkim riječima neo i didymos što znači novi blizanac. To je srebrno bijeli metal koji brzo potamni na zraku. Sporo reagira s hladnom vodom, a mnogo brže s toplom. Zapali se na zraku kada se zagrije i izgara do Nd2O3. Glavni izvor lakih lantanoida je mineral monacit (Ce, La, Nd, Pr fosfat) koji se nalazi u monacitnim pijescima. Koristi se za izradu piroforne legure od koje se rade kremenčići za upaljače. Boji staklo od čisto ljubičaste do vinsko crvene. Staklo koje sadrži neodimij može se upotrebljavati za lasere i u astronomiji.
nikal → nickel
Nikal je 1751. godine otkrio Axel Fredrik Cronstedt (Švedska). Ime je dobio po imenu demonskog bića iz germanske mitologije od njemačke riječi kupfernickel što znači Old Nick bakar ili Vražji bakar. To je sjajni, srebrno bijeli metal koji zajedno sa željezom i kobaltom čini trijadu željeza. Mekan je, kovak i savitljiv i može se polirati do visokog sjaja. Otporan je na koroziju u zraku. Topljiv u razrijeđenim oksidirajućim kiselinama, a u koncentriranoj nitratnoj kiselini se pasivira. Vrlo je otporan na lužine sve do temperature od 500 °C. Duža izloženost niklenoj prašini i nekim njegovim spojevima je kancerogena. Nikal se u prirodi najčešće javlja kao garnierit ((Ni, Mg)6Si4O10(OH)8), pentlandit ((Ni, Fe)9S8) i niklein (NiAs). Više od tri četvrtine nikla upotrebljava se za izradu različitih legura sa i bez željeza. Ostatak se upotrebljava za galvansko niklanje materijala, za katalizatore, za izradu Ni-Cd baterija i kovanog novca.
dušik → nitrogen
Dušik je 1772. godine otkrio Daniel Rutherford (Škotska). Ime mu dolazi od grčkog naziva za salitru - nitron i riječi genesis što znači stvarati. Lavoisier mu je dao ime azote od grčke riječi azotikos što znači onaj koji ne podržava život. To je plin bez boje i mirisa koji je skoro inertan na sobnoj temperaturi. Dio je mnogih organskih i anorganskih spojeva. Ne gori niti podržava gorenje. Nalazi se slobodan u zraku (78 %) kao i vezan u spojevima salitri (KNO3), čilskoj salitri (NaNO3), amonijaku (NH3). Dobiva se destilacijom tekućeg zraka. Upotrebljava se kao sirovina za dobivanje dušične kiseline, amonijaka, umjetnih gnojiva, eksploziva.
osmij → osmium
Osmij je 1803. godine otkrio Smithson Tennant (Engleska). Ime je dobio prema grčkoj riječi osme što znači miris zbog otrovnog mirisa hlapljivog tetraoksida. To je sjajni srebrni metal, ekstremno tvrd i krt na povišenim temperaturama. Zajedno s iridijem i platinom čini skupinu teških platinskih metala. Stabilan je na zraku, u vodi i kiselinama. Sprašeni metal oksidira u lako hlapljivi tetraoksid, vrelišta na 130 °C, karakterističnog mirisa sličnog kloru i jako otrovnog. Pare OsO4 naročito oštećuju sluznicu oka. U prirodi se pojavljuje obično kao pratitelj bakarnih i nikalnih ruda, ili kao osmiridij (prirodna legura osmija i iridija) koja sadrži rutenij. Upotrebljava se za legiranje platine i paladija (povećava im tvrdoću).
Ostwaldov proces → Ostwald’s process
Ostwaldov proces je proces kojim se u tri stupnja dobiva nitratna kiselina, u prvom stupnju reagiraju amonijak i kisik (uz platina-rodij kao katalizator) čime nastaje dušikov monoksid i voda
U drugom stupnju dušikov monoksid reagira s kisikom pri čemu nastaje dušikov dioksid
U trećem stupnju otapanjem nastalog dušikovog dioksida u prisustvu zraka dobivamo nitratnu kiselinu
kisik → oxygen
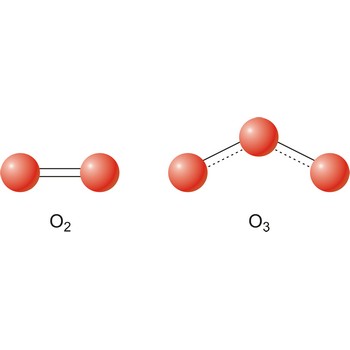
Kisik je 1774. godine otkrio Joseph Priestley (Engleska). Ime mu je dao Lavoisiera od grčke riječi oxys što znači oštar ili kiseo i riječi genes što znači tvoriti. To je plin bez boje i mirisa i ekstremno je reaktivan. Stvara okside sa svim ostalim elementima izuzev plemenitih plinova. Kisik je nezapaljivi plin ali podržava gorenje. Nešto je teži od zraka i dobro se otapa u vodi, topljivost mu je oko 3 % (volumna). Javlja se u dvije alotropske modifikacije, kao dvoatomna i kao troatomna molekula (ozon). I jedna i druga su jaka oksidacijska sredstva. Topljivost ozona u vodi je gotovo 50 puta veća nego topljivost dvoatomnog kisika. Kisik je najrasprostranjeniji element Zemljine kore. Skoro polovica mase je kisik, a po broju atoma je brojniji nego svi ostali elementi zajedno. Kisik se industrijski dobiva ili frakcijskom destilacijom ukapljenog zraka ili elektrolizom vode. Najčešće se upotrebljava kao oksidacijsko sredstvo.
ozon → ozone
Ozon je alotropska modifikacija kisika kod koje se kisik pojavljuje u molekulama koje se sastoje od tri atoma. Nastaje u atmosferi prilikom električnih pražnjenja i djelovanjem ultraljubičastih zraka.
Ozon je modrikasti plin karakterističnog mirisa. Topljivost u vodi mu je oko 50 puta veća nego kisika. Poslije fluora najjače je oksidacijsko sredstvo.
Citiranje ove stranice:
Generalić, Eni. "X-zrake." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav