Faradayevi zakoni elektrolize → Faraday’s laws of electrolysis
Faradayevi zakoni elektrolize su dva zakona koja je formulirao britanski kemičar i fizičar Michael Faraday (1791.-1867.):
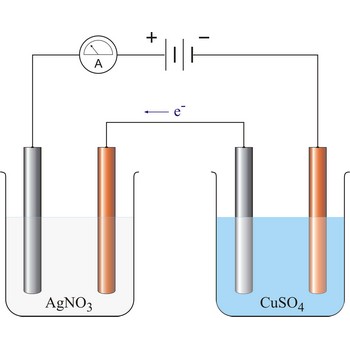
1. Količina tvari koja se izluči na elektrodi proporcionalna je količini naboja (Q = I·t) koja je protekla tijekom elektrolize.
gdje je z = broj elektrona koji se izmijeni u reakciji a F = Faradayeva konstanta i iznosi 96 487 C mol-1.
2. Mase elemenata koje se izluče s istom količinom struje su direktno proporcionalnu njihovim kemijskim ekvivalentima.
Prolaskom struje od 96 487 C u prvom elektrolizeru razvit će se 1 mol Ag i 1/4 mol O2 a u drugom 1/2 mol Cu i 1/4 mol O2. Relevantne polureakcije su
Gibbsova slobodna energija → Gibbs free energy
Gibbsova slobodna energija (G) jest energija oslobođena ili apsorbirana u reverzibilnom procesu pri konstantnoj temperaturi i tlaku. Definirana je jednadžbom
gdje je H entalpija, S entropija a T termodinamička temperatura. Naziva se još i Gibbsova energija ili samo slobodna energija.
Promjena Gibbsove slobodne energije, ΔG, određuje smjer kemijske reakcije. Ako je ΔG neke reakcije negativan, reakcija će se spontano odvijati dok se ne uspostavi ravnotežno stanje. Kada je postignuto ravnotežno stanje, onda je ΔG = 0.
fazni dijagram → phase diagram
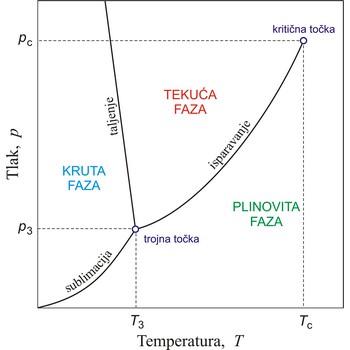
Ravnotežna stanja koja se uspostavljaju, pri određenim uvjetima, između pojedinih agregatnih stanja ili faza prikazuju se faznim dijagramom ili dijagramom stanja.
Krivulje na faznom dijagramu prikazuju ravnotežna stanja između dviju faza. Točku u kojoj su sve tri faze u ravnoteži nazivamo trojna točka. Krivulja isparavanja završava u kritičnoj točki. Iznad te temperature (kritična temperatura) ni u kojim uvjetima ne može se vodena para prevesti u tekuće stanje.
termodinamički zakoni → thermodynamic laws
Termodinamički zakoni temelj su termodinamike:
Prvi zakon ili zakon o očuvanju energije glasi: "Suma svih oblika energije u zatvorenom sustavu konstantna je."
Drugi zakon: "Toplina ne može sama od sebe prijeći s hladnijeg na toplije tijelo, i to ni neposredno ni posredno."
Treći zakon: "Entropija savršenog kristala približava se nuli kako se termodinamička temperatura približava nuli."
destilacija → distillation
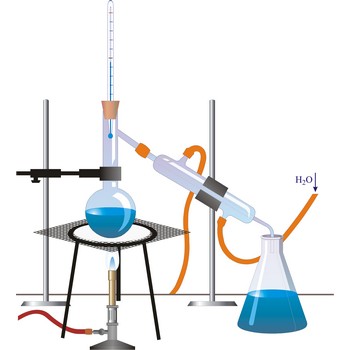
Destilacija je postupak koji služi za odjeljivanje ili prečišćavanje komponenti iz njihovih smjesa. Tekućina se zagrijava na temperaturu vrenja a nastale se pare kondenziraju i prikupljaju (destilat). U parnoj fazi ima više lakše hlapljive komponente nego u tekućoj fazi, u kojoj raste sadržaj komponente s višim vrelištem. Parcijalni tlak pojedine komponente ovisi o koncentraciji te komponente u smjesi i definiran je Raoultovim zakonom. Za odvajanje tekućina bliskog vrelišta provodimo frakcijsku destilaciju U tvari osjetljivih na povišenu temperaturu upotrebljava se vakuumska destilacija (sniženjem tlaka snižava se vrelište smjese).
apsorbancija → absorbance
Apsorbancija (A) je logaritam omjera intenziteta upadnog zračenja (Po) i propuštenog zračenja (P) kroz uzorak (izuzimajući efekte posude u kojoj je uzorak).
Apsorpcija svjetlosti kroz otopine može se matematički opisati Beer-Lambertovim zakonom
gdje je A apsorbancija na danoj valnoj duljini svjetlosti, ε je molarni apsorpcijski (ekstinkcijski) koeficijent (L mol-1 cm-1), svojstven svakoj molekulskoj vrsti i ovisan o valnoj duljini svjetlosti, b je duljina puta svjetlosti kroz uzorak (cm) a c je koncentracija tvari u otopini (mol L-1).
apsorpcija → absorption
Apsorpcija je pojava da tvar iz jedne faze prolazi graničnu površinu i u drugoj se fazi više ili manje jednolično raspodjeljuje u koncentraciji većoj nego što je u unutrašnjosti prve faze.
koeficijent aktiviteta → activity coefficient
Koeficijent aktiviteta (γ ili f) pokazuje odstupanje otopine od idealnog ponašanja. Koeficijent aktiviteta nekog iona opada s porastom koncentracije i naboja svih prisutnih iona u otopini. Tek kod vrlo razrijeđenih otopina koeficijent aktiviteta približava se jedinici. U jako razrijeđenim otopinama, kod kojih je m manje od 0.01, za približno određivanje koeficijenta aktiviteta može se upotrijebiti Debye-Huckelov granični zakon
gdje je γi = koeficijent aktiviteta vrste i, z = naboj iona a μ = ionska jakost otopine.
Koeficijent aktiviteta neelektrolita, odnosno neutralnih molekula jednak je jedinici.
adsorpcija → adsorption
Adsorpcija je pojava da se na graničnoj površini između dviju faza (površini čvrstog tijela okruženog tekućinom ili plinom) nakuplja neka tvar u koncentraciji većoj nego što vlada u unutrašnjosti susjednih faza. Tvar na kojoj se vrši adsorpcija naziva se adsorbens. Za dobre adsorbense karakteristično je da imaju vrlo veliku površinu.
Citiranje ove stranice:
Generalić, Eni. "Gibbsov zakon faza." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav