Rezultati 1–10 od 10 za Faradayev kavez
Faradayev kavez → Faraday cage
Faradayev kavez predstavlja zaštitu od električnog polja. Sastoji se od metalne mreže, odnosno kaveza unutar kojeg se nalazi električna oprema koja se na taj način štiti od djelovanja električnog polja. Ime je dobio prema britanskom znanstveniku Michaelu Faradayu (1791.-1867.).
Faradayeva konstanta → Faraday constant
Faradayeva konstanta (F) električni je naboj jednog mola jednostruko nabijenih pozitivnih iona.
gdje je NA Avogadrova konstanta (6.022×1023 mol-1) a e naboj elektrona (1.602×10-19 C).
Faradayevi zakoni elektrolize → Faraday’s laws of electrolysis
Faradayevi zakoni elektrolize su dva zakona koja je formulirao britanski kemičar i fizičar Michael Faraday (1791.-1867.):
1. Količina tvari koja se izluči na elektrodi proporcionalna je količini naboja (Q = I·t) koja je protekla tijekom elektrolize.
gdje je z = broj elektrona koji se izmijeni u reakciji a F = Faradayeva konstanta i iznosi 96 487 C mol-1.
2. Mase elemenata koje se izluče s istom količinom struje su direktno proporcionalnu njihovim kemijskim ekvivalentima.
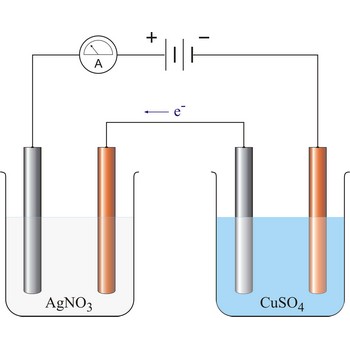
Prolaskom struje od 96 487 C u prvom elektrolizeru razvit će se 1 mol Ag i 1/4 mol O2 a u drugom 1/2 mol Cu i 1/4 mol O2. Relevantne polureakcije su
Bunsenov plamenik → Bunsen burner
Bunsenov plamenik standardni je izvor topline u laboratoriju. Faradayev izum usavršio je njemački kemičar Roberts Bunsen (1811.-1899.) za potrebe svojih radova na spektroskopiji. Bunsenov plamenik sastoji se od metalne cijevi kroz koju se usmjerava mlaz plina i postolja. Zrak se uvlači kroz otvore na dnu cijevi prekrivene prstenom kojim se regulira protok zraka. Kada prsten potpuno prekriva otvore plamenik gori žutim sigurnosnim plamenom. Uz potpuno slobodne otvore, u cijevi je dovoljno zraka i plin gori plavim plamenom koji dostiže temperature od 1 500 °C. Bunsenovim plamenikom može se zagrijava izravno plamenom ili posredno preko azbestne mrežice i vodene kupelji.
Bunsen, Robert Wilhem → Bunsen, Robert Wilhem
Robert Wilhem Bunsen (1811.-1899.) njemački je kemičar koji je imao profesuru u Kasselu, Marburgu i Heidelbergu. Njegova rana istraživanja na organometalnim spojevima arsena dovela su, zbog eksplozije, do gubitka jednog oka. Bunsenov najvažniji rad je razvoj nekoliko tehnika za odvajanje, identificiranje i mjerenje različitih tvari. Unaprijedio je galvanski članak kako bi mogao izolirati čiste metale - Bunsenov članak.
Osnovni komad laboratorijskog pribora, plamenik koji nosi njegovo ime, nije izumio on već je unaprijedio Faradayev izum za potrebe svojih istraživanja spektroskopije. Kombinacijom Bunsenovog plamenika i staklene prizme (Bunsen-Kirchhoffov spektroskop) zajedno s njemačkim fizičarom Gustavom Kirchoffom otkrio je cezij (1860.) i rubidij (1861.).
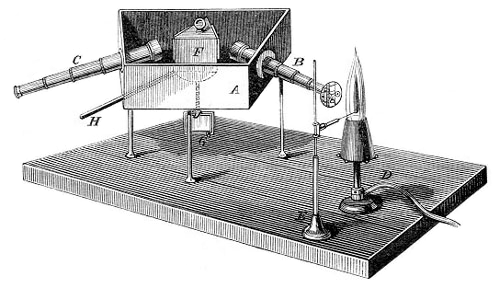
kulometrija → coulometry
Kulometrija je kvantitativna elektrokemijska analitička metoda koja se sastoji od mjerenja protekle količine elektriciteta. Temelji se na Faradayevim zakonima.
Ilkovičeva jednadžba → Ilkovic equation
Ilkovičeva jednadžba je relacija koja se koristi u polarografiji a daje odnos između difuzijske struje (id) i koncentracije (c) depolarizatora, tj difundirajuće elektroaktivne vrste koja se reducira ili oksidira na kapajućoj živinoj elektrodi. Jednadžbu je 1934. izveo slovački fizičar Dionýz Ilkovič (1907.-1980.) primjenom Fickovih zakona difuzije.
gdje je k konstanta Ilkovičeve jednadžbe koja uključuje Faradayevu konstantu, π i gustoću žive i iznosi 708 za maksimalnu a 607 za prosječnu graničnu struju, D je koeficijent difuzije depolarizatora u danom mediju (cm2/s), n je broj elektrona izmijenjenih na elektrodi, m je brzina istjecanja žive kroz kapilaru (mg/sec), t je vrijeme kapanja a c je koncentracija depolarizatora (mol/cm3).
Nernstova jednadžba za elektrodni potencijal → Nernst’s electrode potential equation
Za opću reakciju nekog redoks-sustava
ovisnost elektrodnog potencijala redoks sustava o aktivitetu oksidiranog i reduciranog oblika u otopini daje nam Nernstova jednadžba za elektrodni potencijal:
gdje je E = elektrodni potencijal redoks-sustava
E° = standardni elektrodni potencijal redoks-sustava
R = univerzalna plinska konstanta
T = termodinamička temperatura
F = Faradayeva konstanta
z = broj elektrona koji se izmjenjuju u redoks-reakciji
aO = aktivitet oksidiranog oblika
aR = aktivitet reduciranog oblika
n = stehiometrijski koeficijent oksidiranog oblika
m = stehiometrijski koeficijent reduciranog oblika
superkritična fluidna ekstrakcija → supercritical fluid extraction
Superkritična fluidna ekstrakcija (SFE) je slična ekstrakciji s organskim otapalima ali s boljom difuzijom, nižom viskoznošću i manjom napetošću površine. Glavne prednost upotrebe superkritičnih fluida za ekstrakciju su niska cijena, neotrovnost i mnogo jednostavnije i jeftinije uklanjanje otapala nego kod ekstrakcije s organskim otapalima. SFE je jednostavno najbolja tehnologija za ekstrakciju osjetljivih materijala. Suprekritični ugljikov dioksid (scCO2) se upotrebljava za ekstrakciju kofeina iz kave i čaja. Pri tome on prodire duboko u zeleno zrno i otapa od 97 % do 99 % prisutnog kofeina.
Heyrovsky-Ilkovičeva jednadžba → Heyrovsky-Ilkovic equation
U polarografiji, Heyrovsky-Ilkovičeva jednadžba opisuje krivulju ovisnosti jakosti struje o potencijalu (polarografski val) reverzibilnih redoks sustava
gdje je R opća plinska konstanta, T je apsolutna temperatura, F je Faradayeva konstanta, n je broj elektrona izmijenjenih u elektrodnoj reakciji a D i D1 su koeficijenti difuzije. E1/2 je potencijal karakterističan za danu reakciju i osnovni elektrolit (poluvalni potencijal).
Kako bi dobili E1/2 iz gornje jednadžbe nacrtat ćemo graf ovisnosti ln[(id-i)/i] o potencijalu. Vrijednost E1/2 očita se iz grafa u točki u kojoj pravac siječe ordinatu. Ako su procesi na elektrodi reverzibilni iz nagiba pravca (nF/RT) može se izračunati broj izmijenjenih elektrona, n.
Citiranje ove stranice:
Generalić, Eni. "Faradayev kavez." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav