glukoza → glucose
Glukoza (grožđani šećer, krvni šećer) ugljikohidrat je iz skupine monosaharida ili jednostavnih šećera kemijske formule C6H12O6. Stari naziv dekstroza potječe od toga što glukoza zakreće ravninu polarizirane svjetlosti u desno. Prema broju ugljikovih atoma u svojoj molekuli glukoza je heksoza, a prema funkcionalnoj skupini aldoza (aldoheksoza). Glukoza je najrasprostranjeniji šećer u prirodi. Slobodna se nalazi u raznom voću i medu a vezana u disaharidima (saharozi, maltozi, laktozi), polisaharidima (škrobu, glikogenu, celulozi) i raznim drugim spojevima. Kod čovjeka se može naći slobodna u krvi ili kao rezerva pohranjena u jetri i mišićima u obliku glikogena.
Glukozu sintetiziraju biljke procesom fotosinteze i pohranjuju u polimernom obliku kao škrob. U probavnom sustavu škrob se hidrolizira u glukozu koja se zatim iskorištava u stanicama za dobivanje energije. Ukupno se iz jedne molekule glukoze može dobiti 36 molekula ATP-a.
Zbog tetraedarskih kutova koje čine veze među ugljikovim atomima, molekula glukoze može zauzeti takvu konformaciju da hidroksilna skupina vezana na petom ugljikovom reagira s karbonilnom skupinom pri čemu nastaje poluacetal, odnosno šesteročlani heterociklički prsten. Time se javlja još jedan asimetrični centar na atomu C-1, tako da D-glukoza može postojati u dva oblika, kao α-D-glukopiranoza i β-D-glukopiranoza. Ta su dva ciklička oblika u ravnoteži, tj. oni mogu preći jedan u drugog preko aldehidnog oblika.
invertni šećer → invert sugar
Invertni šećer je smjesa jednakih količina glukoze i fruktoze nastala hidrolizom saharoze (običnog šećera). Ime mu dolazi od činjenice da nastala smjesa zakreće ravninu polarizirane svjetlosti u suprotnom smjeru od saharoze. Saharoza zakreće ravninu polarizirane svjetlosti udesno ([α]D = +66.5°). Invertni šećer zakreće ravninu polarizirane svjetlosti u lijevo ([α]D = -22°) (obrnuto od kazaljke na satu) zbog jakog utjecaja ljevokretne prirode fruktoze ([α]D = -92°).
Pravljenje umjetnog meda (invertni šećerni sirup): Otope se dva dijela šećera (1 kg) u jednom dijelu vode (0.5 kg) uz miješanje i lagano zagrijavanje. Doda se 1 g limunske kiseline ili sok od jednog limuna. Smjesa se zagrije do laganog vrenja i tako održava između 15 minuta i jednog sata. Krajnji rezultat je ljepljivi zlatni sirup koji se ostavi na sobnoj temperaturi da se ohladi.
Gratzelova sunčeva ćelija → Gratzel solar cell
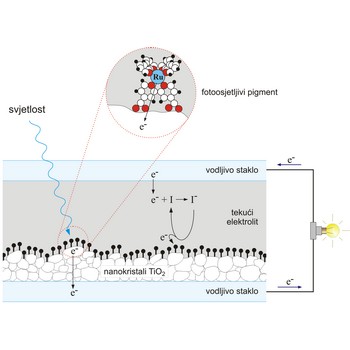
Grätzelova sunčeva ćelija je fotoelektrokemijska ćelija koju je razvio Michael Grätzel sa suradnicima. Oponaša djelomice prirodnu sunčevu ćeliju, koja omogućava biljkama da ostvare fotosintezu. U prirodnoj sunčevoj ćeliji molekule klorofila apsorbiraju svjetlost i to najjače u crvenom i plavom dijelu spektra, dok se zelena svjetlost reflektira. Apsorbirana energija dovoljna je za izbacivanje elektrona iz pobuđenog klorofila. U prijenosu tog naboja, sudjeluju potom druge molekule. U Grätzelovoj ćeliji su, također, za stvaranje naboja apsorpcijom svjetlosti i prijenos tog naboja "zaduženi" različiti dijelovi ćelije.
Na vodljivo staklo nanesen je sloj nanokristala poluvodiča TiO2 čija je površina jako velika. Na TiO2 nanesen je fotoosjetljivi pigment koji čine rutenijevi ioni povezani s organskim molekulama koje jako apsorbiraju vidljivu svjetlost. Fotopobuđeni elektroni prelaze s rutenijevih iona na kristalite TiO2, koji ih odvode daleko od iona-donora. Čitav sustav uronjen je u tekući jodidni elektrolit koji preuzima elektrone s elektrode i prenosi ih na rutenijeve ione kako bi se nastavio proces apsorpcije svjetlosti.
Efikasnost ovih ćelija iznosi oko 10 % i raste u difuznoj svjetlosti, tj. za oblačna vremena.
luminiscencija → luminescence
Luminiscencija (latinski lumen znači svjetlo) je zajednički naziv za pojave emisije elektromagnetskog zračenja (UV, vidljivog ili IR) atoma ili molekula kao posljedica prijelaza elektrona iz pobuđenog u niže energetsko stanje, obično u osnovno stanje. Kako se pojava svijetljenja odvija bez zračenja topline naziva se i hladno svjetlucanje. Može biti izazvana kemijskim procesom (kemoluminiscencija), biološkim procesom (bioluminiscencija), djelovanjem alfa i ß-zraka (radioluminiscencija), svjetlosti (fotoluminiscencija), električne struje (elektroluminiscencija), topline (termoluminiscencija), mrvljenjem (triboluminiscencija) i sl.
S obzirom na trajanje sekundarnog zračenja luminescencija se dijeli na:
- fluorescenciju - traje samo dok djeluje pobuda
- fosforescenciju - sekundarno zračenje traje i nakon prestanka pobude.
magnezij → magnesium
Magnezij je 1808. godine otkrio Sir Humphry Davy (Engleska). Ime mu potječe od grčkog naziva za magnezijev oksid (MgO) - magnesia alba, prema okrugu u Thessaly, Grčka. To je polutvrdi, sjajni, srebrno bijeli metal, koji na zraku potamni zbog zaštitne prevlake oksida. Može se kovati, lijevati i valjati. Gori na zraku uz pojavu vrlo intenzivne svjetlosti. Lako se otapa u kiselinama a reagira i s vodom na povišenim temperaturama uz oslobađanje vodika. Magnezij se upotrebljava kao snažno redukcijsko sredstvo koje može reducirati mnoge metalne okside. Najvažniji izvor magnezija su minerali dolomit (CaCO3·MgCO3) i magnezit (MgCO3), te morska voda. Glavno područje primjene magnezija je metalurgija, posebno za izradu lakih legura.
ekvivalencija mase i energije → mass-energy equivalence
U specijalnoj teoriji relativnosti Einstein je pokazao da se masa i energija ne mogu očuvati odvojeno već se može govoriti samo o očuvanju ukupne mase i energije sustava. Energijski ekvivalent mase dan je vjerojatno najpoznatijom jednadžbom:
u kojoj je m masa tijela a c brzina svjetlosti. Cockcroft i Walton (1932.) su prvi dokazali ispravnost Einsteinove jednadžbe.
živa → mercury
Živa je poznata od davnih vremena (~1500. godine prije Krista). Ime je dobila od latinske riječi hydrargyrum što znači tekuće srebro. To je sjajni, srebrno bijeli metal. Pri sobnoj temperaturi je tekućina. Loše vodi toplinu i električnu struju. Stabilna je na zraku. Ne reagira s lužinama i većinom kiselina. Otapa se samo u oksidirajućim kiselinama. Tekuća živa otapa mnoge metale dajući amalgame. Ovisno o količini otopljenog metala, amalgami mogu biti tekući ili čvrsti. Živine pare su vrlo otrovne. Lako se resorbira čak i preko nepokrivenih dijelova kože. Imaju kronični kumulativni efekt. Organski spojevi žive, kao što je metil-živa, su također jaki otrovi. U prirodi žive ima dvadesetak puta više nego kadmija. Može se pronaći samorodna ili u mineralu cinabaritu (HgS). Klor-alkalne elektrolize su najveći potrošači žive gdje se živa upotrebljava kao katoda kod elektrolize, zbog velikog prenapona vodika na njoj i stvaranja amalgama s produktom. Sa živom se pune termometri, barometri ili se izrađuju lampe koje isijavaju svjetlost bogatu ultraljubičastim zrakama.
metar → metre
Metar (m) je osnovna SI jedinica za duljinu.
Metar je duljina koja odgovara putu što ga prijeđe svjetlost u vakuumu za vrijeme od 1/299 792 458 s.
Ova definicija, prihvaćena na Generalnoj konferenciji za mjere i utege u listopadu 1983., zamijenila je definiciju iz 1967. temeljenu na kriptonovoj lampi.
mikroskop → microscope
Mikroskop je naprava koja stvara uvećanu sliku malih objekata. Optički (svjetlosni mikroskop) koristi vidljivu svjetlost i sustav leća za prikazivanje uvećane slike objekta. Tipično povećanje optičkog mikroskopa je 1500× ("1500 puta") s teoretskom granicom razlučivosti od 200 nm. Za razliku od svjetlosnih, elektronski mikroskopi koriste prolazak elektronsko snopa kroz, ili preko površine uzorka. Kako elektronski snop ima mnogo manju valnu duljinu od svjetlosti s elektronskim mikroskopom mogu se vidjeti objekti manji od 2 nm.
Citiranje ove stranice:
Generalić, Eni. "Svjetlost." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav