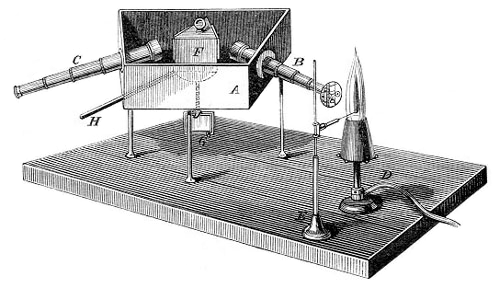
Bunsenov plamenik → Bunsen burner
Bunsenov plamenik standardni je izvor topline u laboratoriju. Faradayev izum usavršio je njemački kemičar Roberts Bunsen (1811.-1899.) za potrebe svojih radova na spektroskopiji. Bunsenov plamenik sastoji se od metalne cijevi kroz koju se usmjerava mlaz plina i postolja. Zrak se uvlači kroz otvore na dnu cijevi prekrivene prstenom kojim se regulira protok zraka. Kada prsten potpuno prekriva otvore plamenik gori žutim sigurnosnim plamenom. Uz potpuno slobodne otvore, u cijevi je dovoljno zraka i plin gori plavim plamenom koji dostiže temperature od 1 500 °C. Bunsenovim plamenikom može se zagrijava izravno plamenom ili posredno preko azbestne mrežice i vodene kupelji.
Bunsen, Robert Wilhem → Bunsen, Robert Wilhem
Robert Wilhem Bunsen (1811.-1899.) njemački je kemičar koji je imao profesuru u Kasselu, Marburgu i Heidelbergu. Njegova rana istraživanja na organometalnim spojevima arsena dovela su, zbog eksplozije, do gubitka jednog oka. Bunsenov najvažniji rad je razvoj nekoliko tehnika za odvajanje, identificiranje i mjerenje različitih tvari. Unaprijedio je galvanski članak kako bi mogao izolirati čiste metale - Bunsenov članak.
Osnovni komad laboratorijskog pribora, plamenik koji nosi njegovo ime, nije izumio on već je unaprijedio Faradayev izum za potrebe svojih istraživanja spektroskopije. Kombinacijom Bunsenovog plamenika i staklene prizme (Bunsen-Kirchhoffov spektroskop) zajedno s njemačkim fizičarom Gustavom Kirchoffom otkrio je cezij (1860.) i rubidij (1861.).
Bunsenov članak → Bunsen’s cell
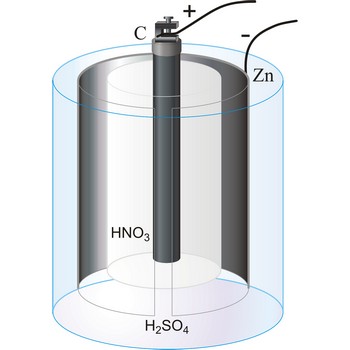
Bunsenov članak je primarni članak koji je razvio Robert W. Bunsen. Sastoji se od cinkove katode uronjene u razrijeđenu otopinu sumporne kiseline i ugljikove anode uronjene u koncentriranu otopinu dušične kiseline. Elektrolitske otopine odijeljene su poroznom stjenkom. Članak ima elektromotornu silu od 1.9 V.
bireta → burette
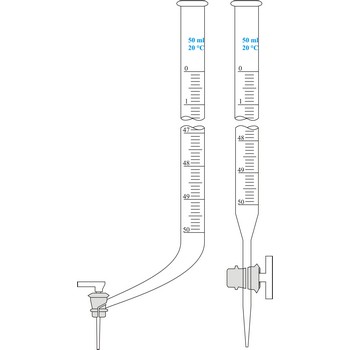
Bireta je graduirana staklena cijev koja na donjoj strani ima stakleni pipac pomoću kojeg se može ispustiti točno određena količina tekućine. Unutrašnji promjer birete mora u čitavoj dužini biti jednak jer o tome ovisi točnost mjerenja volumena. Birete se prvenstveno koriste u volumetrijskoj analizi za titraciju sa standardnom otopinom reagensa. Najčešće se koristi Schellbachova bireta od 50 mL s podjelom na 0.1 mL. Svaka bireta je kalibrirana na izljev. Za serijska određivanja upotrebljavaju se automatske birete.
kalandriranje → calendering
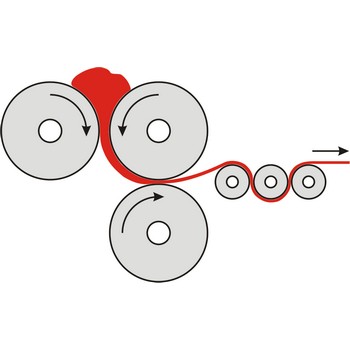
Kalandriranje je proces oblikovanja materijala u tanke filmove (foliju) njegovim provlačenjem između zagrijanih valjaka.
kalomel elektroda → calomel electrode
Kalomel elektroda referentna je elektroda temeljena na polureakciji
Tablica: Ovisnost potencijala kalomel elektrode o temperaturi i koncentraciji KCl prema standardnoj vodikovoj elektrodi
| potencijal prema SHE / V | |||
|---|---|---|---|
| t / °C | 0.1 mol dm-3 | 3.5 mol dm-3 | zasić. otop. |
| 15 | 0.3362 | 0.254 | 0.2511 |
| 20 | 0.3359 | 0.252 | 0.2479 |
| 25 | 0.3356 | 0.250 | 0.2444 |
| 30 | 0.3351 | 0.248 | 0.2411 |
| 35 | 0.3344 | 0.246 | 0.2376 |
kalorimetar → calorimeter
Kalorimetar je uređaj za određivanje količine topline koja se oslobađa ili troši tijekom neke kemijske reakcije. Služi i za određivanje specifične topline.
kondenzator → capacitor
Naprava koja pohranjuje električne naboje. Simbol za kondenzator u shemama strujnih krugova je —| |—.
ugljikohidrat → carbohydrate
Ugljikohidrati su polihidroksi aldehidi ili ketoni, ili spojevi koji hidrolizom daju takve spojeve. Često se upotrebljava i naziv saharidi, naziv izveden od latinskog naziva za šećer - saccharum). Ugljikohidrati su najraširenija klasa organskih spojeva i čine više od 50 % Zemljine suhe biomase. Sva hrana koju trošimo svoje porijeklo vuče iz biljaka koje, procesom fotosinteze, iz ugljikovog dioksida i vode stvaraju jednostavne šećere (glukozu). Složeniji ugljikohidrati, kao što su celuloza i škrob, nastaju iz glukoze. Klorofil u biljkama apsorpcijom Sunčeve svjetlosti dobiva energiju neophodnu za sintezu ugljikohidrata
U vrijeme kad još nije bila poznata njihova struktura ugljikohidrate se smatralo spojevima ugljika i vode što se moglo izraziti općom formulom Cx(H2O)y. Kasnija istraživanja pokazala su da ovi spojevi nisu hidrati ali ime je ostalo.
Ugljikohidrati se mogu podijeliti u dvije skupine: na jednostavne šećere (monosaharide), koji se ne mogu rastaviti na manje jedinice djelovanjem razrijeđene kiseline, i na složene šećere koji su sastavljeni od dvaju (disaharidi) ili više (oligosaharidi i polisaharidi) monosaharida povezanih acetalnom (glikozidnom) vezom. Složeni šećeri se hidrolizom mogu rastaviti na jednostavne šećere.
Carnotov kružni proces → Carnot cycle
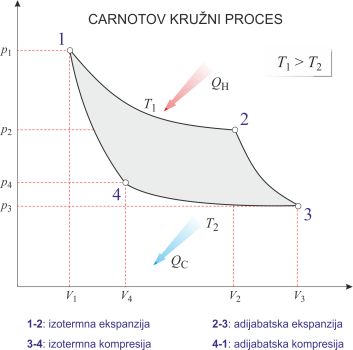
Francuski fizičar Nicolas Léonard Sadi Carnot (1796.-1832.) opisao je 1824. kružni proces pri kojem se prijelazom topline iz toplijeg spremnika u hladniji spremnik dobiva maksimalni rad. Carnotov kružni proces sastoji se od četiri povratljiva parcijalna procesa
1-2: Izotermna ekspanzija na temperaturi T1 uz dovođenje topline QH.
2-3: Adijabatska ekspanzija do temperature T2.
3-4: Izotermna kompresija na temperaturi T2 uz odvođenje topline QC.
4-1: Adijabatska kompresija nazad do temperature T1.
Izvršeni rad jednak je zbroju izvršenih radova parcijalnih procesa, a prikazan je osjenčanom površinom ograničenom krivuljama koje prikazuju promjene stanja.
Citiranje ove stranice:
Generalić, Eni. "Rare earth elements." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav