galvanski članak → galvanic celll
Galvanski članak (naponski članak, Voltin članak) jest elektrokemijski članak u kojem se kemijska energija spontano pretvara u električnu. Galvanski članak sastoji se od dva polučlanka, a svaki polučlanak od elektrode uronjene u elektrolit. Elektrolit može biti zajednički za obje elektrode ili različit za svaku elektrodu. Dva elektrolita odvajamo polupropusnom membranom ili ih spajamo elektrolitskim mostom. Ako se elektrode povežu nekim vodičem, elektroni putuju kroz vodič od negativnog pola prema pozitivnom polu.
Danielov članak je primjer galvanskog članka. Sastoji se od bakrene i cinkove elektrode, a kao elektrolit služe otopine bakrova(II) sulfata i cinkova sulfata odijeljene polupropusnom membranom. Kada se elektrode spoje električnim vodičem kroz strujni krug će proteći električna struja. Na negativnom polu (cinkovoj elektrodi) zbiva se proces oksidacije A na pozitivnom polu (bakrenoj elektrodi) zbiva se proces redukcije.
Elektromotornu silu galvanskog članka možemo izračunati iz razlike redoks potencijala tvari koja se reducirala (bakra) i tvari koja se oksidirala (cinka).
Galvanski članak može se shematski prikazati upotrebom okomite crte. Uobičajeno je da se oksidirana vrsta piše s lijeve strane.
Ime je dobila u čast talijanskog znanstvenika i liječnika Luigia Galvania (1737.-1798.).
boca ispiralica → gas washing bottle
Boca ispiralica (boca za pranje plinova ili Drechselova boca) omogućava jeftin ali učinkovit način za pranje i sušenje plinova. Plin u bocu ulazi kroz središnju vertikalnu dovodnu cijev čiji se vrh nalazi ispod površine medija za pranje (sušenje). Dovodna cijev na svom kraju može imati pločicu od sinteriranog stakla koja smanjuje veličinu mjehurića, čime se povećava kontaktna površina između plina i tekućine. Mjehurići plina prolaze kroz medij i izlaze kroz bočnu cijev koja se nalazi na vrhu boce. Ime je dobila po njemačkom kemičaru Edmundu Drechselu (1843.-1897.).
Gibbsov zakon faza → Gibbs phase rule
Gibbsov zakon faza određuje broj faza termodinamičkog sustava u ravnoteži. Dan je izrazom
gdje je C broj komponenti smjese, P je broj faza a F broj stupnjeva slobode, tj. broj neovisnih varijabli koje se mogu promijeniti a da se ne promijeni broj faza.
staklena elektroda → glass electrode
Staklena elektroda je elektroda osjetljiva na vodikove ione. Sastoji se od staklene membrane, unutarnje referentne elektrode i unutarnje otopine. Može se također prirediti i staklena elektroda osjetljiva na natrijeve ione.
Staklena elektroda ima ekstremno velik električni otpor. Membrana tipične staklene elektrode (debljine od 0.03 mm do 0.1 mm) ima električni otpor od 30 MΩ do 600 MΩ). Aktivitet vodikovih iona u unutrašnjoj otopini je stalan. Površina staklene membrane mora biti hidratizirana da bi djelovala kao pH elektroda. kada se staklena membrana uroni u vodenu otopinu na njenoj površini se formira tanki gel sloj pri čemu dolazi do ionske izmjene između iona natrija u kristalnoj rešetki stakla i vodikovog iona. Ista stvar se dešava i na unutrašnjoj strani membrane.
Najjednostavnije objašnjenje rada staklene membrane je da se staklo ponaša kao slaba kiselina (staklo-H).
Aktivitet vodikovih iona u unutrašnjoj otopini je stalan. Kada se na vanjskoj strani staklene membrane promijeni koncentracija vodikovih iona staklo će se protonirati ili deprotonirati. Razlika pH otopina s unutrašnje i vanjske strane staklene membrane stvara elektromotornu silu proporcionalnu toj razlici.
globalno zatopljenje → global warming
Globalno zatopljenje ili efekt staklenika pojava je koja se zbiva u atmosferi zbog prisustva određenih plinova koji apsorbiraju infracrveno zračenje. Vidljive i ultraljubičaste zrake sposobne su prodrijeti kroz atmosferu i zagrijati Zemljinu površinu. Ovu energiju Zemlja reemitira kao infracrveno zračenje, koje zbog veće valne duljine biva apsorbirano od strane ugljikova dioksida. Posljedica toga je povećanje srednje temperature Zemlje i njene atmosfere (globalno zatopljenje). Slično se dešava i u stakleniku gdje svjetlost i duže ultraljubičaste zrake mogu proći kroz staklo ali infracrvenu radijaciju staklo apsorbira i dio reemitira u staklenik.
Ova pojava se smatra velikim rizikom i opasnošću za okoliš. Prosječno povećanje temperature može promjeniti klimu te može dovesti do otapanja ledenih polarnih kapa, a onda bi porast razine mora mogao imati katastrofične posljedice. Pokraj ugljikova dioksida, koji nastaje sagorijevanjem fosilnih goriva, negativan utjecaj na atmosferu imaju dušikovi oksidi, ozon, metan i klorofluorougljici.
glutaminska kiselina → glutamic acid
Glutaminska kiselina spada u negativno nabijene aminokiseline. To je jedna od dvije aminokiseline koje sadrže karbonsku kiselinu u pobočnom lancu. Kao i sve nabijene aminokiseline i ova kiselina se često nalazi na površini bjelančevine utječući na njenu topljivost i ionski karakter. Asparaginska i glutaminska kiselina igraju važnu ulogu u aktivnim centrima enzima. Glutaminska kiselina se često naziva i glutamat jer je pri fiziološkom pH karboksilna kiselina disocirana u svoj anionski oblik. Glutaminska kiselina nije esencijalna kiselina jer ljudski organizam svu potrebnu kiselinu može sintetizirati iz drugih aminokiselina.
- Kratice: Glu, E
- IUPAC ime: 2-aminopentanska dikiselina
- Molekularna formula: C5H9NO4
- Molekularna masa: 147.13 g/mol
glicin → glycine
Glicin najjednostavnije je građena aminokiselina. Iako je nepolaran ne doprinosi hidrofobnim interakcijama. Nedostatak pobočnog lanca daje glicinu mnogo veću konformacijsku slobodu ugradnje u bjelančevine. Nalazi se u sastavu gotovo svih bjelančevina i to u visokom postotku. To je ujedno i jedina aminokiselina koja nije optički aktivna. Glicin nije esencijalna aminokiselina i u najvećoj mjeri nastaje iz serina, ali se može dobiti i iz treonina.
- Kratice: Gly, G
- IUPAC ime: 2-aminooctena kiselina
- Molekularna formula: C2H5NO2
- Molekularna masa: 75.07 g/mol
glikogen → glycogen
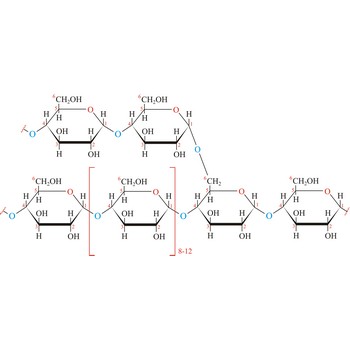
Glikogen ili animalni škrob je polisaharid koji životinje (među njima i čovjek) koriste za skladištenje molekula glukoze. Organizam stvara glikogen iz viška glukoze i pohranjuje ga u jetri i mišićnom tkivu. Struktura mu je slična strukturi amilopektina iz škroba, ali je mnogo razgranatiji i veće relativne molekularne mase (može se sastojati od preko 100 000 glukoznih jedinica). Osnovni lanci glikogena sastoje se od molekula glukozne povezanih α(1→4) glikozidnim vezama. Pobočni lanci, vezani α(1→6) glikozidnim vezama, granaju se na približno svakih 10 ostataka glukoze (kod amilopektina je grananje na približno svakih 25 glukoznih jedinica). Pri napornom radu glikogen se cijepa nazad u glukozu a razgranata struktura omogućuje enzimima da hidrolizu započnu na više mjesta i tako brzo stvore organizmu potrebnu glukozu.
Citiranje ove stranice:
Generalić, Eni. "Periodni_sustav_elemenata." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav