nezasićeni ugljikovodik → unsaturated hydrocarbon
Nezasićeni ugljikovodici u svojoj molekuli sadrže ugljikove atome povezane dvostrukim (alkeni) ili trostrukim vezom (alkini).
van der Waalsova sila → van der Waals’ force
Van der Waalsova sila jest slaba privlačna sila između dviju molekula koja se javlja zbog interakcije električkih dipola. Može dovesti do stvaranja stabilnih, ali slabo povezanih dimernih molekula ili skupina. Nazvane su po nizozemskom fizičaru Johannesu van der Waalsu (1837.-1923.).
Gratzelova sunčeva ćelija → Gratzel solar cell
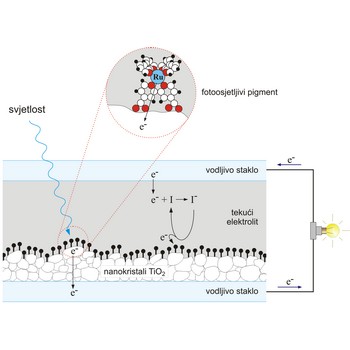
Grätzelova sunčeva ćelija je fotoelektrokemijska ćelija koju je razvio Michael Grätzel sa suradnicima. Oponaša djelomice prirodnu sunčevu ćeliju, koja omogućava biljkama da ostvare fotosintezu. U prirodnoj sunčevoj ćeliji molekule klorofila apsorbiraju svjetlost i to najjače u crvenom i plavom dijelu spektra, dok se zelena svjetlost reflektira. Apsorbirana energija dovoljna je za izbacivanje elektrona iz pobuđenog klorofila. U prijenosu tog naboja, sudjeluju potom druge molekule. U Grätzelovoj ćeliji su, također, za stvaranje naboja apsorpcijom svjetlosti i prijenos tog naboja "zaduženi" različiti dijelovi ćelije.
Na vodljivo staklo nanesen je sloj nanokristala poluvodiča TiO2 čija je površina jako velika. Na TiO2 nanesen je fotoosjetljivi pigment koji čine rutenijevi ioni povezani s organskim molekulama koje jako apsorbiraju vidljivu svjetlost. Fotopobuđeni elektroni prelaze s rutenijevih iona na kristalite TiO2, koji ih odvode daleko od iona-donora. Čitav sustav uronjen je u tekući jodidni elektrolit koji preuzima elektrone s elektrode i prenosi ih na rutenijeve ione kako bi se nastavio proces apsorpcije svjetlosti.
Efikasnost ovih ćelija iznosi oko 10 % i raste u difuznoj svjetlosti, tj. za oblačna vremena.
hematit → haematite
Hematit, Fe2O3, najrašireniji je i najstabilniji željezov oksid te jedna od najzastupljenijih željezovih ruda u prirodi. U laboratorijskim uvjetima hematit se može pripraviti različitim metodama kemijske sinteze. Kontrolom uvjeta sinteze pripravljaju se čestice hematita različitih oblika i veličine. Oblik i veličina kristala hematita određuju njegova fizikalna svojstva, a time i komercijalnu primjenu, npr. kao pigmenata, senzora ili katalizatora.
Željezovi oksidi imaju značajnu tehnološku primjenu. Tradicionalno se upotrebljavaju kao pigmenti, pokrivaju široki raspon boja od žute do crne. Željezovi oksidi kao pigmenti otporni su na kiseline i lužine te visoke temperature. Osim u proizvodnji boja koriste se u gumarskoj i građevinskoj industriji te industriji papira. Budući da su željezovi oksidi netoksični kao pigmenti, koriste se i u prehrambenoj, kozmetičkoj i farmaceutskoj industriji.
vertikalna energija ionizacije → vertical ionisation energy
Vertikalna energija ionizacije je energija potrebna da se ukloni elektron iz atoma, molekule ili iona u plinovitoj fazi bez da se ukloni bilo koja jezgra. Vertikalna energija ionizacije je veća ili jednaka adijabatskoj energiji ionizacije.
valna funkcija → wavefunction
Valna funkcija (Ψ) matematička je funkcija koja amplitudu vala opisuje kao funkciju položaja (i ponekad kao funkciju vremena i/ili elektronskog spina). Valna funkcija koristi se u kemiji i njome se opisuje ponašanje elektrona vezanih na atome ili u molekule.
slabi elektrolit → weak electrolyte
Slabi elektroliti su oni elektroliti koji u vodenim otopinama samo djelomično disociraju na ione i koji su u ravnoteži s nedisociranim molekulama. Njihove vodene otopine slabo provode električnu struju. Npr. acetatna kiselina samo djelomično disocira pa otopina acetatne kiseline sadrži molekule acetatne kiseline, vodikove ione i acetatne ione.
halogeni elementi → halogens
U 17. skupinu periodnog sustava spadaju fluor (F), klor (Cl), brom (Br), jod (I) i astat (At). Zajedničkim imenom nazivaju se halogenima (oni koji tvore soli) zbog toga što izravno s metalima daju soli. U vanjskoj ljusci imaju 7 elektrona pa su izrazito elektronegativni. Reagiraju sa skoro svim metalima i mnogim nemetalima. Reaktivnost im opada porastom atomske mase. Halogeni imaju jak neugodan miris i gore sjajnim plamenom.
U elementarnom stanju halogeni elementi prave dvoatomne molekule. Kako raste volumen atoma, rastu i Van der Waalsove privlačne sile. Tako su pri sobnoj temperaturi fluor i klor plinovi, brom tekućina, a jod i astat čvrste tvari.
tvrdoća → hardness
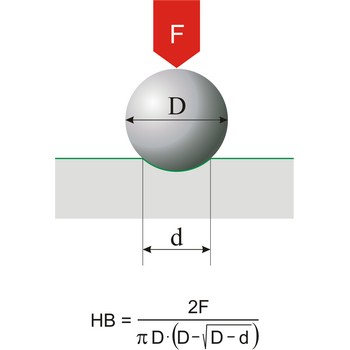
Tvrdoća je otpor materijala prema utiskivanju tijela određene veličine, oblika i poznatog opterećenja. Ova se definicija odnosi na sve tipove skala tvrdoća osim Mohrove skale, koja je zasnovana na otpornosti na grebanje i koristi se uglavnom za minerale. Najčešće korištene skale tvrdoća su: Brinellova (za lijevano željezo), Rockwellova (za lim i toplinski obrađeni čelik) i Knoop (za metale).
teška voda → heavy water
Molekule vode sastavljene su od dva atoma vodika i jednog atoma kisika (H2O). Ako se vodikovi atomi u molekuli vode zamijene s deuterijevim atomima nastat će teška voda (D2O). Deuterij se razlikuje od vodika po tome što ima jedan neutron više u jezgri atoma. Udio teške vode u normalnoj vodi je približno 1:5000 i može se koncentrirati elektrolizom. Teška voda ima i više vrelište (101.4 °C) i više ledište (3.6 °C) od normalne vode. Teška voda je 1.11 puta (20/18=1.11) teža od obične vode.
Citiranje ove stranice:
Generalić, Eni. "Linearni oblik molekule." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav