vitriolno ulje → oil of vitriol
Vitriolno ulje je staro ime za sumpornu kiselinu (H2SO4). U staro vrijeme sumporna kiselina proizvodila se zagrijavanjem zelene galice (lat. vitriol, FeSO4*7H2O) i sakupljanjem kiselih para koje su pri tom nastajale.
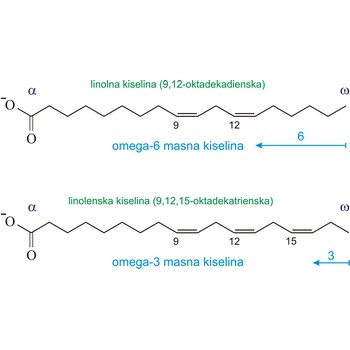
omega-3 masne kiseline → omega-3 fatty acids
Omega-3 masne kiseline su polinezasićene masne kiseline (imaju više od jedne dvostruke veze). Ime omega-3 kaže nam da se prva dvostruka veza nalazi na trećem ugljikom atomu (n-3) od metilnog kraja (-CH3) molekule (omega kraja). Tri najvažnije omega-3 masne kiseline su alfa-linolenska kiselina (ALA, 18:3n-3), eikosapentenska kiselina (EPA, 20:5n-3) i dokosaheksaenska kiselina (DHA, 22:6n-3). ALA se može naći u biljkama a EPA i DHA nalaze se u ribama.
Omega-6 u imenu masne kiseline kaže da se prva dvostruka veza nalazi između šestog i sedmog ugljikovog atoma brojeći od metilenskog kraja masne kiseline (omega kraja).
Onsagerove relacije → Onsager relations
Onsagerove relacije su važan set jednadžbi u termodinamici ireverzibilnih procesa. Onsager je uzeo da postoji linearna ovisnost struja (Ji)o silama (Xj) i to formulirao na sljedeći način:
Koeficijenti Lij nazivaju se fenomenološkim koeficijentima i karakteriziraju uzajamni utjecaj dvaju nepovratnih procesa i i j. Onsager je pretpostavio da su Lij = Lji i da karakteriziraju međusobni utjecaj dvaju nepovratnih procesa i i j. Ovu teoriju je 1931. predstavio norveški kemičar Lars Onsager (1903.-1976.).
optička aktivnost → optical activity
Optička aktivnost je sposobnost kiralnih molekula da zakreću ravninu polariziranog svjetla. Molekule optički aktivnih tvari ne mogu se preklopiti s vlastitom zrcalnom slikom, slično kao lijeva i desna ruka.
optički aktivna tvar → optically active matter
Optički aktivne tvari jesu one tvari koje zakreću ravninu polarizirane svjetlosti ulijevo ili udesno.
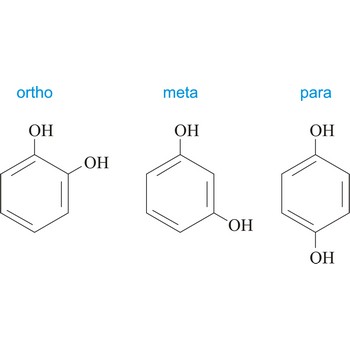
ortho položaj → ortho position
Ortho položaj u organskoj kemiji položaj je u kojem su na benzenovom prstenu vezane dvije skupine u položajima 1 i 2. Upotrebljava se kratica o-, npr. o-hidrokinon je 1,2-dihydroxybenzene.
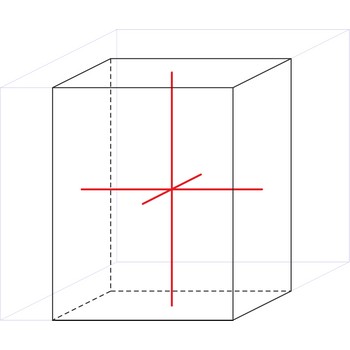
ortorompski kristalni sustav → orthorhombic crystal system
U ortorompskom ili rompskom kristalnom sustavu sve tri kristalografske osi okomite su jedna na drugu i različitih duljina.
a ≠ b ≠ c
α = β = γ = 90°
osmotski tlak → osmotic pressure
Osmotski tlak (Π) jest tlak potreban da se očuva osmotska ravnoteža između otopine i čistog otapala odvojenih membranom propusnom samo za otapalo. U idealnim razrijeđenim otopinama
gdje je cB koncentracija otopljene tvari, R je molarna plinska konstanta a T je temperatura.
Ostwaldov zakon razrjeđenja → Ostwald’s dilution law
Ostwaldov zakon razrjeđenja izraz je za ovisnost molarne provodnosti Λ otopine elektrolita o koncentraciji. To se može napisati kao jednadžba pravca
gdje je c koncentracija, Kc je koncentracijska konstanta ravnoteže, i Λ0 je provodnost kod cΛ = 0. Iz podataka za molarnu provodnost pri raznim koncentracijama može se iz odsječka odrediti Λ0 a iz nagiba pravca Kc. Ovaj zakon je prvi iznio njemački kemičar Wilhelm Ostwald (1853.-1932.).
Ostwaldov proces → Ostwald’s process
Ostwaldov proces je proces kojim se u tri stupnja dobiva nitratna kiselina, u prvom stupnju reagiraju amonijak i kisik (uz platina-rodij kao katalizator) čime nastaje dušikov monoksid i voda
U drugom stupnju dušikov monoksid reagira s kisikom pri čemu nastaje dušikov dioksid
U trećem stupnju otapanjem nastalog dušikovog dioksida u prisustvu zraka dobivamo nitratnu kiselinu
Citiranje ove stranice:
Generalić, Eni. "Clay triangle." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav