koncentrirana otopina → concentrated solution
Koncentrirana otopina je otopina koja sadrži visoku količinu otopljene tvari, ovisno o maksimalno mogućoj količini koja se može otopiti.
acetal → acetal
Acetali su organski spojevi opće formule R2C(OH)OR’ (R’ ≠ H) nastali adicijom alkohola na karbonilnu skupinu aldehida ili ketona. prvobitno se pojam odnosio samo na spojeve izvedene iz aldehida (jedan R = H) ali je poslije proširen da obuhvati i spojeve izvedene iz ketona (nijedan R = H ). Miješani acetali imaju različite R’ skupine. Nastajanje acetala je reverzibilno; acetali mogu u kiseloj sredini hidrolizirati do aldehida (ketona).
Acetal, 1,1-dietoksietan (CH3CH(OC2H5)2), tekućina je ugodna mirisa nastala adicijom etilnog alkohola na acetaldehid. Služi kao otapalo i u organskim sintezama.
Achesonov proces → Acheson process
Achesonov proces je industrijski proces za dobivanje grafita i silicijevog karbida (karborund). Ime je dobio po svom izumitelju, američkom kemičaru Edwardu Goodrichu Achesonu (1856.–1931.). U ovom se procesu, u električnim pećima zagrijavaju (na temperature više od 2500 °C) čisti kvarcni pijesak (SiO2) i fino usitnjeni petrol-koks (C) pri čemu nastaje silicijev karbid prema reakciji:
Proučavajući utjecaj visoke temperature na proizvedeni karborund Acheson je otkrio da pri 4150 °C silicij ispari ostavljajući čisti grafit.
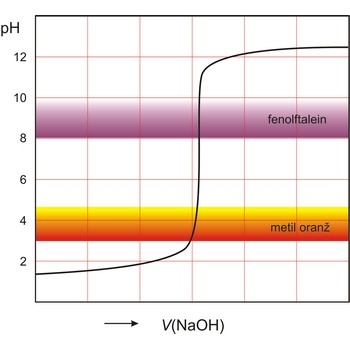
kiselo-bazna titracija → acid-base titration
Kiselo-bazna titracija analitička je tehnika koja se koristi kod volumetrijske analize gdje se kiselina poznate koncentracije koristi pri neutralizaciji lužine poznatog volumena, zatim se utrošeni volumen kiseline koristi da bi se odredila nepoznata koncentracija baze. Prilikom kiselo-bazne titracije koristi se kiselo-bazni indikator da bi se mogla odrediti završna točka titracije.
praskavi pamuk → cracking cotton
Praskavi pamuk je nitroceluloza s visokim sadržajem dušika (oko 13 %), koristi se za proizvodnju bezdimnog baruta.
plin praskavac → fire-damp
Plin praskavac je smjesa od dva volumenska dijela vodika i jednog kisika; zapaljen jako eksplodira, plamen daje visoku temperaturu (2 000 °C).
energija aktivacije → activation energy
Energija aktivacije ili energija aktiviranja reakcije (Ea) energija je koju je potrebno dovesti molekulama da međusobno reagiraju. Da bi molekule kemijski reagirale, moraju se sudariti, ali međusobno mogu reagirati samo one molekule koje imaju veću energiju od energije aktiviranja. U kemijskoj kinetici energija aktivacije je visina potencijalne barijere koja odvaja produkte od reaktanata. Što je energija aktivacije veća, to manji broj molekula može prijeći vrh energetske barijere i reakcija je sporija.
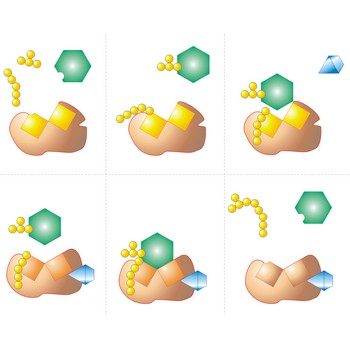
aktivno mjesto → active site
Aktivno mjesto je džep, odnosno udubina na enzimskoj molekuli koja odgovara molekuli reaktanta kao ruka rukavici. Aktivno mjesto smanjuje energiju aktivacije dotične reakcije.
Citiranje ove stranice:
Generalić, Eni. "Visoka peÃâ¡." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav