zeta potencijal → zeta potential
Zeta potencijal (ζ) jest potencijal preko granice faza svih čvrstih tijela i tekućina. Osobitose odnosi na potencijal difuznog sloja iona koji okružuju nabijenu koloidnu česticu, i koji je velikim dijelom odgovoran za stabilnost koloida. Također se naziva i elektrokinetički potencijal.
poluvalni potencijal → half-wave potential
Poluvalni potencijal (E1/2) je potencijal na kojem je struja polarografskog vala jednaka polovici difuzijske struje (id). Kod reverzibilnih sustava poluvalni potencijal karakterističan je za svaku ionsku vrstu pojedinog elementa (ali ovisi o sastavu otopine) pa se E1/2 može koristiti za kvalitativno određivanje (identifikaciju) elektroaktivnih vrsta.
redoks-reakcija → redox reaction
Redoks-reakcije su oksidacijsko-redukcijske reakcije u kojoj se prenosi jedan ili više elektrona. Kada atom, ion ili molekula izgubi jedan ili više elektrona on se oksidirao. Kada atom, ion ili molekula primi jedan ili više elektrona on se reducirao.
redoks-titracija → redox titration
Redoks-titracija (oksidacijsko-redukcijska titracija) je titracija bazirana na redoks-reakciji. Npr. željezo u vodi se može odrediti tako da se otopljeno željezo prevede u Fe2+ i zatim titrira otopinom kalijeva permanganata (KMnO4), koji je jako oksidacijsko sredstvo.
standardni elektrodni potencijal → standard electrode potential
Standardni elektrodni potencijal (E°) (standardni redukcijski potencijl) definiran je mjerenjem relativnih elektrodnih potencijala uz standardne uvjete (aktivitet 1, tlak 101 325 Pa i temperatura 25 °C) prema standardnoj vodikovoj elektrodi. Po konvenciji članak se piše tako da se oksidirani oblik piše prvi. Na primjer,
Elektromotorna sila gornjeg članka je -0.76 V pa je standardni elektrodni potencijal Zn2+|Zn polućelije -0.76 V.
Kada su aktiviteti oksidiranog i reduciranog oblika jednaki 1, tada je logaritamski član u Nernstovoj jednadžbi za elektrodni potencijal jednak nuli i imamo
Lennard-Jonesov potencijal → Lennard-Jones potential
Lennard-Jonesov potencijal (ili 12-6 potencijal) jednostavni je matematički model koji opisuje interakciju dva nevezana neutralna atoma (poznatu kao van der Waalsova interakcija). Predložio ga je 1924. britanski fizičar Sir John Edward Lennard-Jones (1894-1954). Lennard-Jonesov potencijal opisan je slijedećom reakcijom

gdje je: V potencijalna energija između dva atoma ili molekule, ε je dubina bunara i mjera je koliko jako dvije čestice privlače jedna drugu, σ je udaljenost na kojoj je potencijalna energija između dvije čestice jednaka nuli, r je udaljenost dvije čestice mjerena od centra jedne do centra druge čestice.
potencijalna energija → potential energy
Potencijalna energija (Ep) jest energija pohranjena unutar tijela ili sustava kao posljedica mjesta, oblika ili stanja (uključuje gravitacijsku, električnu, nuklearnu i kemijsku energiju). Gravitacijska potencijalna energija je energija povezana sa stanjem razdvojenosti tijela koja se međusobno privlače gravitacijskom silom. Elastična potencijalna energija povezana je sa stanjem sabijenosti ili rastegnutosti elastičnog tijela (poput opruge). Toplinska energija povezana je s nasumičnim gibanjem atoma i molekula u tijelu.
galvanski članak → galvanic celll
Galvanski članak (naponski članak, Voltin članak) jest elektrokemijski članak u kojem se kemijska energija spontano pretvara u električnu. Galvanski članak sastoji se od dva polučlanka, a svaki polučlanak od elektrode uronjene u elektrolit. Elektrolit može biti zajednički za obje elektrode ili različit za svaku elektrodu. Dva elektrolita odvajamo polupropusnom membranom ili ih spajamo elektrolitskim mostom. Ako se elektrode povežu nekim vodičem, elektroni putuju kroz vodič od negativnog pola prema pozitivnom polu.
Danielov članak je primjer galvanskog članka. Sastoji se od bakrene i cinkove elektrode, a kao elektrolit služe otopine bakrova(II) sulfata i cinkova sulfata odijeljene polupropusnom membranom. Kada se elektrode spoje električnim vodičem kroz strujni krug će proteći električna struja. Na negativnom polu (cinkovoj elektrodi) zbiva se proces oksidacije A na pozitivnom polu (bakrenoj elektrodi) zbiva se proces redukcije.
Elektromotornu silu galvanskog članka možemo izračunati iz razlike redoks potencijala tvari koja se reducirala (bakra) i tvari koja se oksidirala (cinka).
Galvanski članak može se shematski prikazati upotrebom okomite crte. Uobičajeno je da se oksidirana vrsta piše s lijeve strane.
Ime je dobila u čast talijanskog znanstvenika i liječnika Luigia Galvania (1737.-1798.).
potenciometrijska titracija → potentiometric titration
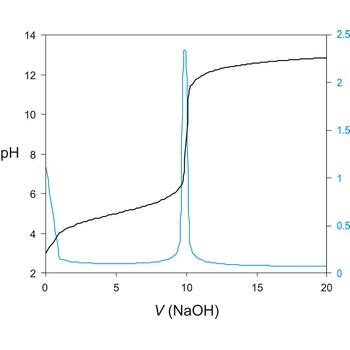
Potenciometrijska titracija je volumetrijska metoda kojom se mjeri potencijal između dvije elektrode (referentne i indikatorske elektrode) kao funkcija dodanog volumena reagensa. Temeljni princip potenciometrijske titracije je određivanje nepoznate koncentracije ispitivane otopine titracijom s nekom standardnom otopinom pri čemu skokovita (nagla) promjena potencijala indikatorske elektrode ukazuje i određuje završnu točku titracije.
Instrumentalno određivanje završne točke ima niz prednosti u odnosu na korištenje indikatora. Vizualno određivanje završne točke opterećeno je subjektivnim faktorima, a ne može se koristiti u mutnim i obojenim otopinama. Potenciometrijske metode određivanja završne točke mogu se primijeniti, ne samo za kiselo-bazne titracije već i kod taložnih, redoks i drugih titracija.
Titracijska krivulja ima karakterističan sigmoidalni oblik. Dio krivulje s maksimalnom promjenom potencijala je ekvivalentna točka titracije. Točku ekvivalencije možemo točnije odrediti iz diferencijalne krivulje ΔE/ΔV gdje maksimum krivulje određuje točku ekvivalencije.
standardna vodikova elektroda → standard hydrogen electrode
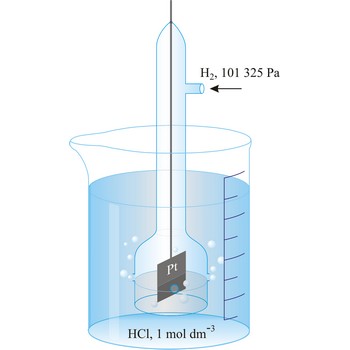
Standardna vodikova elektroda sastoji se od elektrode od spužvaste platine uronjene u otopinu vodikovih iona aktiviteta 1 kroz koju se propušta plinoviti vodik pod tlakom od 101 325 Pa. Standardna vodikova elektroda u članku dogovorno se prikazuje uvijek lijevo
Redoks-potencijal standardne vodikove elektrode, pri svim temperaturama, dogovorno je uzet kao 0.
Citiranje ove stranice:
Generalić, Eni. "Redoks potencijal." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav