klorinitet → chlorinity
Klorinitet (simbol Cl) je definiran kao ukupna količina halida (klorida, bromida i jodida) u 1 kg mora, a da su pri tome jodid i bromid zamijenjeni ekvivalentnom količinom klorida. Kako bi se napravio neovisnim o promjenama atomskih masa halida, klorinitet se danas definira kao masa čistog srebra potrebna da se istalože svi kloridi, bromidi i jodidi pomnožena s 0.37285233. Klorinitet se općenito određuje kako bi se izračunala slanost (salinitet) mora.
Klorinitet se određuje Mohrovom metodom, jednom od najstarijih metoda titracije - uveo ju je 1856. njemački kemičar Karl Friedrich Mohr (1806.-1879.), titracijom uzorka mora sa standardnom otopinom srebrovog nitrata (AgNO3) uz kalijev kromat (K2CrO4) kao indikator.
pri tome se uz AgCl talože još i AgBr i AgI.
Problem kod Mhorove titracije je u tome što srebrov nitrat nije primarni standard. Kako bi ovo izbjegao i omogućio da sva mjerenja saliniteta budu usporediva, predsjednik Međunarodnog povjerenstva za istraživanje mora (ICES, International Council for the Exploration of the Sea), danski fizičar Martin Knudsen (1871.-1949.) definirao je kao standard Normalnu vodu (Eau de mer Normale) stalnog sastava s točno određenim klorinitetom (oko 19.38 ‰). Ova voda je potom korištena za standardizaciju otopine srebrova nitrata. Na taj način sva određivanja kloriniteta referirala su se na isti standard što je omogućilo da svi rezultati budu usporedivi. Upotrebom Normalne vode, Knudsenove pipete i birete za analizu te Hidrografskih tablica dobivali su se rezultati točnosti usporedive onima dobivenim gravimetrijom.
Mjerenjem saliniteta i kloriniteta u devet uzoraka mora iz različitih dijelova svijeta Knudsen je, 1889., došao do empirijske formule za određivanje saliniteta:
Ova formula koristila se do 1962., kada je Zajedničko vijeće za oceanografske tablice i standarde (JPOTS, Joint Panel for Oceanographic Tables and Standards) odredilo novu konstantu proporcionalnosti u Knudsenovoj formuli
ekvivalent → equivalent
Ekvivalent (eq) je jedinica za opisivanje količine kemijske vrste. Nasuprot molu, količina tvari sadržane u jednom ekvivalentu može se mijenjati od reakcije do reakcije.
geokemija → geochemistry
Geokemija je znanost koja proučava kemijski sastav Zemlje. Proučava obilatost pojedinih elemenata i njihovih izotopa, te njihovu distribuciju u okolišu (litosferi, atmosferi, biosferi i hidrosferi).
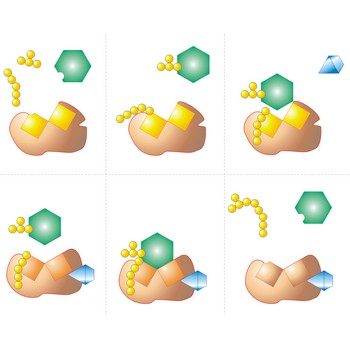
teorija sudara → collision theory
Teorija sudara je teorija koja objašnjava kako se događaju kemijske reakcije i zašto se mijenja brzina reakcije. Da bi se reakcija dogodila moraju se molekule reaktanta sudariti. Samo dio sudara, uspješni sudari, uzrokuje kemijske promjene. Uspješni sudari imaju dovoljno energije (aktivacija energija) u trenutku sudara da prekinu postojeće veze i stvore nove veze, stvarajući reakcijske produkte. Povećavanje koncentracije reaktanata i povišenje temperature povećava broj sudara, odnosno dovodi do povećanja brzine reakcije.
koloidni ion → colloid ion
Koloidni ioni nastaju kada koloidne čestice adsorbiraju određenu vrstu iona iz otopine i nabiju se istovrsnim nabojem. Naboj može potjecati i od kemijske reakcije površine čestice. Koloidne ione nastale adsorpcijom na čestice srebrova klorida možemo prikazati kao
Adsorbirani sloj je monomolekulski (debljine jedne molekule) a koji će koloidni ion nastati, ovisi o tome koji je ion u suvišku. Kako su sada koloidne čestice istoimeno nabijene, dolazi do uzajamnog odbijanja i stabiliziranja koloidne otopine. Naboj koloidne čestice može se ustanoviti elektroforezom.
kondenzacija → condensation
1. Kondenzacija je proces u kojem plin prelazi iz plinovitog u tekuće agregatno stanje, obično je uzrokovana hlađenjem.
2. Kondenzacija u koloidnim sustavima označava proces skupljanja manjih čestica u veće čestice koloidnih dimenzija.
3. Kondenzacija je vrsta kemijske reakcije u kojoj se izdvajaju male molekule kao što su molekule vode, amonijaka, ugljikova dioksida.
korozija → corrosion
Korozija je štetno i nepoželjno trošenje konstrukcijskog materijala kemijskim djelovanjem okoline. Pojam korozije odnosi se i na metalne i na nemetalne konstrukcijske materijale, ali se u užem smislu često primjenjuje samo na metale. Korozija metala prema mehanizmu procesa dijeli se na kemijsku (koroziju u neelektrolitima) i elektrokemijsku (koroziju u elektrolitima).
Kemijska korozija nastaje neposrednim djelovanjem molekula nekog elementa ili spoja na metal pri čemu izravno nastaju korozijski produkti.
Elektrokemijska korozija metala zbiva se u elektrolitima pri čemu dolazi do oksidacije atoma metala u slobodni kation, koji tek sekundarnim procesima daju molekule spoja koji je produkt korozije.
Citiranje ove stranice:
Generalić, Eni. "Kemijska formula." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav