fotokemijska reakcija → photochemical reaction
Fotokemijske reakcije one su reakcije koje se odvijaju pod utjecajem svjetlosti, odnosno pod utjecajem ultraljubičastog, vidljivog i infracrvenog dijela spektra. Na neki sustav može djelovati samo ono zračenje koje taj sustav apsorbira. Fotokemijske reakcije su primjerice fotosinteza, nastajanje fotografije, nastajanje fozgena, nastajanje klorovodika itd.
fotomultiplikator → photomultiplier
Fotomultiplikator (fotomultiplikatorska cijev ili PMT) je svestrani i vrlo osjetljivi detektor elektromagnetnog zračenja u ultraljubičastom, vidljivom i bliskom infracrvenom području elektromagnetskog spektra. Tipični fotomultiplikator sadrži fotoosjetljivu katodu (fotokatodu) iza koje slijede fokusirajuće elektrode, elektrode za pojačavanje (dinode) i elektroda za skupljanje elektrona (anoda) smještene u vakuumsku cijev.
polimorfija → polymorphism
Polimorfija je pojavljivanje čvrste tvari u više inačica s različitim kristalnim strukturama. Različiti polimorfi imaju različite rasporede atoma unutar jedinične ćelije i imaju različita fizikalna svojstva. Prema broju polimorfa razlikujemo dimorfiju, trimorfiju itd. Kalcijev karbonat je dimorfan jer kristalizira heksagonski kao kalcit i rompski kao aragonit. Prevladavajuća kristalna struktura ovisi o temperaturi i tlaku.
Željezo je metal s polimorfnom strukturom. Svaka struktura je stabilna u određenom rasponu temperatura, na primjer, do temperature 912 °C željezo ima bcc kristalnu strukturu (α-željezo ili ferit). U temperaturnom području između 912 C i 1 394 °C kristalizira u fcc kristalnoj rešetki (γ-željezo ili austenit), a pri temperaturi 1 394 °C ponovo dolazi do polimorfne promjene iz fcc u bcc kristalnu strukturu (δ-željezo) koju zadržava do tališta.
Polimorfiju među elementima nazivamo alotropija.
prometij → promethium
Prometij su 1945. godine otkrili J. A. Marinsky, Lawrence Glendenin i Charles D. Coryell (USA). Dobio je ime po Prometeju koji je po grčkoj mitologiji ukrao vatru od bogova. Postoji u dvije alotropske modifikacije. Prometij-145 je najstabilniji izotop i služi kao izvor beta-zračenja. Prometijeve soli svijetle u mraku plavo zelenom svjetlošću. To je otrovan i radiotoksičan metal. Ne pojavljuje se u prirodi. Nastaje kao produkt bombardiranja neodimija s neutronima. Upotrebljava se za izradu nuklearnih baterija gdje osvjetljavajući fotoćeliju proizvodi struju.
radioaktivni indikator → radioactive indicator
Upotrebom odgovarajućih radioaktivnih izotopa mogu se pratiti biokemijski procesi u biljkama, životinjama i ljudima mjereći radioaktivno zračenje primiješanog radioaktivnog indikatora. Umjetni radioaktivni izotopi imaju iste kemijske osobine kao i prirodni izotopi što omogućuje da te prirodne izotope obilježimo primjesom radioaktivnih izotopa i tako slijedimo put tih elemenata tijekom kemijske reakcije. Jedan od najvažnijih radioaktivnih indikatora jest radioaktivni ugljik 14C.
radij → radium
Radij su 1898. godine otkrili Marie Curie (Poljska) i Piere Curie (Francuska). Ime je dobio prema latinskoj riječi radiare što znači zračiti ili sjajiti. To je sjajni srebrni, mekani radioaktivni metal. Vrlo brzo reagira s kisikom iz zraka i vodom. To je visoko radiotoksičan metal koji je kancerogen ako se proguta, udiše ili izlaže njegovom zračenju. Sav radij u prirodi potječe od radioaktivnog raspada težih elemenata, osobito urana. Uranove rude su stoga, glavni izvor radija.
romboedarski kristalni sustav → rhombohedral crystal system
U romboedarskom ili trigonskom kristalnom sustavu sve tri kristalografske osi iste su duljine. Ni jedna od triju osi nije okomita na bilo koju drugu os.
a = b = c
α = β = γ ≠ 90°
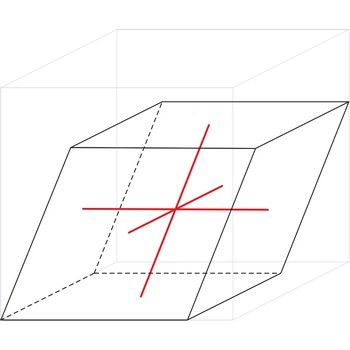
romboedarska rešetka → rhombohedral lattice
Romboedarska ili trigonska rešetka ima po jedan čvor kristalne rešetke u svakom uglu jedinične ćelije. Kristalografski vektori jedinične ćelije su a = b = c a kutovi među njima α=β=γ≠90°.
samarij → samarium
Samarij je 1879. godine otkrio Paul Emile Lecoq de Boisbaudran (Francuska). Ime je dobio po mineralu samariskitu nazvanom tako u čast ruskog rudarskog inženjera Samarskog. To je srebrno bijeli metal koji je stabilan na suhom zraku. Oksidni sloj se formira na površini ako je izložen vlažnom zraku. Metal se sam zapali na zraku ako se zagrije na 150 °C. Glavni izvor teških lantanoida je gadolinit (Y, Ce, Cr, Be, Fe silikat), euksenit (sadrži Y, Ce, Er, Nb, Ti, U) i ksenotim (YPO4 s nešto Th i lakih lantanoida). Nalaze se i u monacitnim pijescima. Koristi se za izradu stakla koje apsorbira infracrveno zračenje, za izradu lasera i studijskih reflektora i kao apsorber neutrona u nuklearnom reaktoru. Upotrebljava se za izradu permanentnih magneta s najvećim otporom prema demagnetizaciji od svih poznatih materijala.
sekunda → second
Sekunda (s) je SI jedinica za vrijeme.
To je trajanje 9 192 631 770 perioda zračenja koje odgovara prijelazu između dvaju hiperfinih nivoa (od F = 4, mF = 0 do F = 3, mF = 0) osnovnog stanja atoma cezija 133 (133Cs). Periodu definiramo kao vrijeme potrebno da svjetlost prevali put koji odgovara jednoj valnoj duljini.
Citiranje ove stranice:
Generalić, Eni. "Gama-zračenje." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav