zakon o određenom sastavu → law of definite composition
Zakon o određenom sastavu kaže da se elementi u danom spoju uvijek spajaju u istom omjeru masa. Ovaj zakon je osnovni zakon u definiranju kemijskih spojeva.
konstanta ravnoteže → equilibrium constant
Konstanta ravnoteže (K) prvi put se pojavljuje u zakonu o djelovanju masa koji su 1863. formulirali norveški kemičari C.M. Guldberg i P. Waage. Reverzibilna kemijska reakcija prikazana jednadžbom
u ravnoteži je onda kada je brzina napredne reakcije jednaka brzini povratne reakcije.
Konstanta ravnoteže definirana je odnosom ravnotežnih aktiviteta produkata i reaktanata
Kod praktičnih mjerenja često se aktiviteti zamjenjuju koncentracijama
Za reakcije u plinskoj fazi umjesto koncetracija upotrebljavaju se parcijalni tlakovi
Termodinamička konstanta K nema jedinicu, dok jedinica za Kp i Kc ovisi o broju molekula koje se pojavljuju u stehiometrijskoj jednadžbi (a, b, c i d).
Veličina konstante ravnoteže ovisi o temperaturi. Ako je napredna reakcija egzotermna, konstanta ravnoteže smanjuje se povećanjem temperature. Što je veća konstanta ravnoteže neke kemijske reakcije, to je ravnoteža više pomaknuta na stranu stvaranja produkata reakcije. Položaj uspostavljene ravnoteže može se mijenjati, ali ne i konstanta. Sustav u ravnoteži brani se od promjene tako da nastoji poništiti vanjski utjecaj (Le Chatelierov princip).
Konstanta ravnoteže kemijske reakcije izravno je proporcionalna promjeni standardne Gibbsove slobodne energije
Le Chatelierov princip → Le Chatelier’s principle
Promijene li se vanjski uvjeti sustava, koji se nalazi u ravnoteži, tada se ravnoteža pomiče u smjeru ponovnog uspostavljanja prvobitnih uvjeta. Princip je prvi put iznio 1888. francuski kemičar Henri Le Chatelier (1850.-1936.).
tekući kristal → liquid crystal
Tekući kristali su tvari u fizikalnom stanju koje je između kristalnog stanja i taline. To stanje se zove mezofaza, a nastaje pri točki taljenja. Najvažnije mezofaze su nematična, holesterična i smektična koje se razlikuju po molekulskim orijentacijama.
fugacitet → fugacity
Fugacitet (f) je termodinamička funkcija koja se koristi umjesto parcijalnih tlakova kod reakcija u kojima sudjeluju realni plinovi. Za neku komponentu smjese definiran je kao
gdje je μ kemijski potencijal.
Fugacitet plinova jednak je tlaku koji bi plin imao da je idealan. Fugacitet tekućina i čvrstih tvari jednak je fugacitetu para s kojima su u ravnoteži. Aktivitet je odnos fugaciteta i fugaciteta standardnog stanja.
gama-zračenje → gamma radiation
Gama-zračenje je elektromagnetsko zračenje vrlo kratkih valnih duljina (0.001 nm - 0.1 nm) i vrlo velikih energija od 10-15 J do 10-10 J (od 10 keV to 10 MeV). Gama-zrake se javljaju kao posljedica uspostavljanja energetske ravnoteže u jezgri nakon izbacivanja α ili β-čestica.
Gama-zrake su jako prodorne i apsorbiraju se u gustim materijalima kao što su olovo i uran. Izlaganje gama-zračenju može biti smrtonosno.
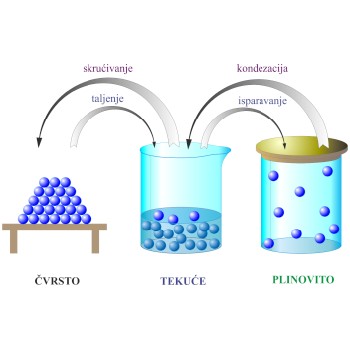
ukapljivanje plinova → gas liquefying
Da bi došlo do prijelaza plina u tekuće stanje, potrebno je ili sniziti temperaturu ili smanjiti volumen ili povećati tlak. Iznad kritične temperature nije moguće ukapljiti plin. Za ukapljivanje zraka Lindeovim postupkom koristi se prigušni ili Joule-Thomsonov efekt. Postupak se sastoji u tome da se stlačeni zrak u kompresoru ohladi rashladnom vodom. Tako ohlađeni zrak ekspandira na niži tlak u prigušnom ventilu pri čemu se ohladi, vraća se u kompresor i usput hladi zrak koji će se ekspandirati. Ponavljanjem tog postupka zrak se toliko ohladi da prijeđe u tekuće stanje.
Paulijev princip zabrane → Pauli exclusion principle
Raspodjela elektrona u pojedinim kvantnim nivoima određena je Paulijevim principom zabrane, koji kaže da u atomu ne mogu dva elektrona imati iste vrijednosti sva četiri kvantna broja n, l, ml i ms. Švicarski fizičar rođen u Austriji Wolfgang Ernst Pauli (1900.-1958.) otkrio je taj princip 1925.
Citiranje ove stranice:
Generalić, Eni. "50 states program guide." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav