željezo → iron
Željezo je poznato od davnih vremena (~2500. godine prije Krista). Simbol elementa dolazi od latinskog naziva za željezo - ferrum. To je sjajni, srebrni, tvrdi i krti metal. Zajedno s kobaltom i niklom čini trijadu željeza. Izložena površina brzo korodira naročito u vlažnom zraku i pri povišenoj temperaturi. Na površini se stvara crveno-smeđi oksid (hrđa). Otapa se u neoksidirajućim kiselinama. U koncentriranoj sulfatnoj i nitratnoj kiselini željezo se pasivira. Feromagnetično je sve do 768 °C. Željezo je najvažniji metal. Proizvodnja mu je veća nego svih ostalih metala zajedno. Glavne rude željeza su magnetit (Fe3O4), hematit (Fe2O3), limonit (FeOOH) i siderit (FeCO3). Željezo se dobiva redukcijom oksida željeza koksom u visokim pećima. Kao čisti metal se malo upotrebljava već se legira s drugim metalima u razne vrste čelika, koji su osnova moderne civilizacije.
Kirchoff, Gustav → Kirchoff, Gustav
Gustav Kirchoff (1824.-1887.) njemački je fizičar koji je, zajedno s njemačkim kemičarom Robertom Bunsenom (1811.-1899.), položio temelje spektralne analize. On je shvatio da su Fraunhoferove linije u spektru Sunca nastale apsorpcijom svjetla elementima u Sunčevoj atmosferi. Kombinacijom Bunsenovog plamenika i staklene prizme (Bunsen-Kirchhoff spektroskop) zajedno s Bunsenom otkrio je cezij (1860.) i rubidij (1861.).
laktoza → lactose
Laktoza (mliječni šećer) je didsaharid koji se sastoji od jedne molekule glukoze povezane s galaktozom β(1→4)-glikozidnom vezom. Laktoza je beta acetal. Javlja se samo u mlijeku sisavaca gdje je ima o 4 % do 7 %. Netolerancija na laktozu česta je bolest koja rezultira proljevom, bolovima u trbuhu i nadutošću a uzrokovana je smanjenom aktivnošću enzima laktaze.
Laktoza je, kao i celebioza i maltoza, reducirajući šećer. Svi reducirajući šećeri pokazuju mutarotaciju kada se otope u vodi. Ravnotežna smjesa pri 20 °C sastoji se od 62.7 % β-laktoze (β-D-galaktopiranozil-(1→4)-β-D-glukopiranoze) i 37.3 % α-laktoze (β-D-galaktopiranozil-(1→4)-α-D-glukopiranoze).
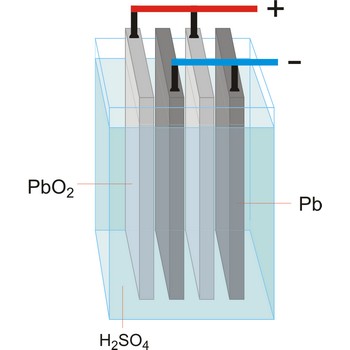
olovni akumulator → lead-acid battery
Olovni akumulator je naprava koja koristi reverzibilne kemijske reakcije za spremanje električne energije. Godine 1859. francuski fizičar Gaston Planté osmislio je prvi olovni akumulator koji se sastojao od olovnih ploča uronjenih u razrijeđenu sumpornu kiselinu. Olovo uronjeno u sulfatnu kiselinu presvuče se slojem olovo(II) sulfata. Ako se kroz ovaj sustav propušta istosmjerna struja dolazi na elektrodama do slijedećih reakcija:
Tako je dobiven izvor struje napona 2 V, koji je poznat kao olovni akumulator. Sam proces pretvaranja električne energije u kemijsku naziva se punjenje akumulatora.
Spajanjem polova olovnog akumulatora u strujni krug na elektrodama se dešavaju slijedeće reakcije:
Proces kojim se kemijska energija pretvara u električnu naziva se pražnjenjem akumulatora.
Olovni akumulatori imaju nisku cijenu, relativno velik napon po ćeliji, malen unutrašnji otpor i mogu dati velike jakosti struje u kratkom vremenu. Mane su mu otrovnost olova, velika masa i pojava samopražnjenja.
lutecij → lutetium
Lutecij su 1907. godine otkrili neovisno jedan o drugom Georges Urbain (Francuska) i Carl Auer von Welsbach (Austrija). Ime je dobio po latinskom nazivu za Pariz - Lutetia. To je srebrno bijeli metal. Relativno je stabilan u suhom zraku. Topljiv je u kiselinama. Glavni izvor teških lantanoida je gadolinit (Y, Ce, Cr, Be, Fe silikat), euksenit (sadrži Y, Ce, Er, Nb, Ti, U) i ksenotim (YPO4 s nešto Th i lakih lantanoida). Nalaze se i u monacitnim pijescima. Koristi se za poboljšavanje mehaničkih svojstava nehrđajučih čelika i kao katalizator kod krekiranja nafte.
makromolekule → macromolecule
Makromolekule su molekule visoke relativne molekularne mase (preko 10 000), čija se struktura sastoji od višestrukog ponavljanja molekula niske relativne molekularne mase. Osim u sintetskim polimerimerima makromolekule se mogu naći i u prirodnim polimerima (ugljikohidratima, lipidima, bjelančevinama itd.). Celuloza je prirodni polimer (polisaharid) nastao spajanjem stotina, ponekad i tisuća molekula glukoze.
mangan → manganese
Mangan je 1774. godine otkrio Johann Gahn (Švedska). Ime je dobio od latinske riječi magnes što znači magnet jer se smatralo da je piroluzit (MnO2) - magnesia nigra vrsta magnezita. To je sivo-bijeli metal sličan željezu ali tvrđi i krtiji. Onečišćeni oblik je reaktivan. Izložena površina se oksidira. Otapa se u razrijeđenim kiselinama oslobađajući vodik. Udisanje manganova praha, para ili spojeva, naročito viših oksida može biti smrtonosno. Mangan je po rasprostranjenosti u Zemljinoj kori deseti element. U prirodi se pojavljuje u obliku manganita(Mn2O3·H2O), piroluzita (MnO2), hausmanita (Mn3O4), rodokrosita (MnCO3) i psilomelana (BaMn9O16(OH)4). Elementarni mangan se može dobiti redukcijom rude s aluminijem. Kao feromangan troši se u velikim količinama u metalurgiji. Mangan čeliku izvanredno povećava tvrdoću i otpornost na trošenje, te se od njega izrađuju željezničke tračnice i čeljusti drobilica.
molibden → molybdenum
Molibden je 1778. godine otkrio Carl William Scheele (Švedska). Ime je dobio od grčke riječi molibdos što znači olovo. To je sjajni, srebrni, vrlo tvrdi metal ali mekši od wolframa. Može se dobiti i u obliku tamno sivog do crnog praha. Otporan je na otopine i taline lužina, a ne otapa se ni u hladnim kiselinama koje nemaju oksidacijsko djelovanje. U Zemljinoj kori ima ga otprilike sto puta manja od kroma. Glavne rude molibdena su molibdenit (MoS2), powelit (CaMoO4) i vulfenit (PbMoO4). Mnogo molibdena se dobiva kao nusproizvod kod dobivanja bakra. Najviše se primjenjuje u metalurgiji za legiranje čelika koji se upotrebljavaju za izradu brzoreznih alata. Već i mali postotak molibdena daje čeliku veliku tvrdoću koja se zadržava i pri visokim temperaturama.
niobij → niobium
Niobij je 1801. godine otkrio Charles Hatchett (Engleska). Ime je dobio po Tantalovoj kćeri Niobi iz grčke mitologije zbog velikih teškoća kod njegovog izdvajanja. Nazivan je još i kolumbij. To je srebrni, blistavi mekani metal čija se izložena površina prevuče se oksidnim filmom. Oksidira se kada se zagrije iznad 200 °C. U prirodi ga ima kao i nikla a javlja se zajedno s tantalom u rudama tantalitu, niobitu ili kolumbitu ((Fe, Mn)[(Nb, Ta)O3]2). Upotrebljava se za proizvodnju specijalnih antikorozivnih čelika, za izradu elektroda za elektrozavarivanje.
dekapiranje → pickling
Dekapiranje je čišćenje kovina, uglavnom čeličnih limova, od okujine i rđe, uronjavanjem u razrijeđenu sumpornu (w(H2SO4) = 10 %) ili solnu kiselinu pri određenoj temperaturi (80 °C). Otopini se dodaje inhibitor radi sprječavanja piting korozije metala.
Citiranje ove stranice:
Generalić, Eni. "Bunsen’s cell." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav