energija → energy
Energija (E, U) je karakteristika sustava i definirana je kao sposobnost sustava da vrši rad. Jedinica za energiju je džul (J).
Unutrašnja energija tijela zbir je potencijalne i kinetičke energije atoma i molekula koji ga sačinjavaju.
Potencijalna energija jest energija pohranjena unutar tijela ili sustava kao posljedica mjesta, oblika ili stanja (uključuje gravitacijsku, električnu, nuklearnu i kemijsku energiju).
Kinetička energija jest energija kretanja i za tijelo mase m koje ima brzinu v, iznosi mv2/2. Doprinos kinetičke energije je mnogo veći kod plinova, čije molekule imaju vrlo veliku slobodu kretanje, nego kod tekućina i čvrstih tvari.
U izoliranom sustavu energija se može pretvarati iz jednog oblika u drugi, ali ukupna energija ostaje konstantna.
freon → freon
Freoni ili CFC (chlorofluorocarbon) sintetički su spojevi sastavljeni od ugljika, klora i fluora te imaju široku primjenu. Nalazimo ih u rashladnim sustavima hladnjaka i zamrzivača, u sprejevima i tekućinama za čišćenje, a upotrebljavaju se i kao "potisno sredstvo" pomoću kojih se prave pjenasti materijali (stiropor). Oslobađaju atome klora s neparnim brojem elektrona, a oni nastaju cijepanjem molekula uz pomoć sunčeve radijacije valne duljine manje od 450 nm. Sunčevo zračenje daje energiju za cijepanje molekula klora na vrlo aktivne atome klora. Naglo oslobođeni aktivni klor, koji se u obliku molekula nakupljao cijele zime, tj. pod uvjetima niske temperature i smanjene količine sunčeve energije, počinje uništavati molekule ozona. To se događa tako dugo dok se ne "isprazne zalihe" nagomilanog klora, što obično traje oko 6 tjedana. Ako u atmosferu dospije više atoma klora posredstvom freona, onda se to razdoblje produži. Nakon toga uspostavlja se prirodna ravnoteža izgradnje i razgradnje ozona. Inače, freoni nisu aktivni u donjoj atmosferi.
fuleren → fullerene
Fuleren (puno ime, buckminsterfullerene) alotropska je modifikacija ugljika koja se sastoji od 60 ugljikovih atoma u obliku nogometne lopte. Postoje fulereni sačinjeni od različitog broja ugljikovih atoma i različitih veličina. Ugljikovi atomi u fulerenskoj molekuli raspoređeni su unutar peterokuta i šesterokuta. Fulerene su otkrili R.F. Curl Jr., H.W. Kroto i R.E. Smalley. Za ovo otkriće dodijeljena im je Nobelova nagrada za kemiju, 1996. godine.
glutaminska kiselina → glutamic acid
Glutaminska kiselina spada u negativno nabijene aminokiseline. To je jedna od dvije aminokiseline koje sadrže karbonsku kiselinu u pobočnom lancu. Kao i sve nabijene aminokiseline i ova kiselina se često nalazi na površini bjelančevine utječući na njenu topljivost i ionski karakter. Asparaginska i glutaminska kiselina igraju važnu ulogu u aktivnim centrima enzima. Glutaminska kiselina se često naziva i glutamat jer je pri fiziološkom pH karboksilna kiselina disocirana u svoj anionski oblik. Glutaminska kiselina nije esencijalna kiselina jer ljudski organizam svu potrebnu kiselinu može sintetizirati iz drugih aminokiselina.
- Kratice: Glu, E
- IUPAC ime: 2-aminopentanska dikiselina
- Molekularna formula: C5H9NO4
- Molekularna masa: 147.13 g/mol
glukoza → glucose
Glukoza (grožđani šećer, krvni šećer) ugljikohidrat je iz skupine monosaharida ili jednostavnih šećera kemijske formule C6H12O6. Stari naziv dekstroza potječe od toga što glukoza zakreće ravninu polarizirane svjetlosti u desno. Prema broju ugljikovih atoma u svojoj molekuli glukoza je heksoza, a prema funkcionalnoj skupini aldoza (aldoheksoza). Glukoza je najrasprostranjeniji šećer u prirodi. Slobodna se nalazi u raznom voću i medu a vezana u disaharidima (saharozi, maltozi, laktozi), polisaharidima (škrobu, glikogenu, celulozi) i raznim drugim spojevima. Kod čovjeka se može naći slobodna u krvi ili kao rezerva pohranjena u jetri i mišićima u obliku glikogena.
Glukozu sintetiziraju biljke procesom fotosinteze i pohranjuju u polimernom obliku kao škrob. U probavnom sustavu škrob se hidrolizira u glukozu koja se zatim iskorištava u stanicama za dobivanje energije. Ukupno se iz jedne molekule glukoze može dobiti 36 molekula ATP-a.
Zbog tetraedarskih kutova koje čine veze među ugljikovim atomima, molekula glukoze može zauzeti takvu konformaciju da hidroksilna skupina vezana na petom ugljikovom reagira s karbonilnom skupinom pri čemu nastaje poluacetal, odnosno šesteročlani heterociklički prsten. Time se javlja još jedan asimetrični centar na atomu C-1, tako da D-glukoza može postojati u dva oblika, kao α-D-glukopiranoza i β-D-glukopiranoza. Ta su dva ciklička oblika u ravnoteži, tj. oni mogu preći jedan u drugog preko aldehidnog oblika.
površinska napetost → surface tension
Površinska napetost (σ) mjera je za silu kojom bi valjalo djelovati na molekule koje se nalaze na površini tekućine kako bi pokazivale jednaku silu međudjelovanja kao molekule u unutrašnjosti tekućine. Uslijed površinske napetosti tekućina se skuplja u kapljice koje najčešće imaju oblik kugle.
teorija valentne veze → valence bond theory
Teorija valentne veze jest teorija koja objašnjava oblik molekule pomoću preklapanja polupopunjenih atomskih orbitala ili polupopunjenih hibridiziranih orbitala.
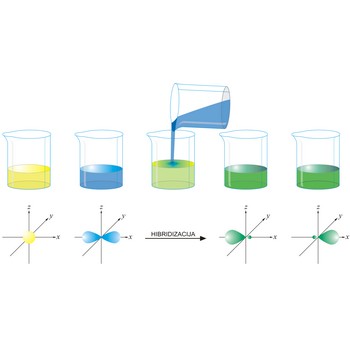
hibridizacija → hybridization
Hibridizacija atomskih orbitala je postupak u kojem se linearnim kombiniranjem valnih funkcija energijski bliskih orbitala stvaraju nove hibridne valne funkcije. Novonastale orbitale su hibridi originalnih i imaju svojstva (oblik, veličinu i energiju) koja se nalaze negdje između svojstava orbitala iz kojih su nastale.
Citiranje ove stranice:
Generalić, Eni. "Linearni oblik molekule." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav