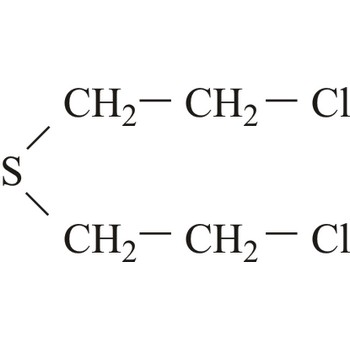vakuum destilacija → vacuum distillation
Vakuum destilacija je destilacija pri sniženom tlaku. Snižavanjem tlaka snižava se temperatura vrelišta pa je moguća destilacija tvari koje bi se razgradile pri povišenoj temperaturi.
tlak pare → vapour pressure
Tlak pare je tlak plina koji je u ravnoteži s tekućinom (ili, ponekad, čvrstim tijelom) pri određenoj temperaturi.
talište → melting point
Talište je temperatura pri kojoj čvrsta tvar prelazi u tekuće stanje pri normalnom tlaku.
Mnogo točnija definicija tališta (ili ledišta) jest da je to temperatura pri kojoj su čvrsta i tekuća faza neka tvari pri određenom tlaku u ravnoteži. Čiste tvari, za razliku od smjesa, imaju oštro definirano talište karakteristično za tu tvar. Hoće li se koristiti naziv talište ili ledište, ovisi o tome da li se tvar zagrijava ili hladi.
živa → mercury
Živa je poznata od davnih vremena (~1500. godine prije Krista). Ime je dobila od latinske riječi hydrargyrum što znači tekuće srebro. To je sjajni, srebrno bijeli metal. Pri sobnoj temperaturi je tekućina. Loše vodi toplinu i električnu struju. Stabilna je na zraku. Ne reagira s lužinama i većinom kiselina. Otapa se samo u oksidirajućim kiselinama. Tekuća živa otapa mnoge metale dajući amalgame. Ovisno o količini otopljenog metala, amalgami mogu biti tekući ili čvrsti. Živine pare su vrlo otrovne. Lako se resorbira čak i preko nepokrivenih dijelova kože. Imaju kronični kumulativni efekt. Organski spojevi žive, kao što je metil-živa, su također jaki otrovi. U prirodi žive ima dvadesetak puta više nego kadmija. Može se pronaći samorodna ili u mineralu cinabaritu (HgS). Klor-alkalne elektrolize su najveći potrošači žive gdje se živa upotrebljava kao katoda kod elektrolize, zbog velikog prenapona vodika na njoj i stvaranja amalgama s produktom. Sa živom se pune termometri, barometri ili se izrađuju lampe koje isijavaju svjetlost bogatu ultraljubičastim zrakama.
metal → metal
Metali ili kovine čine više od dvije trećine svih elemenata koji se mogu naći u prirodi. Od 114 poznatih elemenata, samo 17 su nemetali, 7 su polumetali a ostalih 89 mogu se svrstati u metale.
Metali su neprozirni, imaju karakterističan metalni sjaj, dobri su vodiči topline i električne struje. Električna vodljivost metala općenito opada porastom temperature.
Većina se metala može dobro kovati i istezati. Na sobnoj su temperaturi svi, osim žive, u čvrstom stanju. Mogu se koristiti u čistom stanju, ali se češće miješaju s drugim metalima i nemetalima u legure.
molibden → molybdenum
Molibden je 1778. godine otkrio Carl William Scheele (Švedska). Ime je dobio od grčke riječi molibdos što znači olovo. To je sjajni, srebrni, vrlo tvrdi metal ali mekši od wolframa. Može se dobiti i u obliku tamno sivog do crnog praha. Otporan je na otopine i taline lužina, a ne otapa se ni u hladnim kiselinama koje nemaju oksidacijsko djelovanje. U Zemljinoj kori ima ga otprilike sto puta manja od kroma. Glavne rude molibdena su molibdenit (MoS2), powelit (CaMoO4) i vulfenit (PbMoO4). Mnogo molibdena se dobiva kao nusproizvod kod dobivanja bakra. Najviše se primjenjuje u metalurgiji za legiranje čelika koji se upotrebljavaju za izradu brzoreznih alata. Već i mali postotak molibdena daje čeliku veliku tvrdoću koja se zadržava i pri visokim temperaturama.
plikavac → mustard agent
Plikavci su dobili ime zbog sličnosti rana uzrokovanih onima koje izazivaju opekline. Međutim, plikavci također uzrokuju i velika oštećenja očiju, dišnog sustava i unutrašnjih organa. Uobičajeni plikavac (iperit), 1,1-tio-bis-[2-kloroetan], reagira s velikim brojem bioloških molekula. Učinak plikavaca javlja se sa zadrškom: prvi simptomi se javljaju između 2 i 24 sata nakon izloženosti. Pri sobnoj temperaturi plikavci su tekućine niske hlapljivosti i stabilne su tijekom skladištenja.
Citiranje ove stranice:
Generalić, Eni. "Critical temperature." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav