kvadratna planarna geometrija molekule → square planar molecular geometry
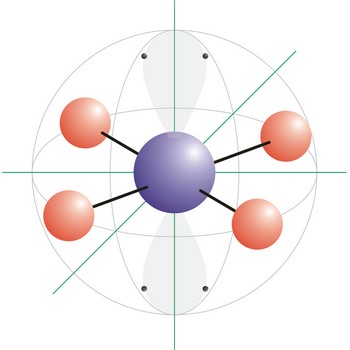
Kvadratna planarna geometrija molekule onaj je oblik molekule kod kojeg su četiri veze i dva slobodna elektronska para vezani na centralni atom molekule. Ksenonov tetraflurid (XeF4) primjer je kvadratne građe molekule. Nepodijeljeni elektronski parovi smještaju se u dva nasuprotna vrha oktaedra a fluorovi atomi u preostala četiri tvoreći kvadrat oko ksenona. Oktaedarski raspored elektronskih orbitala posljedica je sp3d2 (ili d2sp3) hibridizacije na centralnom atomu.
kvadratna piramidalna geometrija molekule → square pyramidal molecular geometry
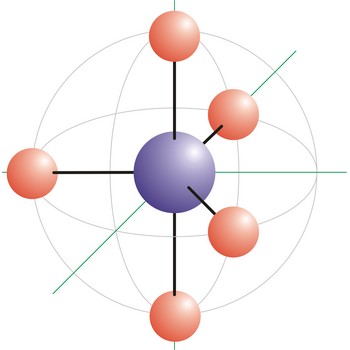
Kvadratna piramidalna geometrija molekule onaj je oblik molekule kod kojeg su pet veza i jedan slobodan elektronski par vezani na centralni atom molekule. Bromov pentafluorid (BrF5) primjer je molekule koja ima geometriju kvadratne piramide. Smještaj nepodijeljenog elektronskog para potpuno je proizvoljan jer su svih šest elektronskih skupina ekvivalentne. Oktaedarski raspored elektronskih orbitala posljedica je sp3d2 (ili d2sp3) hibridizacije na centralnom atomu.
superkritična fluidna kromatografija → supercritical fluid chromatography
Superkritična fluidna kromatografija (SFC) je hibridna tehnika plinske i tekućinske kromatografije. Važnost SFC je u tome što dopušta razdvajanje i određivanje skupina spojeva koje se uobičajeno ne mogu odrediti niti plinskom niti tekućinskom kromatografijom. Spojevi koji se određuju su ili neisparivi ili osjetljivi na povišenu temperaturu tako da se ne može upotrijebiti plinska kromatografija ili nemaju funkcionalnih grupa koje je moguće odrediti tekućinskom kromatografijom. SFC se može primijeniti za određivanje različitih materijala uključujući prirodne spojeve, droge, hranu, pesticide, herbicide, goriva i eksplozive.
T-oblik geometrije molekule → T-shaped molecular geometry
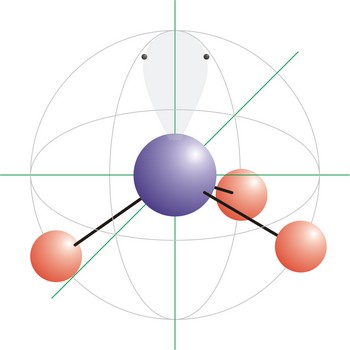
T-oblik molekule imaju molekule koje oko centralnog atoma imaju tri veze i 2 slobodna elektronska para. Atomi vezani na centralni atom leže na krajevima slova T s kutovima od 90° između njih. Elektronske orbitale usmjerene u vrhove trigonske bipiramide posljedica su sp3d (ili dsp3) hibridizacije na centralnom atomu. ICl3 ima T-oblik molekule.
tetraedarska geometrija molekule → tetrahedral molecular geometry
Tetraedarska geometrija molekule onaj je oblik kod kojeg u molekuli postoje četiri veze na centralnom atomu bez slobodnih elektronskih parova. Atomi vezani na centralni atom leže na vrhovima tetraedra s kutom od 109.5° između njih. Tetraedarski raspored elektronskih orbitala posljedica je sp3 hibridizacije na centralnom atomu. Npr. amonijev ion (NH4+) i metan (CH4) imaju tetraedarsku geometriju molekule.
trigonska bipiramidalna geometrija molekule → trigonal bipyramidal molecular geometry
Trigonska bipiramidalna geometrija molekule oblik je molekule kod kojeg je na centralni atom vezano pet veza bez ijednog slobodnog elektronskog para. Tri veze su raspoređene u ekvatorijalnoj ravnini atoma pod kutom od 120° svaka, a druge dvije su na osi centralnog atoma. Aksijalne veze su pod pravim kutom u odnosu na ekvatorijalne veze. Elektronske orbitale usmjerene u vrhove trigonske bipiramide posljedica su sp3d (ili dsp3) hibridizacije na centralnom atomu. Molekula PCl5 ima trigonsku bipiramidalnu geometriju.
trigonska planarna geometrija molekule → trigonal planar molecular geometry
Trigonska planarna geometrija molekule onaj je oblik kod kojeg su tri veze vezane na centralni atom u molekuli bez ijednog slobodnog para elektrona. Veze su raspoređene u ekvatorijalnoj ravnini s međusobnim kutovima od 120°. Elektronske orbitale usmjerene prema vrhovima trokuta posljedica su sp2 hibridizacije na centralnom atomu. Karbonatni ion (CO32-) ima trigonsku planarnu geometriju molekule.
trigonska piramidalna geometrija molekule → trigonal pyramidal molecular geometry
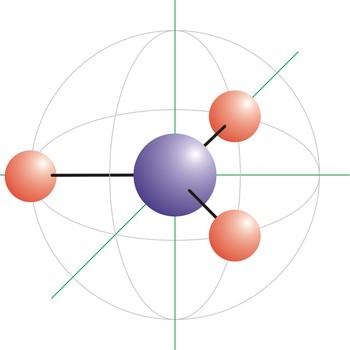
Trigonska piramidalna geometrija molekule onaj je oblik molekule kod kojeg su tri veze i jedan slobodan elektronski par vezani na centralni atom molekule. Tetraedarski raspored elektronskih orbitala posljedica je sp3 hibridizacije na centralnom atomu. Molekula amonijaka (NH3) ima trigonsku piramidalnu geometriju.
dipolarni ion → zwitterion
Dipolarni ili dvojni ion (zwitterion), poznat i kao unutarnja sol, jest ion koji ima pozitivan i negativan naboj na različitim mjestima iste molekule. Kako ion na sebi istovremeno ima suprotne naboje električki je neutralan. Dipolarni ioni nastaju iz spojeva koji u svojim molekulama imaju i kisele i bazne skupine (amfoliti).
Sve aminokiseline koje se mogu naći u bjelančevinama (proteinima) su amfoliti je sadrže kiselu karboksilnu skupinu (-COOH) i baznu amino skupinu (-NH2). Aminokiseline u čvrstom stanju nalaze se u obliku dipolarnog iona. Dodatkom kiseline u otopinu koja sadrži dipolarne ione aminokiseline karboksilatna skupina prima proton (H+) i aminokiselina postaje pozitivno nabijena. Dodatkom lužine amino skupina gubi proton pri čemu aminokiselina postaje negativno nabijena.
Citiranje ove stranice:
Generalić, Eni. "Toyota hybrid nz." Englesko-hrvatski kemijski rječnik & glosar. 29 June 2022. KTF-Split. {Datum pristupa}. <https://glossary.periodni.com>.
Glosar
Periodni sustav